Niewydolność serca
Hiponatremia w codziennej pracy kardiologa
Michał Kacprzak, Marzenna Zielińska
Wprowadzenie
Hiponatremia, definiowana jako zmniejszenie stężenia jonów sodu [Na+] w surowicy poniżej 135 mmol/l, jest najczęstszym zaburzeniem elektrolitowym występującym w praktyce klinicznej, spotykanym u około 20-30% hospitalizowanych pacjentów. Ryzyko jej wystąpienia wzrasta już po 40 r.ż. i jest ponad 5-krotnie większe u osób powyżej 81 r.ż. [1,2]. Liczne badania wykazały, że wiąże się ona z wyraźnie większą śmiertelnością, chorobowością i dłuższą hospitalizacją, zwłaszcza u chorych z niewydolnością serca, marskością wątroby i chorobami neurologicznymi. Prawidłowe diagnozowanie hiponatremii, uwzględniające jej różne postacie i przyczyny, jest niezbędną umiejętnością w codziennej pracy kardiologa klinicysty.
Patogeneza hiponatremii
W warunkach fizjologicznych objętość przestrzeni pozakomórkowej i osmolalność osocza utrzymywane są dzięki ścisłej kontroli stężenia sodu w surowicy. Mechanizmami odpowiedzialnymi za utrzymanie tej równowagi są z jednej strony ilość przyjmowanych płynów, którą reguluje uczucie pragnienia, z drugiej strony wydalanie wody przez nerki, które reguluje m.in. przysadkowy hormon antydiuretyczny – wazopresyna. Zaburzenie tej równowagi, wynikające z nadmiernej podaży płynów czy też częściej upośledzenia nerkowego wydalania wody, może prowadzić do rozwoju hiponatremii. Inną przyczyną dyselektrolitemii może być także nadmierna utrata jonów sodowych drogą nerkową i pozanerkową (np. w przebiegu biegunek) [3,4].
Hiponatremia, w przeciwieństwie do hipernatremii zawsze związanej ze wzrostem osmolalności (tonii), może być związana zarówno z obniżoną (hiponatremia hipotoniczna), prawidłową (hiponatremia izotoniczna), jak i podwyższoną efektywną osmolalnością osocza (hiponatremia hipertoniczna).
Hiponatremia hipotoniczna, tzw. z rozcieńczenia, z którą najczęściej spotykamy się w praktyce klinicznej, wynika z nadmiernej retencji wody w ustroju. Jeśli podaż wody przewyższa możliwość jej usunięcia przez nerki, dochodzi do rozcieńczenia płynów ustrojowych, a zatem ich hipoosmolalności, zwanej też hipotonią. W rezultacie dochodzi do przesunięć płynów między przestrzenią zewnątrz- i wewnątrzkomórkową, prowadzących do obrzęku komórek. Szczególnie groźnym powikłaniem hiponatremii, będącym stanem zagrożenia życia, jest wynikający z niej obrzęk mózgu.
Rzadziej spotyka się hiponatremię hipertoniczną – dochodzi do niej, gdy w osoczu obecne są inne, czynne osmotycznie substancje nieprzechodzące przez błony komórkowe (np. glukoza w hiperglikemii czy mannitol podczas podawania dożylnego). Dochodzi wówczas do wzrostu efektywnej osmolalności osocza, przesunięcia płynów z przestrzeni wewnątrzkomórkowej do pozakomórkowej, co w efekcie prowadzi do odwodnienia komórek. Podaż parenteralna i utrzymywanie się w przestrzeni pozakomórkowej znacznych objętości płynów izotonicznych, niezawierających jonów sodowych (np. roztworów izotonicznych stosowanych podczas zabiegów przezcewkowej resekcji prostaty) prowadzi natomiast do hiponatremii izotonicznej, która nie wiąże się z przesunięciami płynów i zmianą uwodnienia komórek.
Ze względu na odmienny patomechanizm i postępowanie lecznicze, istotny jest inny podział hiponatremii zależny od objętości płynów w przestrzeni pozakomórkowej, ocenianej badaniem klinicznym chorego.
Z hiponatremią hipowolemiczną mamy do czynienia, gdy utrata wody i jonów sodu jest jedynie częściowo wyrównywana płynami bezelektrolitowymi. Najczęstszymi jej przyczynami są nadmierne pocenie, masywne biegunki lub wymioty, niedobór glikokortykosteroidów i mineralokortykosteroidów, diureza osmotyczna spowodowana mannitolem lub hiperglikemią, stosowanie diuretyków, ucieczka płynów do trzeciej przestrzeni (np. w przebiegu niedrożności jelit, zapalenia otrzewnej czy oparzeń).
Hiponatremia izowolemiczna (bez cech przewodnienia) spowodowana jest najczęściej zespołem nadmiernego wydzielania hormonu antydiuretycznego (syndrome of inappropriate antidiuretic hormone hypersecretion, SIADH) w przebiegu nowotworów (przede wszystkim płuc), chorób ośrodkowego układu nerwowego (udary mózgu, krwawienia, urazy), infekcji płucnych, ostrej niewydolności oddechowej lub okresu okołooperacyjnego. Rozwój SIADH może być także indukowany przez niektóre leki. W stanach tych wydzielanie wazopresyny nie jest hamowane mimo zmniejszenia się osmolalności osocza. Rzadszymi przyczynami hiponatremii izowolemicznej są: niedoczynność tarczycy, niedoczynność nadnerczy, stosowanie diuretyków tiazydowych i dieta ubogosolna.
Do hiponatremii hiperwolemicznej dochodzi w przebiegu niewydolności serca, marskości wątroby, zespołu nerczycowego, ostrej i przewlekłej niewydolności nerek. W stanach tych, mimo przewodnienia organizmu, obserwuje się zmniejszone wypełnienie łożyska tętniczego z następczą aktywacją układu współczulnego, układu renina-angiotensyna-aldosteron i wydzielaniem wazopresyny niezależnie od bodźców osmotycznych.
Rola wazopresyny w rozwoju hiponatremii w niewydolności serca
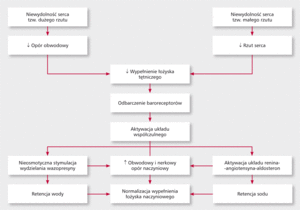
Uważa się, że utrzymanie wypełnienia łożyska tętniczego jest głównym wyznacznikiem nerkowego wydalania sodu i wody, zarówno w stanach fizjologicznych, jak i w patologii. Odbarczenie baroreceptorów tętniczych obecnych w lewej komorze, zatoce szyjnej i łuku aorty spowodowane zmniejszeniem rzutu serca, spadkiem oporu i ciśnienia tętniczego zmniejsza hamowanie (a więc aktywuje) ośrodka układu współczulnego znajdującego się w rdzeniu przedłużonym. Zwiększone napięcie układu współczulnego wydaje się mieć kluczową i pierwotną rolę w neurohormonalnej odpowiedzi na niedostateczne wypełnienie łożyska tętniczego. Dochodzi jednocześnie do aktywacji układu renina-angiotensyna-aldosteron (RAA) oraz wzmożonego wydzielania wazopresyny. Ta ostatnia pełni kluczową rolę w rozwoju hiponatremii (ryc. 1) [5].
Wazopresyna jest 9-aminokwasowym peptydem produkowanym przez podwzgórze, magazynowanym przez tylny płat przysadki i wydzielanym przez niego pod wpływem aktywacji współczulnej lub wzrostu osmolalności osocza krwi. Działanie antydiuretyczne wykazuje przez aktywację receptora V2, obecnego w cewkach zbiorczych nerek. Uruchomienie kaskady sygnałów wewnątrzkomórkowych prowadzi do zwiększonej syntezy akwaporyny-2 i ekspresji jej cząstek na błonie komórek wyściełających cewki zbiorcze. Białka te, pełniące rolę kanałów wodnych, zwiększają przepuszczalność cewek zbiorczych dla wody [6].
U pacjentów z niewydolnością serca wobec utrzymywania się błędnego koła neurohormonalnego na pierwszy plan wysuwa się tzw. nieosmotyczna regulacja wydzielania hormonu antydiuretycznego. W rezultacie obserwuje się stale podwyższone stężenie wazopresyny mimo prawidłowej lub nawet obniżonej osmolalności osocza.
Hiponatremia hipotoniczna a dalsze zaburzenia równowagi wodno-elektrolitowej ustroju
Hiponatremia hipotoniczna, niezależnie od przyczyny, prowadzi do dalszych zaburzeń równowagi wodno-elektrolitowej ustroju. Ich przebieg jest różny w zależności od czasu trwania hiponatremii. Jeżeli trwa ona krócej niż 48 godzin, mówimy o hiponatremii ostrej, jeżeli dłużej lub jej czas jest nieznany, rozpoznajemy hiponatremię przewlekłą. Hiponatremię przebiegającą bezobjawowo traktować należy również jako przewlekłą.
Ostra hiponatremia hipotoniczna prowadzi do gwałtownego przemieszczania się hipoosmolalnego płynu z przestrzeni zewnątrzkomórkowej do wnętrza komórek, co powoduje wzrost ich objętości. W przypadku komórek ośrodkowego układu nerwowego zajmujących przestrzeń ograniczoną pokrywą czaszki, przyrost objętości może prowadzić do obrzęku mózgu z objawami ciasnoty wewnątrzczaszkowej.
W hiponatremii hipotonicznej przewlekłej, zwłaszcza jeśli stężenie sodu spada powoli, ustrój uruchamia mechanizmy adaptacyjne. Adaptacja komórek do hipoosmolalnego środowiska zewnętrznego polega na aktywnym transporcie na zewnątrz różnych substancji osmotycznie czynnych, takich jak np. jony potasu, sodu, chlorku lub cząsteczki glutaminianu i asparaginianu. Zjawisko to prowadzi do zmniejszenia przezbłonowego gradientu osmotycznego, dzięki czemu komórki nie są tak bardzo narażone na obrzęk i uszkodzenie, stają się jednak bezbronne wobec nagłego wzrostu osmolalności płynu zewnątrzkomórkowego powodowanego np. przez szybki wlew dożylny dużych ilości roztworu NaCl. Ponieważ nie mają już rezerw cząstek czynnych osmotycznie, nie są w stanie zapobiec ucieczce wody ze swojego wnętrza, co prowadzi do ich odwodnienia. W ośrodkowym układzie nerwowym gwałtowne odwodnienie komórek prowadzi do demielinizacji struktur mózgowia.