Przedwczesne dodatkowe pobudzenia komorowe, które obserwowano u chorych z obniżoną LVEF w następstwie stosowania trastuzumabu, ustępowały po poprawie funkcji skurczowej lewej komory (wzroście LVEF do zakresu prawidłowych wartości).[17] Obserwowano rzadkie przypadki napadowego AF po zastosowaniu sunitynibu, cetuksymabu, alemtuzumabu. Podczas wlewu z rytuksymabu występowały zaburzenia rytmu, takie jak: napadowe AF, przedwczesne pobudzenia nadkomorowe i częstoskurcz komorowy, które ustępowały po zatrzymaniu stosowania leku.[18] Z kolei dazatynib, nilotynib i lapatynib mogą powodować wydłużenie odstępu QT, ale rzadko jest ono istotne i przekracza 500 ms.[5]
Wydłużonego odstępu QT, który wskazuje na zwiększone ryzyko nagłego zgonu arytmicznego, należy także spodziewać się podczas stosowania worynostatu. Po tym leku opisywano także epizody migotania przedsionków.
Interleukina-2 z kolei może powodować napady migotania przedsionków, częstoskurcz nadkomorowy, przedwczesne dodatkowe pobudzenia komorowe, nieutrwalony i utrwalony częstoskurcz komorowy.[5]
Wydłużenie odstępu QT jako marker ryzyka nagłego zgonu arytmogennego
1. Odstęp QT to czas pomiędzy początkiem załamka Q a końcem załamka T w standardowym zapisie elektrokardiograficznym (EKG).
2. Czas ten odzwierciedla elektryczną depolaryzację i repolaryzację komór.
3. Za przebieg depolaryzacji i repolaryzacji odpowiadają kanały błonowe kardiomiocytów, które regulują napływ i wypływ jonów do i z komórek sercowych.
4. Prawidłowa depolaryzacja zależy od wzajemnego stosunku nagłego napływu do komórek jonów dodatnich (Na+ i Ca++) oraz wypływu jonów K+ z komórek. Kiedy odkomórkowy prąd jonów K+ zaczyna przeważać nad prądem dokomórkowym, zaczyna się faza repolaryzacji.
5. Nieprawidłowa czynność błonowych kanałów jonowych doprowadza do zaburzeń w prądach, nieprawidłowości potencjału kardiomiocytów, wydłużenia fazy depolaryzacji lub repolaryzacji oraz do wydłużenia odstępu QT.
Odstęp QT koryguje się w zależności od częstości pracy serca za pomocą metod matematycznych, których jest kilka, jednak nie wykazano wyższości żadnej z nich.
Najczęściej używa się wzoru Bazetta. Wydłużony odstęp QT jest uważany za marker zwiększonego ryzyka wystąpienia arytmii komorowych, w tym polimorficznego częstoskurczu komorowego – TdP, i zagrożenia nagłym zgonem. Wydłużenie odstępu QT nie oznacza, że u każdego chorego na pewno wystąpi arytmia prowadząca do zgonu. Coraz częściej poddaje się krytyce znaczenie tego parametru w ocenie bezpieczeństwa terapii. Duża cześć chorych leczonych z powodu nowotworów ma wydłużony odstęp QTc i nie występują u nich złośliwe arytmie oraz nagłe arytmiczne zgony sercowe. Jednak uznaje się, że każde wydłużenie odstępu QT następujące podczas terapii powinno zwiększyć ostrożność przy stosowaniu leków przeciwnowotworowych.
Za prawidłowy odstęp QTc przyjmuje się < 450 ms u mężczyzn i < 460 ms u kobiet. Za klinicznie istotne wydłużenie QT przyjmuje się QTc > 500 ms lub wydłużenie po zastosowaniu leczenia QTc o > 60 ms.[19]Te wartości wskazują na duże zagrożenie TdP i nagłym zgonem i dlatego po ich przekroczeniu stosowanie leku powinno zostać przerwane. Ostateczna decyzja oczywiście uzależniona jest od dokładnej oceny stosunku ryzyka (TdP/nagłego zgonu) do korzyści uzyskanych dzięki leczeniu.
Mniej wiadomo o zagrożeniu TdP przy wydłużeniu odstępu QTc do wartości w przedziale 450 (460)-500 ms. Dla QTc z tego przedziału zaleca się szczególną ostrożność, wyrównanie innych czynników predysponujących do zaburzeń rytmu i ścisły monitoring pacjenta podczas stosowania leku.
Prawie wszystkie leki powodujące wydłużenie odstępu QT hamują szybką komponentę opóźnionego prostowniczego prądu jonów potasu (IKr), które wypływają z komórki za pośrednictwem białek kanałowych kodowanych przez gen (HERG, KCNH2 – ether-a-go-go-related gene). Budowa kanałów prądu IKr sprzyja powinowactwu do cząsteczek niektórych leków. Zidentyfikowano polimorfizmy genu KCNH2, które kodują białka kanałów prądu IKr charakteryzujące się zwiększonym powinowactwem do cząsteczek niektórych leków. To zjawisko tłumaczy, dlaczego tylko u niektórych osób dochodzi do wydłużenia odstępu QT podczas stosowania danej terapii. Połączenie się cząsteczki leku z białkiem kanału prądu IKr powoduje jego zablokowanie, hamuje przepływ jonów K oraz doprowadza do wydłużenia czasu potencjału czynnościowego i do wydłużenia odstępu QT. Mutacje odpowiedzialne za zjawisko wydłużenia odstępu QT ujawniające się pod wpływem leków nazywa się ukrytymi/cichymi mutacjami (silent mutations).
Wydłużenie odstępu QT jest najbardziej charakterystycznym zjawiskiem dla trójtlenku arsenu, stosowanego jako lek kolejnej linii w ostrej białaczce promielocytowej. Istotne wydłużenie odstępu QTc występuje u 37-68 proc. osób leczonych.
W jednym badaniu u 26,5 proc. pacjentów QTc przekraczało 500 ms i u 35,4 proc. wydłużyło się o ≥ 60 ms po rozpoczęciu leczenia.[20]
Wydłużony odstęp QT utrzymuje się zwykle od jednego do pięciu tygodni po zakończeniu stosowania trójtlenku arsenu, zaś po ośmiu tygodniach powraca do wartości wyjściowych u wszystkich chorych.[21]
Cząsteczka trójtlenku arsenu hamuje szybką składową opóźnionego, prostującego prądu jonów potasu (IKr), wolną składową prądu jonów potasu (IKs) i prąd jonów potasu zależny od ATP (IATP), modulując potencjał kardiomiocytów. W EKG obserwuje się, oprócz wydłużenia odstępu QT, obniżenie odcinka ST i spłaszczenie załamka T.
Podczas leczenia trójtlenkiem arsenu mogą wystąpić:
- przedwczesne dodatkowe pobudzenia nadkomorowe,
- przedwczesne dodatkowe pobudzenia komorowe,
- przyspieszony rytm komorowy,
- nieutrwalony VT,
- utrwalony VT,
- TdP.
Podczas stosowania tego leku opisywano stosunkowo często przypadki nagłych zgonów sercowych, które przyczynowo łączono z mechanizmem arytmicznym.[22] Opisywano także incydentalne epizody zaburzeń przewodnictwa przedsionkowo-komorowego: blok przedsionkowo-komorowy Wenckebacha, Mobitza, blok przedsionkowo-komorowy III stopnia.
Podczas stosowania trójtlenku arsenu zaleca się częste wykonywanie EKG w celu wczesnej identyfikacji chorych z istotnie wydłużonym QT. Zaleca się także bezwzględnie wyrównanie innych potencjalnych, modyfikowalnych przyczyn arytmii (zwłaszcza dyselektrolitemii, niedokrwistości, zaburzeń kwasowo-zasadowych itp.). W przypadku wydłużenia odstępu QTC > 500 ms i bezwzględnej konieczności kontynuacji leczenia, lek należy podawać w warunkach szpitalnych, monitorując stale EKG.[20]
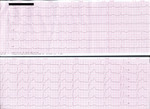
Ryc. 3. Napadowe migotanie przedsionków zarejestrowane u pacjentki z rakiem piersi w trakcie chemioterapii zawierającej antracykliny.