Inne artykuŁy
Prewencja malarii u osób planujących krótkie podróże
David O. Freedman, MD
Artykuł rozpoczyna się od zwięzłej prezentacji problemu klinicznego, następnie autor przedstawia różne schematy postępowania i wytyczne zapobiegania malarii. Na końcu artykułu zamieszczono zalecenia kliniczne dotyczące omawianego problemu.
Trzyosobowa rodzina wybiera się na safari do Afryki Południowej. W planie podróży są 3 dni w Kapsztadzie w RPA, 3 dni w Parku Narodowym Krugera (również w RPA) oraz 3 dni nad Wodospadami Wiktorii na granicy Zambii i Zimbabwe. Trzydziestojednoletni mężczyzna nie przyjmuje żadnych leków, ale niedawno zakończył leczenie fluoksetyną z powodu depresji. Jego 29-letnia żona, która wygrała podróż w konkursie na najlepszego sprzedawcę w swojej firmie, jest zdrowa i aktualnie jest w 15. tygodniu ciąży. Ich 7-letnie dziecko również nie ma kłopotów zdrowotnych. W jaki sposób można zmniejszyć ryzyko zachorowania na malarię tej rodziny i jakie środki ochronne zastosować?
Problem kliniczny
Malaria jest chorobą wywoływaną przez pasożyta – pierwotniaka atakującego erytrocyty. Do przeniesienia zarodźca malarii z jednego człowieka na drugiego dochodzi w wyniku ukąszenia przez komara widliszka, który jest aktywny jedynie od zmierzchu do świtu. Malarię u ludzi wywołują 4 gatunki: zarodziec sierpowy (Plasmodium falciparum; u nieuodpornionych turystów choroba może mieć przebieg śmiertelny), zarodziec ruchliwy (P. vivax), zarodziec owalny (P. ovale) i zarodziec malaryczny (P. malariae). Ocenia się, że z ok. 1500 przypadków malarii obserwowanych każdego roku w USA prawie dwie trzecie wywołuje P. falciparum, ok. jednej trzeciej P. vivax; rzadko natomiast obserwuje się zakażenia P. ovale lub P. malariae.1 W 2006 r. w USA zanotowano 6 zgonów z powodu malarii. Przypadki tej choroby wywołanej przez P. falciparum zdarzają się głównie wśród osób niestosujących żadnej profilaktyki farmakologicznej lub stosujących niewłaściwą profilaktykę. Większość zachorowań dotyczy nie turystów, ale imigrantów oraz ich dzieci udających się w odwiedziny do przyjaciół i rodziny w ojczystym kraju. Osoby te często nie przyjmują zapobiegawczo leków, czego przyczyną mogą być względy finansowe lub przeświadczenie, że odporność na malarię utrzymuje się przez całe życie, również na emigracji.1-4
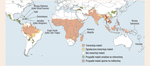
Do zarażeń malarią dochodzi w ponad 100 krajach świata (ryc. 1),5 położonych zarówno w rejonach tropikalnych, gdzie nowe przypadki pojawiają się przez cały rok, jak i w strefie klimatu umiarkowanego, gdzie niebezpieczeństwo grozi tylko w cieplejszych miesiącach. Obszar, na którym pojawiają się zarażenia, jest zmienny i może być bardzo ograniczony (nawet na obszarach przedstawionych na ryc. 1 jako zagrożone malarią). Bardzo dokładne mapy często pokazują obszary zagrożenia, które pod względem epidemiologicznym mogą nie mieć istotnego znaczenia dla turystów. Stanowią one tylko wskazówkę, że zawsze należy zachować dużą ostrożność, szczególnie jeżeli nie dysponuje się dokładnymi i aktualnymi danymi na temat sytuacji epidemiologicznej w danym kraju.
Do najistotniejszych objawów malarii u turystów należą podwyższenie ciepłoty ciała oraz pojawianie się objawów grypopodobnych, m.in. bólów głowy i pleców.7 Mogą wystąpić wymioty, biegunka, kurcze w jamie brzusznej oraz kaszel, ale są to objawy często pojawiające się również w przebiegu innych chorób. W podręcznikach można znaleźć informacje, że dla malarii charakterystyczne są kilkugodzinne epizody gorączkowe pojawiające się w 2-3-dniowych odstępach. Warto jednak pamiętać, że tor gorączkowy u turystów ma zazwyczaj charakter nieregularny. Objawy choroby wywołanej przez P. falciparum najczęściej pojawiają się po 9-14 dniach od ukłucia przez komara, ale u o osób stosujących suboptymalną profilaktykę mogą wystąpić nawet z kilkumiesięcznym opóźnieniem. W ok. 95% przypadków objawy malarii pojawiają się do 30 dni od zakończenia podróży. Jeżeli we wcześniejszym okresie nie przeprowadzi się odpowiednich badań i nie zastosuje leczenia, w naczyniach włosowatych może dojść do sekwestracji erytrocytów zarażonych pasożytem, co z kolei może być przyczyną ciężkiej choroby, łącznie z postacią mózgową, i zgonu. Objawy zarażenia innymi gatunkami zarodźca malarii mogą pojawić się od 12 dni do wielu miesięcy po ekspozycji na patogen, ale rzadko mają przebieg śmiertelny.
Celem artykułu jest przedstawienie sposobów postępowania w przypadku zagrożenia malarią u osób wybierających się w krótką podróż. „Krótka podróż” definiowana jest różnie, ale często przyjmuje się kryterium czasowe 3 tygodni lub mniej. Dłuższe podróże to zupełnie inne zagadnienie, omówione w osobnym opracowaniu.8
Strategie postępowania i dowody naukowe
Ocena ryzyka zachorowania powinna opierać się na dokładnej analizie planu podróży podczas konsultacji lekarskiej. Najlepiej, aby taka wizyta odbyła się mniej więcej miesiąc przed podróżą. Na stronach Centers for Disease Control and Prevention (CDC) (http://www.cdc.gov/malaria/travel/index.htm) oraz World Health Organization (WHO) (http://www.who.int/ith/countries/en/index.html) znajdują się najistotniejsze informacje o transmisji malarii oraz inne regularnie uaktualniane materiały, które można wykorzystać do oceny ryzyka.5,6,9 Lekarze, którzy nie są dobrze zaznajomieni ze specyfiką konkretnych obszarów występowania choroby, mogą posłużyć się dokładniejszymi mapami, dostępnymi w kilku publikacjach.9-11 Należy jednak zaznaczyć, że pomimo wykorzystania informacji z tak wielu źródeł opracowanie w pełni wiarygodnych danych o ryzyku zarażenia w wybranym regionie może być trudne.
Choć rozważania o częstości zarażeń malarią w lokalnej społeczności stanowią nieodzowny element oceny ryzyka, warto pamiętać, że ze względu na odmienny styl życia ryzyko zarażenia będzie istotnie mniejsze w przypadku turystów odwiedzających dany region niż w przypadku autochtonów. Wyjątkiem może być Afryka Subsaharyjska, gdzie odnotowuje się większość przypadków malarii; ryzyko zarażenia na tym obszarze jest bardzo wysokie, niezależnie od zachowań turysty. Natomiast na innych obszarach transmisja, szczególnie o znacznym nasileniu, może mieć ograniczony charakter (nawet na obszarach zacieniowanych na ryc. 1). Przyjmuje się, że porównanie częstości zarażeń wśród miejscowej ludności z częstością zarażeń turystów odzwierciedla ruch turystyczny na danym obszarze. Przykładem mogą być badania turystów przeprowadzone przez GeoSentinel w 32 regionach świata. Wykazano w nich, że w stosunkowo niewielkim stopniu narażeni są turyści podróżujący po Ameryce Południowej (tab. 1).12
Można to wytłumaczyć dużą dysproporcją między liczbą turystów odwiedzających obszary przybrzeżne i aglomeracje miejskie, gdzie malaria nie ma charakteru endemicznego, a liczbą turystów udających się na tereny wiejskie w głębi kontynentu, gdzie malaria jest chorobą endemiczną (ryc. 1). Z badań prowadzonych wśród europejskich turystów odwiedzających Indie wynika, że ogólna częstość zachorowań jest niewielka, prawdopodobnie dlatego że celem dużej części podróży służbowych i turystycznych są obszary miejskie, na których ryzyko zarażenia jest niewielkie.13,14 W niektórych rejonach miejskich i w przypadku turystów, którzy przyjechali w odwiedziny do znajomych oraz rodzin w kraju swoich przodków, ryzyko zarażenia jest istotnie wyższe niż wśród innych grup turystów podróżujących po Indiach. W 2006 r. kraj ten znalazł się na drugim miejscu pod względem liczby przywleczonych do USA przypadków malarii (łącznie 121 przypadków) na liście sporządzonej przez CDC.1
Oprócz trasy do czynników wpływających na ryzyko zarażenia malarią należą czas trwania podróży, pora roku, stosowanie lub niestosowanie przez turystę ochrony przed komarami i czas przebywania w miejscach, gdzie może być narażony na ukąszenia. Zagrożenie można istotnie zmniejszyć, przebywając w godzinach wieczornych i nocnych wyłącznie w pomieszczeniach klimatyzowanych lub w miejscach, gdzie liczba komarów jest niewielka.
Uważa się, że za wyjątkiem Afryki Subsaharyjskiej oraz niektórych miast w Indiach wyjazdy do miast stołecznych oraz na inne obszary wielkomiejskie (a taki jest zazwyczaj cel większości podróży służbowych) nie są w istotnym stopniu związane z ryzykiem zachorowania na malarię. Ryzyko to zwiększa się, jeśli turysta przebywa na terenach w najbliższym sąsiedztwie tych miast. Komar widliszek roznoszący zarodźca malarii w ciągu życia pokonuje dystans około 1 km. Ocenia się, że dzienne wycieczki na obszary, gdzie malaria występuje endemicznie, nie zwiększają istotnie ryzyka. I odwrotnie, nawet kilkugodzinna ekspozycja na ukłucia komarów na obszarze o dużym ryzyku transmisji może zakończyć się zarażeniem. Rozważając decyzję o zastosowaniu profilaktyki farmakologicznej, należy uwzględnić fakt, że turysta może zmienić trasę podróży oraz źle rozumieć, na czym polega mało istotne zagrożenie epidemiologiczne związane z wycieczką.
Sposób postępowania
Profilaktyka niefarmakologiczna

Tabela 2. Instrukcje dla turystów przed wyjazdem na tereny endemicznego występowania zarodźców malarii
Wszyscy turyści planujący wycieczkę na tereny, gdzie malaria ma charakter endemiczny, powinni bardzo dokładnie zaznajomić się z niefarmakologicznymi sposobami ochrony przed ukłuciami komarów. Należy do nich stosowanie środków odstraszających zawierających N,N-dietylo-m-toluamid (DEET), zakładanie koszul z długimi rękawami, długich spodni, obuwia chroniącego całe stopy oraz dokładne sprawdzanie pomieszczeń sypialnych (tab. 2). Choć tylko w jednym badaniu wykazano, że stosując te metody, można ograniczyć częstość zachorowań na malarię wśród turystów,16 ich skuteczność w zmniejszeniu liczby ukąszeń nie budzi wątpliwości.16-18
Profilaktyka farmakologiczna
Stosowane obecnie schematy profilaktyki farmakologicznej opracowano przede wszystkim z myślą o zapobieganiu zgonom z powodu ciężkiej malarii wywołanej zarażeniem P. falciparum. Leki te znajdują również zastosowanie w prewencji zarażeń wywołanych przez inne gatunki Plasmodium, ale w przypadku zarażeń wywołanych przez P. vivax i P. ovale notowano nawroty choroby.
Oporność P. falciparum na chlorochinę jest zjawiskiem niemalże powszechnym. Chlorochina jest skuteczna tylko w Meksyku, na obszarach Ameryki Środkowej położonych na wschód od Kanału Panamskiego, Karaibach, w Azji Wschodniej oraz kilku krajach Bliskiego Wschodu. Na pozostałych obszarach endemicznego występowania malarii zarówno CDC, jak i WHO zalecają stosowanie atowakwonu z proguanilem,19-22 meflochiny23-24 lub doksycykliny.25 Wykazano, że każda z tych metod charakteryzuje się ponad 95% skutecznością w prewencji malarii wywołanej przez P. falciparum. W badaniach z randomizacją prowadzonych wśród turystów oraz innych osób nieuodpornionych z terenów endemicznego występowania malarii porównywano skuteczność atowakwonu z proguanilem oraz doksycykliny z innymi lekami; w randomizowanych badaniach kontrolowanych placebo oceniano skuteczność meflochiny w grupie miejscowej ludności częściowo uodpornionej przeciwko malarii, a w retrospektywnych badaniach porównywano skuteczność meflochiny oraz innych preparatów stosowanych przez turystów.
Oporność na meflochinę obserwowano w niewielu wiejskich regionach Azji Południowo-Wschodniej (ryc. 1). Warto jednak zaznaczyć, że turyści rzadko odwiedzają tamte tereny. Wybierając lek dla osoby podróżującej na obszar występowania malarii opornej na chlorochinę, powinno się uwzględnić takie czynniki, jak: czas trwania podróży, wiek podróżnych, ich dotychczasowe choroby, występujące wcześniej objawy nietolerancji leków, możliwości finansowe, a u kobiet – możliwość ciąży.26 W tabeli 3 zebrano najistotniejsze informacje na temat leków stosowanych w profilaktyce, łącznie z przeciwwskazaniami oraz działaniami niepożądanymi. Atowakwon z proguanilem to najlepiej tolerowane połączenie, ale przy dłuższych podróżach trzeba wziąć pod uwagę czynnik ekonomiczny. Każdy chory powinien uzyskać bardzo dokładne informacje na temat sposobu przyjmowania zalecanych leków (tab. 2).
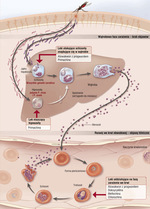
Leki przeciwmalaryczne, takie jak chlorochina, meflochina i doksycyklina, w odróżnieniu od wielu innych leków nie zabezpieczają turystów przed pierwotnym zarażeniem zarodźcem malarii, mają raczej wpływ na późniejsze fazy rozwojowe pasożyta, kiedy po początkowym etapie dojrzewania w wątrobie zaczyna zarażać erytrocyty (ryc. 2). W związku z tym w celu eradykacji zarodźców, które mogą być jeszcze uwalniane do krwiobiegu z wątroby, leki tego typu powinny być przyjmowane przez co najmniej 4 tygodnie po ostatniej ekspozycji na ukąszenie przez komara. Warto jednak pamiętać, że atowakwon z proguanilem wpływa nie tylko na patogeny znajdujące się w krwiobiegu, ale może także oddziaływać na aktywną replikację pasożyta w wątrobie (ryc. 2). Stosowanie tego leku można zakończyć po tygodniu od ustania ekspozycji na komary.
Farmakologiczną profilaktykę przeciw malarii z zastosowaniem atowakwonu z proguanilem należy rozpocząć 1-2 dni przed podróżą na tereny, gdzie malaria jest chorobą endemiczną, a w przypadku chlorochiny – tydzień przed planowanym wyjazdem. Leczenie meflochiną powinno zacząć się przynajmniej dwa, a najlepiej trzy tygodnie przed wycieczką. Ma to na celu przede wszystkim obserwację chorego pod względem występowania działań niepożądanych, które mogłyby być przyczyną odstawienia leku, i umożliwienie wprowadzenia alternatywnego schematu leczenia. Wskazaniem do zaprzestania podawania atowakwonu z proguanilem i zastosowania innego preparatu mogą być nagłe stany lękowe o niejasnej etiologii, depresja, pobudzenie i splątanie. Warto także mieć na uwadze, że pierwszy dzień spędzony na obszarze endemicznego występowania malarii nie musi odpowiadać pierwszemu dniowi pobytu w kraju o zwiększonym ryzyku zarażenia malarią.
Kobiety w ciąży
Przebieg malarii u kobiet w ciąży jest cięższy, zwiększa się również ryzyko niekorzystnych następstw choroby (zarówno dla matki, jak i płodu). Żaden z leków wykorzystywanych w profilaktyce farmakologicznej nie gwarantuje 100% skuteczności. Obydwie instytucje, WHO i CDC, zalecają, aby kobiety w ciąży nie podróżowały na tereny, na których malaria ma charakter endemiczny.5,6 Większość ciężarnych rezygnuje z takich wyjazdów, ale u kobiet, które mimo wszystko decydują się na wyprawę lub muszą w niej uczestniczyć, lekiem z wyboru w przypadku malarii opornej na chlorochinę jest meflochina (tab. 3). Ze względu na niewielką liczbę danych dotyczących stosowania tego leku w pierwszym trymestrze ciąży zaleca się, aby – jeżeli to możliwe – odłożyć podróż do późniejszego okresu ciąży.27,28 Wykazano, że w ciąży bezpiecznie można stosować preparaty zawierające 20% DEET.29 Należy jednak pamiętać, że powinny one być stosowane częściej, ponieważ czas ich działania jest krótszy niż preparatów o stężeniu co najmniej 30%.
Dzieci
Dzieciom podaje się zasadniczo te same leki z jednym wyjątkiem – nie powinno się stosować doksycykliny u dzieci poniżej 8 r.ż. Opublikowano również zalecenia dotyczące dawkowania leków przeciwmalarycznych u dzieci z uwzględnieniem masy ciała. W przypadku atowakwonu z proguanilem dostępne są mniejsze dawki leku (tabletki zawierają jedną czwartą dawki dla dorosłych). Niestety, meflochina nie jest dostępna w mniejszej dawce, tak więc każdą tabletkę trzeba dzielić na czworo. Dla dzieci o najmniejszej masie ciała tabletki, które mają gorzki smak, najpierw muszą zostać przez farmaceutę rozkruszone, a następnie zważone i zmieszane z syropem zawierającym cukier lub czekoladę. Dawkowanie raz w tygodniu znacznie ułatwia stosowanie leku u małych dzieci. Uważa się, że u dzieci można stosować preparaty zawierające DEET w stężeniu do 30%,30 ale nie prowadzono badań nad preparatami o większym stężeniu.
Późne nawroty
Jeżeli chlorochina, meflochina, doksycyklina i atowakwon z proguanilem są stosowane zgodnie ze wskazaniami, odpowiednio długo i osiągają odpowiednie stężenia w surowicy, to chronią przed rozwojem choroby wywołanej przez każdy z czterech gatunków zarodźca malarii.31 Przykładowo, skuteczność atowakwonu z proguanilem w prewencji malarii wywołanej przez P. vivax ocenia się na 84-100%.21,32 Warto pamiętać, że leki te nie działają w obrębie wątroby i nie mają wpływu na swoiste uśpione formy pasożyta (hipnozoity) – typowe dla P. vivax i P. ovale (ryc. 2).33,34 Hipnozoity mogą podlegać samoistnej reaktywacji po tygodniach lub nawet miesiącach od pierwotnego zarażenia. Uwolnienie tych form do krwiobiegu powoduje chorobę o późnym początku lub jej nawrót. (Za rozwój objawów klinicznych malarii oraz stany gorączkowe odpowiedzialne są formy pasożyta znajdujące się w erytrocytach, a nie w wątrobie). Każdego roku notuje się kilkaset przypadków późnych nawrotów malarii u chorych zarażonych P. vivax lub P. ovale. Dotyczy to również turystów powracających z wypraw, podczas których ściśle stosowali się do zaleceń przyjmowania chlorochiny, meflochiny, doksycykliny lub atowakwonu z proguanilem.1,35,36 Takich późnych nawrotów nie obserwuje się u zarażonych P. falciparum i P. malariae, są to bowiem gatunki nietworzące hipnozoitów.
Jedynym lekiem działającym na hipnozoity P. vivax i P. ovale w wątrobie jest primachina.37 Najczęściej stosuje się ją u osób, które były narażone na dłuższy lub krótki, ale intensywny kontakt z komarami na obszarze o zwiększonym ryzyku zarażenia P. vivax lub P. ovale, nawet gdy P. falciparum jest zasadniczym dominującym patogenem. Ocenia się, że stosowanie primachiny raz dziennie przez 14 kolejnych dni po zakończeniu podróży może zmniejszyć ryzyko nawrotu.38 Bardzo trudno dokładnie ocenić ryzyko nawrotu choroby dla osób przebywających na konkretnym obszarze. Istotnym problemem może być również konieczność zastosowania drugiego leku profilaktycznego. Z tych właśnie powodów nie stosuje się zbyt często farmakologicznej profilaktyki przeciwnawrotowej, jest ona zarezerwowana najczęściej dla chorych o udokumentowanej i wydłużonej ekspozycji na zakażenie.
Primachina w profilaktyce pierwotnej
Primachina charakteryzuje się wyjątkowym mechanizmem podwójnego działania w wątrobie (ryc. 2), dlatego niektórzy specjaliści zalecają ją jako lek drugiego rzutu w prewencji pierwotnego zarażenia wszystkimi czterema gatunkami zarodźca malarii.36,38,39 Zaletą primachiny jest możliwość wykorzystania jej również w profilaktyce przeciwnawrotowej. Powszechne wykorzystanie primachiny w farmakologicznej profilaktyce pierwotnej jest jednak ograniczone przez ryzyko hemolizy u osób z niedoborem dehydrogenazy glukozo-6-fosforanowej (G6PD). Jest to choroba występująca stosunkowo często u przedstawicieli rasy czarnej pochodzących z krajów śródziemnomorskich oraz u Azjatów.40 Przed zastosowaniem primachiny w profilaktyce pierwotnej lub w prewencji późnego nawrotu konieczne jest wcześniejsze wykonanie badań w kierunku G6PD.
Wątpliwości
Bezpieczeństwo meflochiny
W ostatnim czasie zwrócono uwagę na zaburzenia neuropsychiczne oraz inne działania niepożądane mogące mieć związek z meflochiną (tab. 3). Ocenia się, że od 1989 r. meflochinę przyjmowało ok. 30 mln osób, istnieje też sporo opracowań poświęconych temu lekowi.24,41-45 Po zastosowaniu go w farmakologicznej profilaktyce malarii w zalecanych dawkach poważne działania niepożądane, takie jak drgawki czy psychozy, pojawiają się rzadko, u 1/6500-1/10 600 pacjentów.46,47 Mniej groźne, ale uciążliwe objawy neuropsychologiczne, takie jak bezsenność, koszmary senne, nadmierna drażliwość czy depresja, występują u 1/200-1/500 leczonych.26,45 Warto jednak zauważyć, że nie ma pełnych danych na temat tych objawów u turystów nieprzyjmujących meflochiny.45 Bardzo wyraziste sny zgłasza 15-25% osób przyjmujących ten lek, są one jednak dość dobrze tolerowane. Ogólnie ocenia się, że ok. 95% pacjentów jest w stanie ukończyć zaplanowane leczenie.
Schemat terapii wyczekującej
W niektórych krajach, szczególnie europejskich,48 pracownicy opieki zdrowotnej zazwyczaj nie zalecają stosowania profilaktyki farmakologicznej osobom planującym krótkie wycieczki na tereny o niskim lub umiarkowanym ryzyku zarażenia malarią.13,14,48,49 Doradza się natomiast zabranie w podróż zestawu leków przeciwmalarycznych w celu samodzielnego rozpoczęcia leczenia w przypadku pojawienia się stanów gorączkowych, jeżeli w ciągu 24 h uzyskanie pomocy lekarskiej będzie niemożliwe. Taki sposób postępowania nie uzyskał jednak akceptacji większości pozostałych krajów, ponieważ zaobserwowano, że znaczna część turystów, mimo dostępu do pomocy medycznej, samodzielnie ordynuje sobie leki, często stosując je w nieodpowiednich dawkach, szczególnie gdy są poważnie chorzy.
Wytyczne opracowane przez towarzystwa naukowe
Infectious Diseases Society of America opracowało wytyczne profilaktyki malarii dla turystów.50 Zgodnie z nimi do podstawowych sposobów profilaktyki pierwotnej w zależności od obszaru należy stosowanie chlorochiny lub atowakwonu z proguanilem, meflochiny lub doksycykliny. Znalazły się wśród nich także zasady profilaktyki pierwotnej z wykorzystaniem primachiny jako leku alternatywnego, jednak bez dokładnych wskazań dotyczących jego zastosowania. Nie zajęto się także profilaktyką przeciwnawrotową.
Podsumowanie i zalecenia
Z danych dostępnych dla lekarzy niezajmujących się medycyną tropikalną wynika, że trzyosobowa rodzina, którą opisałem na początku artykułu, podczas części podróży do Parku Narodowego Krugera oraz nad Wodospady Wiktorii może być narażona na kontakt z malarią oporną na chlorochinę. Wydaje się, że w przypadku mężczyzny najbardziej odpowiednie będzie stosowanie codziennie atowakwonu z proguanilem. (Meflochina jest przeciwwskazana ze względu na depresję w wywiadzie. Istotną wadą doksycykliny, szczególnie w klimacie tropikalnym, mogą być działania niepożądane: nadwrażliwość na światło, a u kobiet zwiększone ryzyko grzybicy pochwy. Dla części turystów niski koszt leczenia kompensuje jednak ewentualne niedogodności.) Stosowanie atowakwonu z proguanilem należy rozpocząć drugiego dnia wycieczki – w Cape Town, dwa dni przed pierwszą możliwą ekspozycją na malarię. Lek powinien być przyjmowany przez 7 dni po opuszczeniu terenów, gdzie malaria ma charakter endemiczny. Atowakwon z proguanilem powinien być również zastosowany u 7-letniego dziecka. Lek trzeba podawać wg takiego samego schematu jak ojcu, ale w mniejszych dawkach. Matce należałoby odradzić podróż, gdyby jednak nalegała (a tak często się zdarza), należałoby zastosować meflochinę zgodnie z ogólnym schematem dawkowania. Oprócz profilaktyki farmakologicznej istotnym elementem postępowania powinno być też rygorystyczne stosowanie się do zaleceń ochrony przed komarami, korzystanie ze środków odstraszających zawierających 20% DEET, zakładanie ubrań chroniących przed ukąszeniami, spanie w pomieszczeniach klimatyzowanych lub dokładnie sprawdzonych. Biorąc jednak pod uwagę fakt, że żaden ze sposobów ochrony przed ukąszeniami komarów nie jest w 100% skuteczny, wszyscy powinni zostać dokładnie poinstruowani o sposobie postępowania na wypadek, gdyby u któregokolwiek z członków rodziny po powrocie do domu pojawiły się stany gorączkowe (tab. 2).




Komentarz
prof. dr hab. med. Piotr Zaborowski, Klinika Chorób Odzwierzęcych i Tropikalnych WUM, Warszawa
prof. dr hab. med. Piotr Zaborowski
Artykuł Davida O. Freedmana, bez wątpienia znawcy przedmiotu, dotyczy profilaktyki zachorowań na malarię w trakcie krótkich podróży. Czas ten został przez autora ograniczony do maksymalnie trzech tygodni. Biorąc pod uwagę okres utajenia zarażenia od ukłucia zarażonego komara do pojawienia się pierwszych objawów klinicznych, jest to czas zakreślony w pełni racjonalnie, bo oznacza, że przeważająca liczba zachorowań ujawni się po powrocie do miejsca zamieszkania. Chciałbym także zwrócić uwagę na znakomicie dobrany opis sytuacji klinicznej. Każdy element tego opisu znajduje wyjaśnienie w treści artykułu, a potem wyjaśnienie w jego podsumowaniu.
Malaria jest chorobą pasożytniczą, wywoływaną przez pierwotniaki z rodzaju Plasmodium. Obecnie największe znaczenie epidemiologiczne przypisuje się czterem gatunkom tych pierwotniaków (P. falciparum, P. vivax, P. ovale i P. malariae), chociaż w ostatnich latach nagromadzono sporo dowodów na patogenność jeszcze jednego gatunku – P. knowlesi.1,2 Ten ostatni bez wątpienia pochodzi od małp człekokształtnych i stanowi nowe wyzwanie epidemiologiczne w krajach Azji Południowo-Wschodniej, szczególnie w Malezji i Chinach. Co prawda, wektory przenoszące ten gatunek plazmodiów (Anopheles cracens, A. latens i A. donaldi)3,4 występują na dość ograniczonym obszarze geograficznym, ale sam fakt powtarzania się historycznie znanej drogi przeskoku na ludzi pierwotniaków patogennych dla gryzoni czy zwierząt naczelnych jest sygnałem, że nie wolno lekceważyć możliwości pojawienia się jeszcze innych rodzajów malarii. Wcale nie jest wykluczone, że w kolejce czekają już P. yoelii, P. berghei i P. brasilianum.1,5,6 Znaczenie ewentualnego pojawienia się nowych postaci malarii polega na tym, że kliniczny przebieg tych zarażeń prawdopodobnie będzie się różnił od dotychczasowych. Skoro znane dotychczas postaci względnie łagodnej, ale niekiedy trudno rozpoznawalnej z powodu wytwarzania hipnozoitów w wątrobie trzeciaczki (P. vivax i P. ovale), obarczonej powikłaniami nerkowymi czwartaczki (P. malariae) czy wysoce nieswoistej objawowo malarii złośliwej (P. falciparum) rozpoznawane są z reguły z opóźnieniem, to jak szybko będą rozpoznawane postaci nowe o nieznanym jeszcze obrazie klinicznym?
Z tych oto powodów w komentowanym artykule pojawia się kilka bardzo interesujących informacji, które znane są jedynie prowadzącym specjalistyczne doradztwo w zakresie medycyny podróży, a powinni je znać wszyscy praktykujący lekarze.
Nie wystarczy studiować mapy narażenia na malarię i oporności na leki przeciwmalaryczne stosowane w zapobieganiu tej chorobie. Ryzyko zachorowania zależy od wielu czynników. Jak wynika z badań międzynarodowej sieci klinik medycyny podróży GeoSentinel,7 zajmujących się m.in. obserwacją rozprzestrzenienia zachorowań na malarię, ryzyko jest dziesiątki razy mniejsze np. w Ameryce Południowej niż w subsaharyjskich regionach Afryki. Jest to spowodowane tym, że liczba turystów zapuszczających się głęboko w dżunglę jest zdecydowanie mniejsza niż zwiedzających obszary zurbanizowane. Podobne zjawisko dotyczy ryzyka dla bardzo krótkich, kilkudniowych, pobytów biznesowych w Indiach i obszarów o niskiej endemiczności. Warto zapamiętać dane dotyczące względnego ryzyka zachorowania na malarię w różnych częściach globu, zawarte w tabeli 1. Doskonale posłużą jako argumenty przemawiające za koniecznością stosowania profilaktyki przeciwmalarycznej. Ze wszech miar słuszna jest krytyka poglądu, że zamiast stosowania profilaktyki można pozwolić podróżującym na zażywanie leków przeciwmalarycznych w momencie pojawienia się gorączki i innych objawów chorobowych. Warto zauważyć, że grupa podróżujących, którym można byłoby zaproponować takie postępowanie, jest mocno ograniczona.
Ryzyko zachorowania na malarię zależy także od pory roku (wilgotność, temperatura), liczby komarów i ukłuć oraz czasu przebywania na otwartym terenie endemicznym w porach żerowania komarów, ale również – dyscypliny i wiedzy podróżujących (stosowanie odpowiedniego ubioru, repelentów i leczenia profilaktycznego).
W razie podejrzenia malarii nie wolno zwlekać. Trzeba szybko skierować chorego do wyspecjalizowanego ośrodka referencyjnego (w Polsce: Instytut Medycyny Morskiej i Tropikalnej Akademii Medycznej w Gdańsku, Klinika Chorób Tropikalnych i Pasożytniczych Uniwersytetu Medycznego w Poznaniu oraz Klinika Chorób Odzwierzęcych i Tropikalnych Warszawskiego Uniwersytetu Medycznego).
Opierając się na własnym doświadczeniu i praktyce, gorąco zalecam lekarzom zadawanie pytania o pobyt w regionach klimatu gorącego wszystkim chorym zgłaszającym się z okresową lub nieregularną gorączką trwającą ponad 10 dni. O malarii jako potencjalnej przyczynie takiej gorączki trzeba myśleć również wówczas, gdy pacjenci mają inne objawy osiowe, np. bóle głowy, biegunki czy kaszel.
Tak więc z pełnym przekonaniem polecam każdemu praktykującemu lekarzowi, aby dokładnie przeczytał ten artykuł oraz by ciągle miał pod ręką rycinę 1 oraz tabele 1, 2 i 3. W prostych przypadkach zawarta w nich wiedza powinna wystarczyć do udzielenia porady zdrowym osobom wyjeżdżającym w regiony zagrożenia malarią. Trzeba jednak pamiętać, że diabeł tkwi w szczegółach i że nie jest wstydem dla nikogo pytać o to, czego nie wie się na pewno.
Piśmiennictwo
1. Kocken CHM, Ozwara H, van der Wel A, Beetsma AL i wsp.: Plasmodium knowlesi provides a rapid in vitro transfection system that enables double-crossover gene knockout studies. Infection & Immunity 2002; 70(2): 655-660.
2. Cox-Singh J, Davis TME, Lee K-S i wsp.: Plasmodium knowlesi malaria in humans is wi dely distributed and potentially life-threatening. Clin.Infect.Dis. 2008; 46(2): 165-171.
3. Vythilingam I, NoorAzian YM, Huat TC i wsp.: Plasmodium knowlesi in humans, macaques and mosquitos in peninsular Malaysia. Parasites & Vectors 2008; I, 26 doi: 10.1186/I1756-3305-I-26.
4. Tan CH, Vythilingam I, Matusop A i wsp.: Bionomics of Anopheles latens w: Kapit, Sarawak, Malaysian Borneo in relation to the transmission of zoonotic simian malaria parasite Plasmodium knowlesi. Malaria Journal 2008; 7:52 doi: 10.1186/1475-2875-7-52.
5. Sinden RE, Dawes EJ, Alavi Y i wsp.: Progression of Plasmodium berghei through Anopheles stephensi is density dependent. PLoS Pathog. 2007 3(12): e195. doi: 10.1371/journal.ppat.0030195.
6. Roy S.W., Irimia M.: Origins of human malaria: rare genomic changes and full mitochondrial genomes confirm the relationship of Plasmodium falciparum to other mammalian parasites but complicate the origins of Plasmodium vivax. Mol.Biol.Evol. 2008; 25(6): 1192-1198.
7. Leder K, Black J, O’Brien D, Greenwood Z i wsp.: Malaria in travelers: a review of the GeoSentinel surveillance network. Clin.Infect Dis. 2004; 39(8): 1104-12.