Diagnostyka zagadki echo
Klinika Wad Wrodzonych Serca, Instytut Kardiologii, Warszawa
Echoporada
Mirosław Kowalski
Szanowni Państwo, drodzy Czytelnicy,
Doszedłem do wniosku, że zbyt mało miejsca poświęcam na łamach Zagadek echokardiografii interwencyjnej, a taka dziedzina rodzi się niemal na naszych oczach i intensywnie rozwija. Być może szczegółowe omawianie zabiegów i znaczenia echokardiografii w ich monitorowaniu wykracza poza ramy działu, ale warto kłaść nacisk na poprawność badania na etapie przygotowania i podejmowania decyzji. Od nas bowiem, echokardiografistów, zależy kwalifikacja, a co za tym idzie – skuteczność i bezpieczeństwo zabiegu.
W bieżącej Echoporadzie pragnę zwrócić Państwa uwagę na szczegóły badania u pacjenta z niedokrwienną niedomykalnością mitralną, które mogą mieć znaczenie w wyborze niechirurgicznej opcji leczenia. Wydaje się, że im szybciej będziemy oswajać się z nowymi projekcjami i parametrami, tym bardziej będziemy pomocni kolegom – kardiologom interwencyjnym. Echoszarada, czyli tradycyjna łamigłówka, odbiega od tej problematyki. Proszę wytężyć wzrok i postarać się wydobyć z prezentowanego materiału istotne, stanowiące o dalszych losach chorego nieprawidłowości. Życzę ciekawej lektury!
Mirosław Kowalski
Dane kliniczne:
Mężczyzna, lat 72, z cukrzycą i chorobą wieńcową został przyjęty po raz kolejny do kliniki z powodu duszności wysiłkowej. Chory przebył w 2007 r. zabieg przezskórnej rewaskularyzacji wieńcowej z implantacją stentu typu DES do gałęzi przedniej zstępującej lewej tętnicy wieńcowej, a w 2008 r. zabieg rewaskularyzacji gałęzi okalającej z implantacją dwóch stentów z powodu zawału serca ściany tylno-dolno-bocznej. Od zawału rejestrowano w badaniach echokardiograficznych cechy kardiomiopatii niedokrwiennej z frakcją wyrzutową lewej komory ok. 15% i dużą niedomykalnością mitralną. Wszczepiono choremu kardiowerter-defibrylator. W kolejnych latach był przyjmowany do kliniki z powodu tzw. burzy elektrycznej, pojedynczych wyładowań kardiowertera, a także częstoskurczu komorowego bez interwencji urządzenia. W 2009 roku wykonano u chorego ablację RF z wykorzystaniem systemu CARTO. Pacjent przewlekle leczony był amiodaronem. Ostatnio zgłaszał pogorszenie tolerancji wysiłku (klasa III wg NYHA), bez bólów w klatce piersiowej. Z powodu rozległej akinezy ściany tylno-dolno-bocznej nie kwalifikowano go do leczenia za pomocą układu resynchronizującego. W zdjęciu przeglądowym klatki piersiowej stwierdzono zastój w krążeniu płucnym, powiększoną sylwetkę serca, cechy nadciśnienia płucnego. Leczony był dużymi dawkami leków moczopędnych.
Pytanie:
Jak należy postąpić z chorym? Czy korekcja niedomykalności mitralnej byłaby rozwiązaniem? Na co należałoby zwrócić szczególną uwagę przy podejmowaniu decyzji?
Odpowiedź:
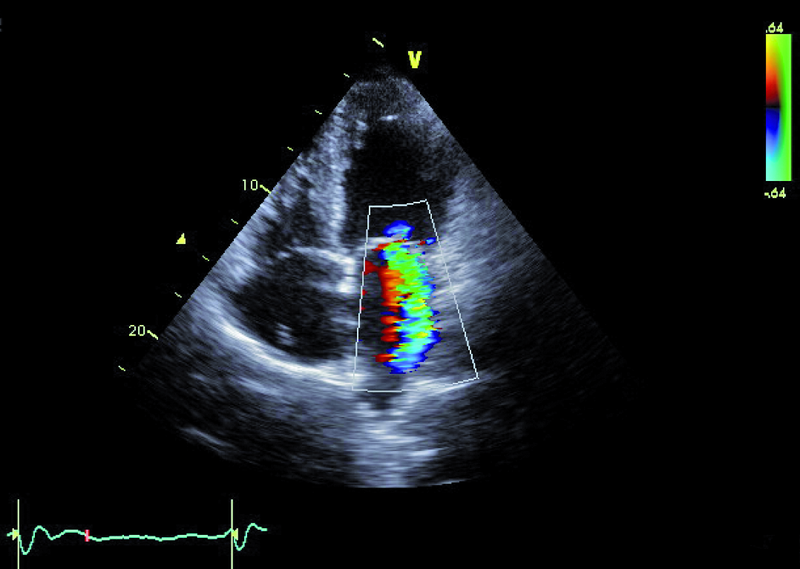
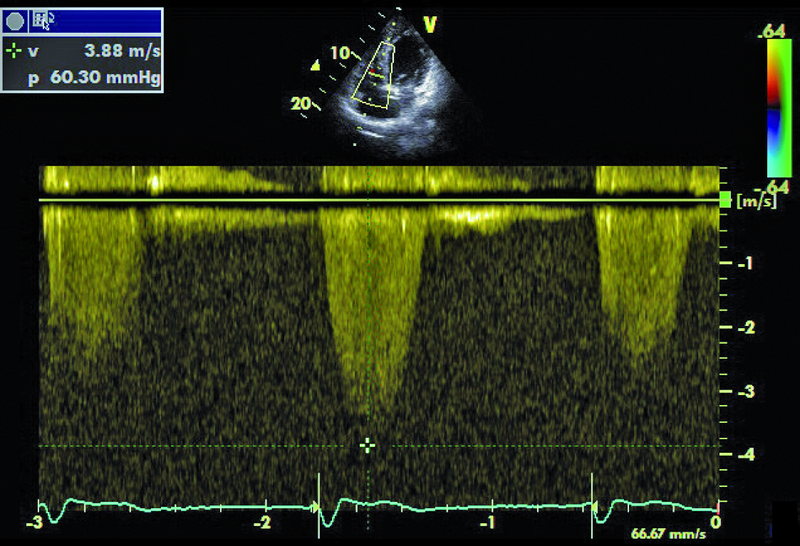
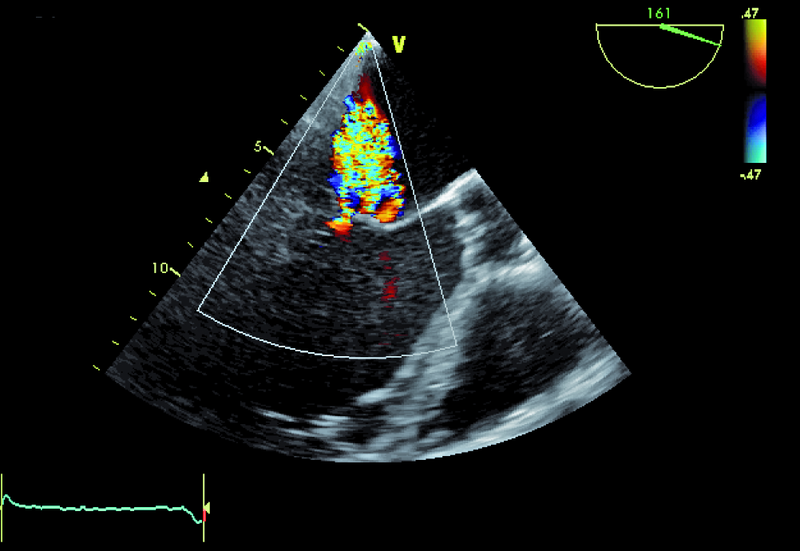
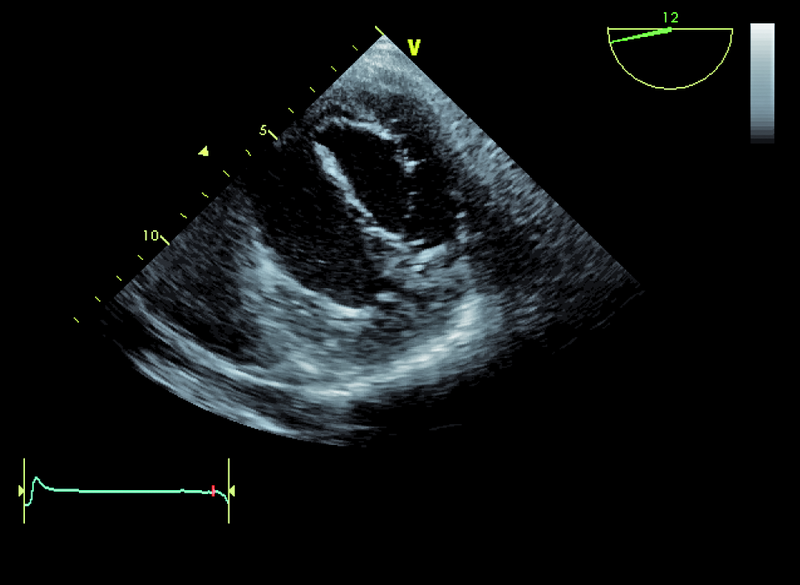
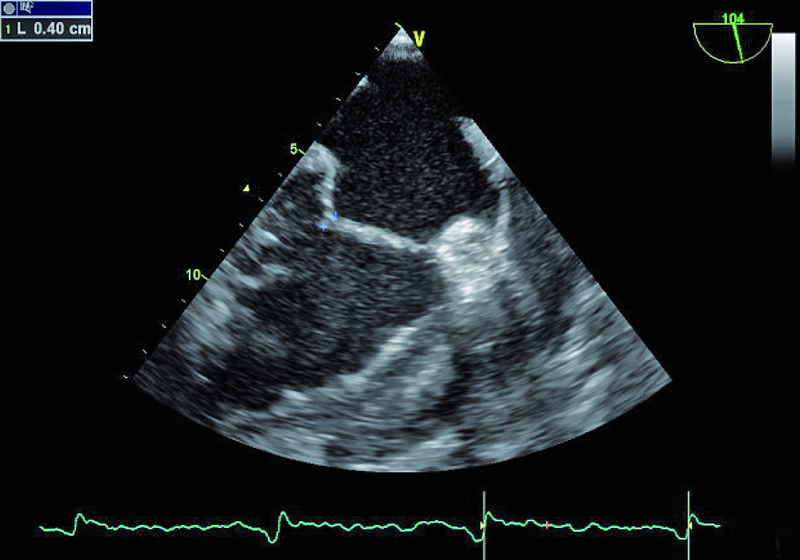
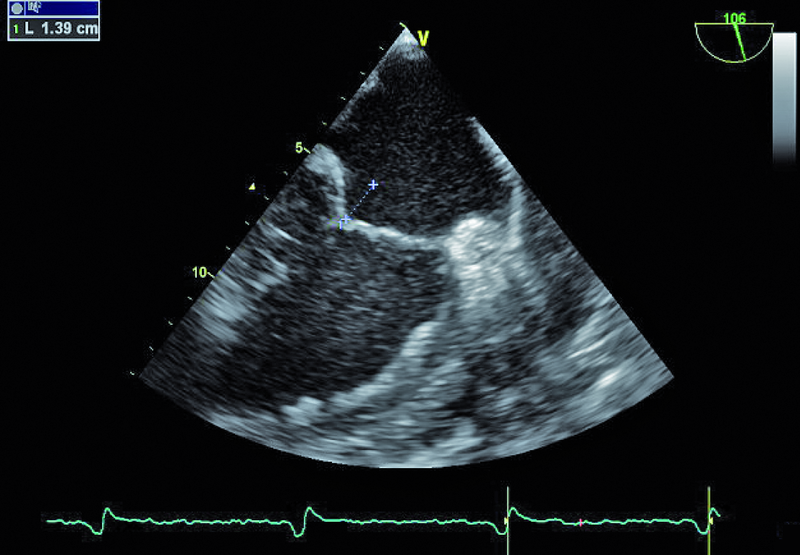
Niedomykalność zastawki mitralnej o etiologii niedokrwiennej pogarsza rokowanie u chorego z chorobą wieńcową i istotnie obniża komfort życia. Fala zwrotna w prezentowanym materiale sięga ujścia żył płucnych (ryc. 1), a ciśnienie w jamie prawej komory jest podwyższone (ryc. 2). U chorych, u których nie ma wskazań do rewaskularyzacji lub u chorych z chorobami współistniejącymi poszukuje się innych metod interwencji poza chirurgiczną naprawą. Punktem wyjścia dla rozważań o możliwości leczenia niechirurgicznego jest dokładna ocena anatomii zastawki. Wykorzystuje się dane zarówno z badania przezklatkowego, jak i przezprzełykowego, choć oczywiście optymalnym rozwiązaniem byłoby zastosowanie obrazowania trójwymiarowego. Sporo uwagi poświęca się ostatnio naprawie płatków zastawki za pomocą tzw. urządzenia mitraclip. Techniką tą można interesować się zwłaszcza w kontekście chorych bez istotnego poszerzenia pierścienia zastawki (w prezentowanym przypadku średnica pierścienia nie przekraczała 35 mm), a z dostatecznie dużą ilością tkanki tworzącej jej płatki. Założeniem techniki mitraclip, przypominającej zabieg chirurgiczny Alfieriego, jest połączenie segmentów środkowych płatka przedniego i tylnego. Skutecznie wykonany zabieg poprawia koaptację płatków i zapoczątkowuje odwrotny remodeling lewej komory, zmniejszający z kolei udział tzw. sił pociągających. Na co trzeba zwrócić uwagę, oceniając pacjenta z niedomykalnością mitralną, towarzyszącą chorobie niedokrwiennej? Niedomykalność (wg podziału Carpentiera typ 3b) powinna rzeczywiście powstawać między segmentami A2 a P2 (ryc. 3), ponieważ tylko w takim wypadku połączenie płatków i wytworzenie dwóch osobnych ujść może choremu przynieść korzyść. Ważnym elementem oceny jest uzyskanie projekcji przezżołądkowej poprzecznej. Ta projekcja bardzo dobrze ilustruje wielkość płatków i ich wzajemną relację (ryc. 4 – większy płatek tylny znajduje się bliżej głowicy). Przeciwwskazaniami do zabiegu implantacji mitraclip może być nadmierna grubość płatków, utrudniająca ich uchwycenie przez ramiona urządzenia, mniejsza niż 2 mm długość koaptacji oraz większa niż 11 mm głębokość koaptacji w stosunku do linii podstawnej pierścienia zastawki. Wymienionych cech nie potwierdzono w badaniu (ryc. 5, 6) i zakwalifikowano chorego do zabiegu w trybie planowym. Warto pamiętać, że echokardiografia służy nie tylko ocenie wskazań do zabiegu, ale stanowi także podstawę jego monitorowania.