Między teorią a praktyką
Rola limfadenektomii w ginekologii onkologicznej
Prof. dr hab. med. Andrzej Witek
Lek. Agnieszka Wróblewska Czech
Dr n. med. Wojciech Szanecki
W ginekologii onkologicznej nowotwór jest traktowany jako choroba wielonarządowa, której nieodłącznym elementem są przerzuty do węzłów chłonnych dwóch obszarów: miednicy mniejszej oraz okołoaortalnych. Ocena przestrzeni zaotrzewnowej stała się przez to integralną częścią diagnostyki przed- i śródoperacyjnej umożliwiającej określenie stopnia zaawansowania klinicznego nowotworu oraz określającej dalszy proces leczenia skojarzonego.[1] Zakres zabiegu operacyjnego jest uzależniony od typu i stopnia zaawansowania nowotworu, warunków anatomicznych oraz stanu zdrowia pacjentki. Wykazano, że właściwie wykonana limfadenektomia podczas operacji chirurgicznych w ginekologii onkologicznej ma wpływ na wydłużenie całkowitego przeżycia pacjentek, pięcioletniego przeżycia oraz okresu wolnego od wznowy.[2] Poniższy artykuł prezentuje przegląd literatury oraz rekomendacji dotyczących obowiązującego zakresu limfadenektomii w poszczególnych nowotworach narządu płciowego kobiety w zależności od stopnia zaawansowania.
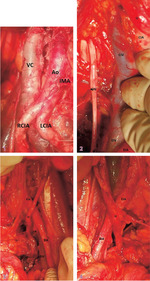
Przerzuty do węzłów chłonnych nie są charakterystyczne jedynie dla nowotworów o wysokim stopniu zaawansowania. W 5-9 proc. przypadków komórki nowotworowe są obecne w węzłach chłonnych we wczesnych stadiach choroby.[3] Spływ chłonki z narządu płciowego odbywa się jedną z kilku dróg: z trzonu macicy i górnej części szyjki chłonka spływa do węzłów chłonnych przymacicznych, które uchodzą do węzłów biodrowych wewnętrznych, z dna i górnej części trzonu wzdłuż więzadła właściwego jajnika kierują się do lędźwiowych (okołoaortalnych) lub poprzez kanał pachwinowy wzdłuż więzadła obłego do węzłów chłonnych pachwinowych powierzchownych, z dolnej części szyjki macicy i górnej części pochwy natomiast do węzłów biodrowych i biodrowych wewnętrznych, łącząc się również z węzłami okołoodbytniczymi i przedkrzyżowymi. Z okolicy jajnika chłonka odpływa w kierunku węzłów biodrowych wspólnych, zasłonowych i biodrowych wewnętrznych, natomiast z jajowodu jedynie do węzłów chłonnych około aortalnych (ryc. 1-4).[3,4] Obecnie uważa się, że nie należy rozgraniczać limfadenektomii miedniczej i okołoaortalnej, ponieważ przemieszczanie się komórek nowotworowych do węzłów chłonnych okołoaortalnych jest niezbędne do wytworzenia antygenowo swoistej tolerancji, a badania molekularne potwierdziły możliwość bezpośredniego przerzutowania do węzłów chłonnych tej okolicy z pominięciem niższych pięter.[5] Zgodnie z obowiązującą literaturą rozróżnia się cztery typy limfadenektomii miedniczej w zależności od zakresu zabiegu.[6] Biopsja węzła wartowniczego umożliwia ograniczenie zabiegu operacyjnego poprzez usunięcie pierwszego węzła na drodze spływu chłonki z określonego obszaru (ang. sentinel lymph node dissection, SLND], co daje możliwość uniknięcia następstw rozległej limfadenektomii, tj. obrzęków limfatycznych, uszkodzeń nerwów lub powikłań naczyniowych.[7] Oznaczenie ww. węzła możliwe jest metodą scyntygraficzną poprzez podanie radioaktywnego technetu, metodą barwnikową błękitem metylenowym, metodą skojarzoną barwnikowo-scyntygraficzną oraz metodą fluorescencyjną.[7] Drugim sposobem limfadenektomii, obecnie niezalecanym ze względu na niską swoistość, jest wycięcie jedynie powiększonych >1 cm węzłów chłonnych. Selektywne wycięcie węzłów chłonnych miednicy mniejszej wiąże się natomiast z usunięciem jedynie niewielkiej liczby węzłów chłonnych miedniczych. Obecnie standardem postępowania operacyjnego w oddziałach ginekologii onkologicznej jest procedura polegająca na całkowitym usunięciu tłuszczowej tkanki limfatycznej znajdującej się w okolicy naczyń biodrowych wspólnych, wewnętrznych i zewnętrznych oraz otworu zasłonowego. Miejsca te charakteryzują się wysokim prawdopodobieństwem wystąpienia przerzutów nowotworowych, a procedura ze względu na rozległość określana jest systemową limfadenektomią miednicy mniejszej.[6]
Limfadenektomia w raku jajnika
Rak jajnika jest jednym z najgorzej rokujących nowotworów narządu płciowego kobiety głównie ze względu brak występowania wczesnych objawów choroby oraz specyficznych markerów nowotworowych cechujących się wysoką specyficznością i czułością w niskich stadiach zaawansowania. Rozpoznanie choroby jest stawiane w przeważającej liczbie przypadków (70 proc.) w wysokim stadium zaawansowania. Zalecanym standardem postępowania w raku jajnika jest obecnie leczenie chirurgiczne polegające na całkowitej cytoredukcji w połączeniu z następową chemioterapią z użyciem karboplatyny z paklitakselem, a w przypadku dużego ryzyka operacji z pozostawieniem zmian >1 cm (ang. gross residual-bulky, GR-B) rozważenie chemioterapii neoadiuwantowej.
Obecność przerzutów nowotworowych raka jajnika w węzłach chłonnych jest charakterystyczna dla zarówno wczesnych, jak i zaawansowanych stadiów choroby (tab. 1), a przerzutowo zmienione węzły chłonne mogą stanowić odpowiednio 22-70 proc. wszystkich węzłów usuniętych podczas operacji.[8] Rozmieszczenie i częstość występowania dodatnich węzłów chłonnych zależy od typu histopatologicznego nowotworu (tab. 2). W przypadku nowotworów surowiczych pierwszym miejscem pojawienia się przerzutów są węzły okołoaortalne powyżej tętnicy krezkowej dolnej. Natomiast guzom niesurowiczym towarzyszą przerzuty zarówno w węzłach okołoaortalnych, jak i miedniczych.[9] Najczęściej dodatnie węzły chłonne okołoaortalne są zlokalizowane po lewej stronie aorty w górnej jej części, w drugiej kolejności wykrywane są pomiędzy aortą i żyłą główną dolną (30 proc.).[6] Wykazano, że zarówno w przedoperacyjnych badaniach obrazowych (czułość i specyficzność tomografii komputerowej w wykrywaniu przerzutów do węzłów chłonnych wynosi odpowiednio 65 i 65,5 proc.), jak i w badaniu palpacyjnym podczas operacji 1/3 pozytywnych węzłów chłonnych nie jest zmieniona makroskopowo.[10,11,12]

Tabela 1. Stopień zajęcia węzłów chłonnych w poszczególnych stopniach zaawansowania raka jajnika według FIGO (ang. International Federation of Gynecology and Obstetrics)[10]

Tabela 2. Częstość zajęcia węzłów chłonnych w zależności od typu histopatologicznego raka jajnika[10]
Dotychczas konsensus w zakresie limfadenektomii w raku jajnika nie został jednoznacznie osiągnięty. Badania randomizowane nie wykazały istotnego wydłużenia całkowitego przeżycia w przypadku wykonania systemowej limfadenektomii.[12,13], natomiast badania retrospektywne wiązały poprawę wyników leczenia z rozległym usunięciem węzłów chłonnych.[9,13] Należy podkreślić, że wcześniejsze badania randomizowane były wykonywane, zanim zabiegi cytoredukcji systemowej w raku jajnika zostały zaakceptowane jako standard postępowania. Znaczenie prognostyczne limfadenektomii miedniczej i okołoaortalnej u pacjentek z zaawansowanym rakiem jajnika poddanych całkowitej cytoredukcji jest obecnie analizowane w prospektywnym badaniu III fazy „Randomized, Multicentre Trial for Lymphadenectomy in Ovarian Neoplasms” (https://clinicaltrials.gov/ct2/show/NCT00712218), którego wyniki powinny być opublikowane w grudniu 2017 roku. Obecne rekomendacje NCCN (ang. National Comprehensive Cancer Network) zalecają usunięcie powiększonych lub podejrzanych nowotworowo węzłów chłonnych u pacjentów z zaawansowanym nowotworem jajnika.[14]
Podczas operacji raka jajnika dąży się do uzyskania całkowitej cytoredukcji z rozległą limfadenektomią miedniczą i okołoaortalną, bez pozostawienia makroskopowych ognisk nowotworowych (ang. no gross residual disease, NGR). W metaanalizie du Boisa i wsp. wykazano znaczne wydłużenie mediany całkowitego przeżycia w przypadku doszczętności zabiegu (NGR – 99,1 mies. v. 36,2 GR-1, ang. gross residual 1).[9] Znamienne wydłużenie pięcioletniego przeżycia (67,4 v. 59,2 proc.) oraz całkowitego przeżycia pacjentek zależy od radykalności zabiegu cytoredukcyjnego oraz zakresu limfadenektomii (jeżeli usunięto co najmniej 20 węzłów chłonnych okołoaortalnych) i wynika z doszczętności usunięcia zmian nowotworowych oraz możliwości określenia stopnia zaawansowania choroby nowotworowej, a w związku z tym wyboru właściwego leczenia skojarzonego.[6] Również badanie Eoh i wsp. potwierdza, że usunięcie co najmniej 20 węzłów chłonnych podczas zabiegu całkowitej cytoredukcji znamiennie wydłuża ogólne przeżycie pacjentek (p<0,001) oraz nieznacznie przedłuża czas wolny od progresji choroby (p=0,059) w porównaniu do pacjentek, u których wykonano selektywne usunięcie <20 węzłów chłonnych.[13] Pozostawienie pozytywnych węzłów chłonnych może być przyczyną oporności na chemioterapię i wiązać się z gorszym rokowaniem nie tylko z powodu słabszej penetracji leków stosowanych podczas następowej chemioterapii do zajętych nowotworowo węzłów chłonnych, lecz również z dalszym rozsiewem poprzez naczynia limfatyczne pomimo wykonania optymalnej cytoredukcji.[13]
W przypadku operacji GR-1 oraz GR-B korzyści z wykonanej limafadenektomii nie są tak znaczące, a często ryzyko rozległego zabiegu chirurgicznego, dużej utraty krwi, limfocele i pooperacyjnych obrzęków limfatycznych (7-22 proc. pacjentek) przewyższa korzyści związane z wydłużeniem czasu wolnego od wznowy o ok. 6 miesięcy.[12]
Wykazano, że u pacjentek w I stopniu zaawansowania nowotworu złośliwego jajnika wykonanie limfadenektomii ma pozytywny wpływ na rokowanie i w całej grupie badanej poprawia znacząco okres pięcioletniego przeżycia (87 v. 92,6 proc., p<0,001), a w szczególności w przypadku raka niejasnokomórkowego jajnika (85,9 v. 93,3 proc., P<0,001). Uważa się, że nie tylko rodzaj nowotworu, lecz również zakres wykonanej limfadenektomii ma wpływ na długość życia pacjentek. W przypadku niewykonania limfadenektomii pięcioletnie przeżycie w I stopniu zaawansowania wynosi 87 proc., natomiast w przypadku usunięcia ≥10 węzłów chłonnych osiąga wartość 93,8 proc., p<0,001.[15] U większości pacjentek w usuniętych węzłach chłonnych podczas rutynowego badania histopatologicznego nie wykryto ognisk nowotworowych. Według Chen i wsp. poprawa wyników leczenia była w tym przypadku związana z występowaniem mikroprzerzutów w usuniętych węzłach chłonnych, niemożliwych do wykrycia podczas rutynowego barwienia hematoksyliną i eozyną.[16] Wiele badań potwierdza znaczący wpływ rozległej limfadenektomii na przebieg i rokowanie raka jajnika. Jednakże występowanie, lokalizacja oraz obraz kliniczny przerzutów do węzłów chłonnych cechują się znaczną odmiennością w zależności od typu histopatologicznego, anatomicznej zmienności osobniczej i zaawansowania choroby, dlatego zakres zalecanej limfadenektomii nie został dotychczas jednoznacznie określony. Ponadto należy podkreślić, że zakres wykonywanej limfadenektomii zależy w dużym stopniu od doświadczenia i liczby zabiegów wykonanych przez operatora oraz tradycji chirurgicznej ośrodka. Istotne wydaje się ujednolicenie zaleceń oraz stworzenie ośrodków wyspecjalizowanych w tej procedurze.
Limfadenektomia w raku szyjki macicy
W krajach rozwijających się rak szyjki macicy jest jednym z najpoważniejszych problemów onkologicznych i stanowi ok. 13 proc. zachorowań na nowotwory u kobiet.[16] Według Globocan (ang. Global Cancer Statistics) nowotwór ten zajmuje obecnie trzecie miejsce pod względem występowania i czwarte pod względem śmiertelności wśród nowotworów u kobiet na świecie. Identyfikacja jednego z najważniejszych czynników ryzyka – infekcji typami onkogennymi wirusa brodawczaka ludzkiego (HPV) umożliwiła wdrożenie profilaktyki pierwotnej oraz zmniejszenie zachorowalności na przestrzeni ostatniej dekady.
Rozprzestrzenianie się raka szyjki macicy zachodzi w pierwszym etapie głównie drogą naczyń chłonnych do węzłów chłonnych miednicy mniejszej: węzłów chłonnych okołoszyjkowych, przymacicznych, biodrowych zewnętrznych i wewnętrznych, a następnie drogą węzłów chłonnych biodrowych wspólnych i pachwinowych do węzłów okołoaortalnych. W raku szyjki macicy pozytywne węzły chłonne okołoaortalne występują u 12 proc. pacjentek, a ich lokalizacja dotyczy najczęściej węzłów do poziomu tętnicy krezkowej dolnej.[17]