Praktyka kliniczna
Trądzik pospolity – nowe spojrzenie na etiologię schorzenia, najnowsze strategie postępowania
Dr hab. med. Beata Bergler-Czop
W pracy podjęto próbę usystematyzowania najnowszych doniesień dotyczących etiologii i leczenia trądziku pospolitego, ze szczególnym uwzględnieniem stosowania retinoidów miejscowych i ogólnych jako jedynych leków, które działają na większość czynników etiologicznych acne
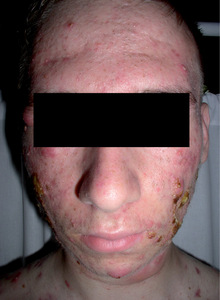
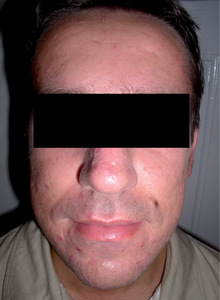
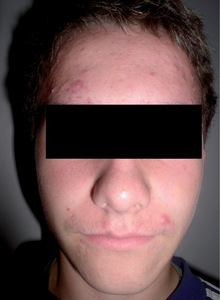
Trądzik pospolity jest najczęściej diagnozowaną dermatozą zapalną u pacjentów pomiędzy 11. a 30. r.ż. Uważa się, że dotyczy on około 80 proc. osób w tej grupie wiekowej lub nawet, uwzględniając zmiany mało nasilone, 100 proc. młodych ludzi. Zmiany w 95 proc. są umiejscowione na twarzy i w górnych okolicach tułowia, sporadycznie w innych partiach ciała, i ze względu na tę lokalizację oraz przewlekły charakter schorzenia niejednokrotnie stanowi ono poważny problem psychologiczny dla pacjenta. W artykule przedstawiamy najnowsze doniesienia dotyczące etiologii i terapii acne (fot. 1,2,3).
Współczesne poglądy na etiopatogenezę trądziku
Etiopatogeneza trądziku jest wieloczynnikowa. U wszystkich chorych na trądzik występuje: wzmożona produkcja łoju, nadmierne rogowacenie przewodów wyprowadzających i ujść gruczołów łojowych, rozwój flory bakteryjnej, a także uwalnianie mediatorów zapalnych w skórze.
Mikrozaskórnik i keratynizacja wewnątrzmieszkowa
Pierwotnym wykwitem w trądziku, który zapoczątkowuje kaskadę zmian zapalnych, jest mikrozaskórnik. Mikrozaskórniki mogą tworzyć się pod wpływem różnych czynników, takich jak: niedobór kwasu linolenowego, nadmierna sekrecja androgenów lub nadmiar wolnych kwasów tłuszczowych. Czynnikiem warunkującym przekształcenie się mikrozaskórnika w zaskórnik jest keratynizacja wewnątrzmieszkowa, która prawdopodobnie spowodowana jest podrażnieniem ścian mieszka włosowego przez materiał łojowy i bakterie, co prowadzi do nadprodukcji i gromadzenia korneocytów. Zjawisku towarzyszy nadprodukcja tonofilamentów, desmosomów oraz keratyny K6 i K16. Wynikiem tego jest wytworzenie, przy udziale enzymu transglutaminazy, skeratynizowanej ,,koperty”. Proces ten powoduje zwężenie kanału wyprowadzającego i utrudnia usuwanie zawartości gruczołu łojowego na powierzchnię skóry. Zjawisko to dotyczy głównie przerośniętych gruczołów łojowych ze szczątkowym włosem w fazie anagenu. W proces keratynizacji zaangażowane są również cytokiny, głównie IL-1, o działaniu prozapalnym.[1,2,3]
W procesie tworzenia zaskórnika rolę odgrywa również zawartość lipidowa mieszka włosowego. Łój w obrębie gruczołów i przewodów wyprowadzających jest jałowy i nie zawiera wolnych kwasów tłuszczowych. Kolonizacja bakteryjna (zwłaszcza Propionibacterium acnes), dzięki odpowiednim enzymom, umożliwia hydrolizę składników łoju do wolnych kwasów tłuszczowych o działaniu drażniącym i chemotaktycznym. Obecnie uważa się jednak, że nie tylko ten składnik odgrywa rolę w etiologii trądziku. Duże znaczenie przypisuje się tu utlenianiu skwalenu oraz niedoborowi kwasu linolowego. Prawdopodobnie nasilona sekrecja łoju sprzyja niedoborowi kwasu linolowego, co nasila komedogenezę. Wykazano również zjawisko znacznego nagromadzenia i zwiększonej aktywności neutrofili w mikrozaskórnikach. Dotyczyło to także neutrofili z okolic skóry niezajętych procesem zapalnym.[3,4,5]
Kolonizacja bakteryjna
Nadmierna produkcja i gromadzenie łoju oraz zamknięcie ujścia gruczołu łojowego sprzyjają kolonizacji bakteryjnej. Mikrozaskórniki zamieszkuje przede wszystkim maczugowiec beztlenowy - Propionibacterium acnes. Inne to m.in.: ziarniniak tlenowy - Staphylococcus epidermidis oraz drożdżak lipofilny - Malassezia furfur. Drobnoustrój ten dzięki obecności lipazy hydrolizuje dwu- i triglicerydy łoju do wolnych kwasów tłuszczowych (FFA - free fatty acids). Wolne kwasy tłuszczowe, które powstają w procesie hydrolizy, mają działanie drażniące, prozapalne oraz nasilające rogowacenie przymieszkowe. Działanie prozapalne mają również: hialurondaza, proteazy i nauraminidazy, produkowane przez Propionibacterium acnes. Drobnoustrój ten uwalnia także niskocząsteczkowe czynniki chemotaktyczne (peptydy), przyciągające granulocyty obojętnochłonne, oraz aktywuje zarówno dopełniacz na drodze alternatywnej, jak i klasyczną odpowiedź immunologiczną. Aktywatorem alternatywnego szlaku dopełniacza jest ściana komórkowa Propionibacterium acnes, która zawiera mannozę. Pod wpływem Propionibacterium acnes dochodzi także do masywnej produkcji anionów nadtlenkowych przez keratynocyty, które w połączeniu z tlenkiem azotu tworzą peroksynitraty, przyczyniające się do rozpadu keratynocytów.[5,6,7,8]
Receptory Toll-like
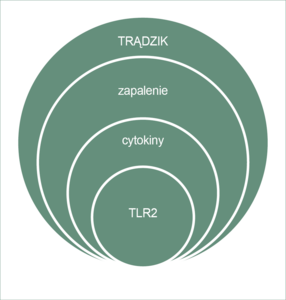
Receptory TLR (Toll-like Receptor) są częścią wrodzonej odpowiedzi immunologicznej typu komórkowego. Receptory tej grupy znajdują się m.in. na keratynocytach i w komórkach Langerhansa naskórka. TLR2 (Toll-like Receptor-2) znajdujący się w monocytach identyfikuje składniki ścian bakterii Gram-dodatnich, m.in. Propionibacterium acnes. Udowodniono, że aktywacja TLR2 w monocytach nasila produkcję TNF-α, IL-1 β i IL-8, co przyciąga do mieszka neutrofile i limfocyty. Natomiast ekspresja TLR2 na keratynocytach hamowana jest przez sole cynku, które są stosowane obecnie głównie jako składnik preparatów złożonych w terapii acne. Receptory te dzielą się na subpopulacje zewnątrz- i wewnątrzkomórkowe. Receptory na powierzchni komórek wykazują przede wszystkim aktywność antybakteryjną, pobudzają aktywność fagocytarną i sygnały pobudzające dojrzewanie komórek. Cząstki wewnątrzkomórkowe rozpoznają głównie wirusy i aktywują geny stymulujące aktywność przeciwwirusową (ryc. 1).[8,9]
Zaburzenia immunologiczne
Chociaż u chorych na trądzik nie wykazano pierwotnych zaburzeń immunologicznych, obserwuje się jednak nadmierną reakcję układu immunologicznego na antygeny Propionibacterium acnes, wyrażającą się podwyższonym mianem przeciwciał, i nadmiernie nasiloną odpowiedź zapalną na śródskórne wstrzyknięcie Propionibacterium acnes, w porównaniu z populacją zdrową. U niektórych badanych stwierdzono nadmierną produkcję IgA oraz nadwrażliwość na standardowe alergeny stosowane w testach.
Wykazano również, że zaburzenia immunologiczne, obok odpowiedzi zapalnej, poprzedzają hiperproliferację keratynocytów na drodze przypominającej reakcję alergiczną typu IV. Aktywowane w ten sposób cytokiny aktywują komórki śródbłonka do produkcji markerów zapalnych naczyń – E-selektyny, cząsteczek adhezyjnych komórek naczyniowych (VCAM-1), cząsteczek adhezji międzykomórkowej (ICAM-1) oraz antygenów HLA leukocytów w naczyniach krwionośnych dookoła mieszka włosowego.[2,10]
Wykazano, że cytokiny prozapalne uwalniane kaskadowo w trądziku, aktywują czynnik transkrypcyjny AP-1 (activator protein). AP-1 indukuje geny metaloproteinazy macierzy zewnątrzkomórkowej (MMP), która rozkłada i przebudowuje macierz skóry.