Znaczenie inozytoli i proporcji ich izomerów stosowanych w celu poprawy profilu metabolicznego i hormonalnego oraz płodności u kobiet
prof. dr hab. n. med. Mirosław Wielgoś1
prof. dr hab. n. med. Dorota Bomba-Opoń1
prof. dr hab. n. med. Piotr Laudański2-4
prof. dr hab. n. med. Piotr Sieroszewski5
prof. dr hab. n. med. Ewa Wender-Ożegowska6
- Zastosowanie inozytoli w regulacji układu hormonalnego, cyklu miesiączkowego i wspieraniu płodności, zwłaszcza u kobiet z PCOS
- Korzyści wynikające z suplementacji inozytoli na etapie planowania ciąży oraz w procedurach wspomaganego rozrodu
- W poszukiwaniu proporcji idealnej – przegląd badań dotyczących kombinacji mio-inozytolu i D-chiro-inozytolu
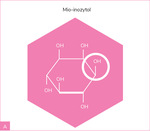
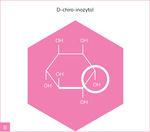
Inozytole, będące chemicznie cyklicznym alkoholem cukrowym, pełnią istotną funkcję w regulacji procesów metabolicznych i hormonalnych. W praktyce klinicznej szczególne znaczenie mają dwa najczęściej badane izomery: mio-inozytol (MIO) oraz D-chiro-inozytol (DCI) (ryc. 1). Obydwa odgrywają rolę w metabolizmie glukozy i lipidów, regulacji cyklu miesiączkowego oraz w poprawie jakości komórek jajowych.
Suplementacja inozytoli znajduje zastosowanie zwłaszcza w terapii zespołu policystycznych jajników (PCOS – polycystic ovary syndrome)1. Wykazano, że inozytole u kobiet z PCOS wpływają na poprawę stanu metabolicznego i hormonalnego, a zarazem przywracają spontaniczną owulację. Również w procedurach wspomaganego rozrodu (ART – assisted reproductive technology) inozytol poprawiał skuteczność stymulacji jajników2.
Obie izoformy inozytolu, tj. MIO i DCI, występujące fizjologicznie w osoczu w proporcji 40 : 1 zdolne są do przeciwdziałania skutkom insulinooporności, gdyż ich aktywność prawdopodobnie obejmuje różne mechanizmy biologiczne3. W jajnikach stosunek MIO do DCI wynosi 100 : 1, jednak w przypadku hiperinsulinemii u kobiet z PCOS ulega on znacznemu zmniejszeniu pod wpływem epimerazy stymulowanej przez insulinę (ryc. 2). Istniejące dowody wskazują, że zaburzenie regulacji androgenów wewnątrz jajników, prawdopodobnie spowodowane brakiem równowagi między MIO a DCI, może być główną przyczyną zatrzymania wzrostu pęcherzyków w PCOS4.
Modulacja aktywności insuliny wpływa na szlaki steroidogenezy, prowadząc do zmniejszenia syntezy androgenów na poziomie zarówno jajników, jak i nadnerczy3. Suplementacja DCI w odpowiedniej proporcji z MIO pomaga w redukcji objawów związanych z hiperandrogenizmem: hirsutyzmu, trądziku i zaburzeń owulacji, dzięki czemu poprawia jakość życia pacjentek5.
Wpływ inozytoli na regulację układu hormonalnego
Inozytol jest głównie wbudowywany w błony komórkowe w postaci fosfatydylo-mio-inozytolu, będącego prekursorem trifosforanu inozytolu (Ins-1,4,5P3, InsP3), który działa jako wtórny przekaźnik regulujący aktywność kilku hormonów, takich jak: hormon folikulotropowy (FSH – follicle-stimulating hormone), hormon tyreotropowy (TSH – thyroid-stimulating hormone) i insulina6,7. Chociaż pula wewnątrzkomórkowego inozytolu składa się głównie z MIO (>99%) w większości tkanek, odnotowano istotne różnice w stężeniach MIO i DCI – stereoizomeru obecnego w tkance tłuszczowej, mięśniowej i wątrobie. To zróżnicowanie w dystrybucji odzwierciedla odmienne funkcje, jakie oba izomery prawdopodobnie pełnią w tych tkankach. Ich proporcje są aktywnie utrzymywane, ponieważ MIO jest enzymatycznie przekształcany w DCI za pomocą zależnej od NAD/NADH epimerazy, zgodnie z zapotrzebowaniem tkankowym, a reakcja enzymatyczna jest stymulowana przez insulinę8.
Dysregulacja aktywności epimerazy wpływa na stosunek MIO do DCI i może zakłócać sygnalizację hormonów, takich jak insulina i FSH. Opublikowane wyniki badań wskazują na występowanie defektu dostępności i/lub wykorzystania MIO i/lub DCI w tkankach u kobiet z PCOS8. Prawdopodobnie przyczynia się to do insulinooporności charakterystycznej dla tego zespołu, gdyż dwa główne stereoizomery inozytolu pełnią odrębne funkcje w sygnalizacji insulinowej. DCI jest głównie zaangażowany w syntezę glikogenu (wątroba, tkanka tłuszczowa i mięśnie), podczas gdy MIO odpowiada za aktywację transporterów glukozy i jej wykorzystanie8,9. Na poziomie jajników DCI jest odpowiedzialny za nadprodukcję testosteronu, podczas gdy MIO uczestniczy w sygnalizacji FSH10. Biorąc pod uwagę fakt, że aktywność epimerazy regulującej stosunek MIO do DCI jest zależna od insuliny, a jajniki nigdy nie stają się insulinooporne (w przeciwieństwie do mięśni i wątroby), zakłada się, że pacjentki z PCOS mogą wykazywać zwiększoną epimeryzację MIO do DCI w jajnikach. Prowadziłoby to do nadprodukcji DCI i niedoboru MIO11,12.
Mio-inozytol i D-chiro-inozytol działają synergistycznie, poprawiając z wykorzystaniem różnych mechanizmów biochemicznych wrażliwość na insulinę. Pierwszy z nich (MIO) jest prekursorem inozytolu trifosforanu, który reguluje wewnątrzkomórkową sygnalizację szlaku insulinowego. Natomiast drugi (DCI) jest zaangażowany w przekształcanie glukozy w glikogen. Terapia łączona MIO i DCI prowadziła do znaczącego zmniejszenia stężenia insuliny na czczo w grupie badanej (p <0,05), która obejmowała kobiety z otyłością i ze zdiagnozowanym PCOS13. Wskaźnik HOMA (homeostasis model assessment) również uległ znacznemu zmniejszeniu zarówno po terapii łączonej MIO i DCI (p <0,05), jak i po zastosowaniu samego MIO13,14. Poprawa insulinowrażliwości i tym samym metabolizmu glukozy może pośrednio wpływać na regulację poziomu hormonu luteinizującego (LH – luteinizing hormone). Wyniki badania dotyczącego terapii łączonej MIO oraz DCI potwierdziły znaczący spadek stężenia LH (mj.m./ml) w grupie badanej (p <0,05), co wskazuje na poprawę równowagi hormonalnej, tak istotnej dla kobiet z PCOS, u których poziom tego hormonu jest często podwyższony13. Suplementacja MIO wpłynęła również na poprawę stosunku LH do FSH oraz obniżenie stężenia prolaktyny15.