Choroba niedokrwienna serca
Klinika Intensywnej Terapii Kardiologicznej, Instytut Kardiologii, Warszawa
Nowe markery niedokrwienia w ocenie ryzyka w ostrym zespole wieńcowym bez uniesienia odcinka ST
Marta Załęska-Kocięcka, Anna Konopka
Wprowadzenie
Ocena ryzyka u pacjentów z ostrym zespołem wieńcowym bez przetrwałego uniesienia odcinka ST (non-ST elevation acute coronary syndrome, NSTE-ACS) wymaga szczególnej uwagi z kilku powodów. Po pierwsze, NSTE-ACS występują częściej niż ostre zespoły wieńcowe z uniesieniem odcinka ST (ST elevation acute coronary syndrome, STE-ACS), co potwierdzają dane z rejestrów [1]. Po drugie, rokowanie w tej populacji chorych istotnie zmienia się w czasie na niekorzyść pacjentów z NSTE-ACS w porównaniu z chorymi z STE-ACS. Ryzyko zgonu wewnątrzszpitalnego w grupie chorych z NSTE-ACS jest mniejsze w porównaniu z ryzykiem w grupie chorych z STE-ACS, jednak po 6 miesiącach wyrównuje się z ryzykiem w grupie STE-ACS [1-3], a po 4 latach od incydentu jest dwukrotnie większe [4]. Po trzecie, zgodnie z obowiązującymi „Wytycznymi dotyczącymi diagnostyki i leczenia ostrych zespołów wieńcowych bez przetrwałego uniesienia odcinka ST” [5] stratyfikacja ryzyka na podstawie wywiadu, oceny klinicznej, badania przedmiotowego, obrazu elektrokardiogramu oraz stężenia biomarkerów ma podstawowe znaczenie w wyborze optymalnej strategii postępowania i powinna być wykonywana u wszystkich chorych (klasa zaleceń I, poziom dowodów A).
Biomarkery w NSTE-ACS są narzędziami diagnostycznymi i rokowniczymi. Odzwierciedlają różne aspekty patofizjologii, czyli martwicę mięśnia sercowego, stan zapalny, aktywację płytek czy aktywację neurohormonalną. Autorki w artykule przedstawiają znaczenie rokownicze biomarkerów niedokrwienia (zwłaszcza przebadanych niedawno i dopiero wdrażanych do praktyki klinicznej) w populacji pacjentów z NSTE-ACS.
Troponiny
Wśród biomarkerów niedokrwienia troponiny sercowe – troponina I (cTnI) i troponina T (cTnT) – stanowią złoty standard zarówno w diagnostyce NSTE-ACS, jak i w ocenie ryzyka w tej populacji chorych. Zawdzięczają to przede wszystkim 100% swoistości dla kardiomiocytów. Należy jednak pamiętać, że wzrost stężenia troponin (cTn) we krwi nie wyjaśnia mechanizmu powstania martwicy komórek mięśnia serca, zatem może świadczyć nie tylko o niedokrwiennym uszkodzeniu mięśnia serca, ale o każdej sytuacji patologicznej, w której dochodzi do przeciążenia, niewydolności i uszkodzenia komórek mięśnia serca, nawet przy prawidłowym jego ukrwieniu. Rokownicze znaczenie troponin w przebiegu NSTE-ACS zostało potwierdzone w ocenie krótko- (30 dni) [6,7] i długoterminowej [8]. Wprowadzenie wysokoczułych testów troponinowych nadało troponinom wykrywanym za ich pomocą nowego znaczenia, czyniąc ten znany od wielu lat biomarker czułym wskaźnikiem użytecznym w bardzo wczesnym wykrywaniu zawału mięśnia sercowego i określaniu rokowania jego następstw.
Nowe wysokoczułe testy troponinowe (hs cTn) wykrywają już 10-100-krotnie mniejsze stężenia troponin przy zachowanej precyzji pomiaru (współczynnik zmienności [CV] <10%), przez co pozwalają wykryć wzrost cTn we wczesnej fazie OZW, kiedy stężenie tego biomarkera jest poniżej progu detekcji tradycyjnych testów. Zastosowanie hs cTn wiąże się nie tylko z wcześniejszą diagnostyką, ale również z częstszym rozpoznawaniem zawału mięśnia sercowego, tzn. stawia się je u części chorych, u których przed erą wysokoczułych testów rozpoznawano by niestabilną chorobę wieńcową [9]. Są to chorzy z dodatnim wynikiem testu hs cTn i ujemnym wynikiem klasycznego testu 4 generacji cTn (hs cTn [+]/cTn [-]). Należy jednak pamiętać, że wysoką analityczną czułość uzyskano kosztem zmniejszonej swoistości testu, co wykazał Keller i wsp. [10].
Mniejsza swoistość i większa czułość, pozwalająca na detekcję troponin nawet u osób zdrowych [11,12], początkowo budziły dużo wątpliwości i stawiały pod znakiem zapytania przyszłość testu. Potwierdzono także, że do uwolnienia troponin dochodzi nie tylko w przebiegu martwicy mięśnia sercowego. Obecnie obok martwicy mięśnia sercowego proponowanych jest 5 potencjalnych mechanizmów odpowiedzialnych za uwolnienie troponin: apoptoza [13], przebudowa mięśnia sercowego [14], uwolnienie produktów proteolizy troponin [15,16], zwiększenie przepuszczalności błony komórkowej niezwiązanej z martwicą komórek [17] i aktywne wydzielanie pęcherzykowe [18].
Diagnostyka ostrych zespołów wieńcowych (acute coronary syndrome, ACS) za pomocą troponin oznaczanych metodą wysokoczułą jest wciąż przedmiotem dyskusji i badań, podobnie jak ocena ich wartości prognostycznej. Wyniki badań są niejednoznaczne, a dodatkowym źródłem trudności są rozbieżności w zakresie metodyki badań, głównie przyjętych progów odcięcia.
Pacjenci z podejrzeniem ACS i dodatnim wynikiem testu hs cTn przy ujemnym wyniku klasycznego testu cTn (hs cTn [+]/cTn [-]) stanowią nową grupę ryzyka. Rosnąca liczba badań dostarcza dowodów, że ryzyko zgonu i zdarzeń sercowo-naczyniowych w tej grupie chorych są porównywalne z ryzykiem stwierdzanym w grupie chorych z zawałem mięśnia sercowego potwierdzonym za pomocą obu testów (hs cTn [+]/cTn [+]). Wskazują na to wyniki badania Hochholzera i wsp. [19]. W analizie statystycznej z użyciem testu Kaplana-Meiera uwzględniającej dane 1159 niewyselekcjonowanych chorych przyjętych z podejrzeniem ACS i bólem w klatce piersiowej trwającym krócej niż 12 godzin wykazano 4-krotnie większe ryzyko zgonu wśród chorych hs cTnT (+)/cTnT (-) (próg odcięcia dla dodatniego wyniku obu testów: stężenie >99 percentyla i CV <10%) w porównaniu z chorymi bez wzrostu troponin w obu testach wykonanych przy przyjęciu (p <0,001) [19]. Ryzyko zawału mięśnia sercowego w okresie 2 lat (nie licząc incydentu przy przyjęciu) było porównywalne w grupie hs cTnT (+)/cTnT (-) i hs cTnT (+)/cTnT (+) [19].
Autorzy potwierdzili przewagę oznaczania troponin metodą wysokoczułą nad oznaczaniem tradycyjnym testem w ocenie ryzyka wystąpienia w ciągu 2 lat: zgonu (pole pod krzywą [AUC] dla hs cTnT 0,79 vs 0,69, p <0,001), zawału mięśnia sercowego (AUC dla hs cTnT 0,62 vs 0,54, p=0,02) oraz zgonu z przyczyn sercowo-naczyniowych lub zawału mięśnia sercowego (AUC dla hs cTnT 0,70 vs 0,60, p <0,001) [19]. W 4-letniej obserwacji wykazano również przewagę zastosowania hs cTnT w ocenie ryzyka poważnych zdarzeń sercowo-naczyniowych (zgonu lub zawału serca niezakończonego zgonem) w analizie krzywych ROC (AUC dla hscTn 0,691 vs 0,639 dla cTnT, p=0,004) [19].
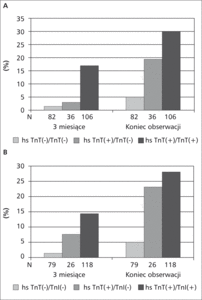
Rycina 1. [A, B] Ryzyko zgonu, zawału mięśnia sercowego niezakończonego zgonem lub hospitalizacji z powodu niewydolności serca w ciągu 3 miesięcy i po zakończeniu obserwacji.
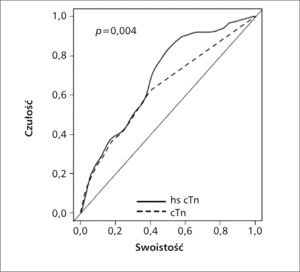
Rycina 2. Przewaga wartości prognostycznej wysokoczułego testu troponinowego (hs cTn) nad testem klasycznym (cTn) w ocenie ryzyka zgonu w ciągu 4 lat od incydentu NSTE-ACS w analizie krzywych ROC.
Melki i wsp., porównując hs cTn, cTnT i cTnI w mniejszej grupie, bo 233 chorych, przyjętych z podejrzeniem NSTE-ACS i objawami trwającymi średnio 5 godzin (zakres 3,3-7,5 godzin), za pomocą wysokoczułego testu troponinowego wykonanego w ciągu 2 godzin od przyjęcia, zidentyfikowali grupę 36 chorych z NSTE-ACS hs cTnT (+)/cTnT (-) i 26 chorych z NSTE-ACS hs cTnT (+)/cTnI (-) [20]. Wśród tych chorych 3-miesięczne i około 2-letnie (zakres 17-27 miesięcy) ryzyko zgonu, zawału mięśnia sercowego niezakończonego zgonem oraz hospitalizacji z powodu niewydolności serca było większe niż u chorych z ujemnym wynikiem każdego z testów i zbliżało się do ryzyka pacjentów z NSTE-ACS hs cTnT (+)/cTnT (+) oraz hs cTnT (+)/cTnI (+), co przedstawiają ryciny 1A i 1B [20]. W analizie z użyciem krzywych ROC nie wykazano jednak istotnych różnic między testami dla wystąpienia złożonego punktu końcowego. Uwzględnienie informacji o bezwzględnym lub względnym wzroście po 2 godzinach od pierwszego pobrania nie wpłynęło na wzrost wartości predykcyjnej wysokoczułego testu. Wieloczynnikowa analiza statystyczna przeprowadzona metodą Coxa wykazała, że hs cTnT jest niezależnym czynnikiem ryzyka wystąpienia złożonego punktu końcowego zarówno w 3-miesięczym, jak i 2-letnim okresie obserwacji [20]. Doniesienia te są zbieżne z wynikami wspomnianej już pracy Hochholzera i wsp. [19], którzy wykazali przewagę testu wysokoczułego nad tradycyjnym w ocenie ryzyka zgonu w wieloczynnikowej analizie proporcjonalnych zagrożeń Coxa przy uwzględnieniu zmiennej w postaci wyniku skali ryzyka TIMI, która uwzględnia wzrost stężenia klasycznie oznaczanej troponiny >0,010 µg/l. Dołączenie danych o stężeniu hs cTn do analizy uwzględniającej wynik tradycyjnego testu powoduje istotną statystycznie poprawę klasyfikacji pacjentów pod względem ryzyka zgonu [19].
Najbardziej odległe rokowanie u chorych z NSTE-ACS hs cTn (+)/cTn (-) określili Ndreppa i wsp., którzy wykazali, że śmiertelność całkowita w ciągu 4 lat od hospitalizacji z powodu podejrzenia NSTE-ACS jest porównywalna w grupie z NSTE-ACS hs cTn (+)/cTnT (-) i NSTE-ACS hs cTn (+)/cTnT (+) (25,1 vs 23,6%) i jednocześnie jest istotnie większa niż w grupie niestabilnej choroby wieńcowej (unstable angina, UA), czyli bez wzrostu stężenia troponin w obu testach (5,2% dla NSTE-ACS hs cTnT [-]/cTnT [-], p <0,001), przy braku istotnych statystycznie różnic między powyższymi 3 grupami w zakresie stosowanego leczenia inwazyjnego i farmakologicznego [21]. Przewagę wysokoczułego testu troponinowego wykazano również w ocenie punktu końcowego, jakim była śmiertelność w 4-letniej obserwacji [21]. Na rycinie 2 krzywe rozbiegają się w górnej części, co odpowiada przewadze wysokoczułego testu w grupie chorych ze stężeniem troponiny T poniżej progu detekcji klasycznego testu. W badaniu nie stwierdzono natomiast istotnych różnic między 3 powyższymi grupami chorych w zakresie śmiertelności w okresie 60 dni oraz drugorzędowych punktów końcowych (zawał mięśnia sercowego niezakończony zgonem, konieczność ponownej rewaskularyzacji) w okresie 60 dni i 4 lat [21].
Wyniki powyższych badań potwierdzają dodatkową wartość prognostyczną wysokoczułych testów troponinowych w porównaniu z testami 4 generacji.
Białko wiążące kwasy tłuszczowe typu sercowego
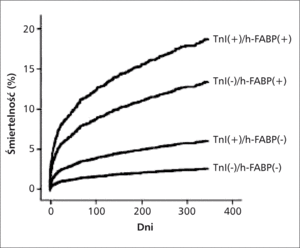
Białko wiążące kwasy tłuszczowe typu sercowego (heart-type fatty acid binding protein, h-FABP) jest niskocząsteczkowym białkiem występującym w cytoplazmie kardiomiocytów. Znajduje się również w mięśniach szkieletowych, gdzie jego stężenie jest 10-krotnie mniejsze niż w mięśniu sercowym, dlatego przypisuje się mu stosunkowo dużą swoistość narządową. Inną zaletą h-FABP jest wczesny wzrost stężenia we krwi w przebiegu ostrego zespołu wieńcowego – stężenie powyżej punktu odcięcia obserwuje się już po 30 minutach od początku bólu w klatce piersiowej, a maksymalne stężenie po ok. 4 godzinach.
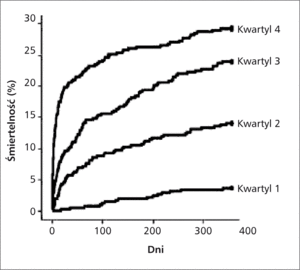
Rycina 3. Krzywe przeżycia Kaplana-Meiera w zależności od kwartylu stężenia h-FABP po skorygowaniu o ryzyko związane ze stężeniem białka CRP oraz czynnikami ryzyka skali GRACE [24].
Wykazano również, że stężenie tego białka może wzrastać nie tylko w niedokrwieniu, ale też w przebiegu przeciążenia hemodynamicznego lewej komory, do którego dochodzi w takich stanach, jak: nadciśnienie tętnicze, niedomykalność lub stenoza zastawki aortalnej, a także zastoinowa niewydolność serca [22,23]. Wykazano, że h-FABP usuwane jest przez nerki, a więc jego wartość diagnostyczna może być ograniczona u chorych z niewydolnością nerek. Jeszcze niedawno z h-FABP wiązano duże nadzieje w diagnostyce ostrego zespołu wieńcowego, ponieważ jego stężenie wzrasta wcześniej niż klasycznych troponin. Jego znaczenie diagnostyczne w ACS będzie najprawdopodobniej ograniczone ze względu na wprowadzenie wysokoczułych testów troponinowych. Z drugiej strony wiadomo, że nowy test troponinowy jest mniej swoisty i być może w przypadku wątpliwości diagnostycznych dla potwierdzenia rozpoznania ostrego zespołu wieńcowego będzie konieczne wykonanie innego testu, na przykład oznaczenie stężenia h-FABP.