Celem diagnozy pacjenta z podejrzeniem CTEPH jest przede wszystkim potwierdzenie rozpoznania, ale też ocena stopnia PH i dysfunkcji prawej komory, które określają ryzyko operacyjne. Kluczowe znaczenie ma również ocena dostępności chirurgicznej przewlekłych zmian zakrzepowo-zatorowych, pozwalająca ustalić, czy pacjent będzie kandydatem do leczenia operacyjnego. Próba oszacowania stopnia rozległości współistniejącej choroby naczyniowej małych tętnic płucnych to kolejny istotny element w kwalifikacji przedoperacyjnej.
Dla określenia ryzyka operacyjnego niezbędna jest ocena funkcji wątroby i nerek. Przed zabiegiem oznacza się też stężenie przeciwciał antyfosfolipidowych (antykoagulantu tocznia, przeciwciał antykardiolipinowych), co pomaga zaplanować intensywność leczenia przeciwzakrzepowego po operacji.
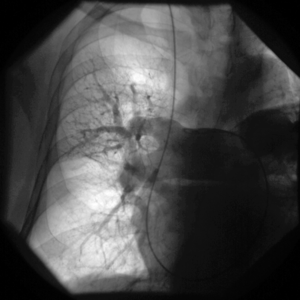
Rycina 3. Arteriografia kontrastowa tętnicy płucnej. Prawie całkowity brak unaczynienia płuca prawego. Widoczne nieliczne tętnice płucne u podstawy płata górnego płuca prawego.
Podstawowym badaniem obrazowym w diagnostyce przyczyn PH jest scyntygrafia perfuzyjna płuc. Prawidłowy obraz scyntygraficzny płuc wyklucza CTEPH. Jednak stwierdzenie zaburzeń perfuzji segmentalnych lub nawet większych nie jest specyficzne dla CTEPH i może występować na przykład w zwłóknieniu śródpiersia, guzach naczyń płucnych czy zapaleniu dużych tętnic płucnych. Zwykle wykonuje się więc także tomografię komputerową klatki piersiowej z opcją naczyniową. Umożliwia ona nie tylko zobrazowanie naczyń płucnych, ale także ocenę ewentualnych patologii innych struktur klatki piersiowej. Opisano wiele nieprawidłowości w TK pacjentów z CTEPH, w tym tak zwaną mozaikową perfuzję w obrazie wysokiej rozdzielczości (HRCT) (ryc. 1), poszerzenie pnia i głównych gałęzi tętnicy płucnej oraz redukcję światła naczyń płucnych wskazującą na obecność materiału zatorowego (ryc. 2). Doświadczony radiolog potrafi w TK wstępnie zróżnicować charakter zmian ostrych i przewlekłych w tętnicach płucnych. W innych postaciach przedwłośniczkowego PH, najczęściej w zespole Eisenmengera, może dochodzić do miejscowego wykrzepiania w poszerzonych tętnicach płucnych, co czasem trudno zróżnicować z CTEPH.
Postawienie wstępnego rozpoznania CTEPH zawsze wymaga potwierdzenia PH w pomiarach hemodynamicznych podczas cewnikowania prawego serca i wykonania, najlepiej jednocześnie, klasycznej kontrastowej arteriografii tętnicy płucnej, którą nadal uważa się za złoty standard w diagnostyce i kwalifikacji do operacji CTEPH (ryc. 3) [4].
Cewnikowanie prawego serca przeprowadza się nie tylko dla potwierdzenia rozpoznania i określenia charakteru PH (przedwłośniczkowe vs pozawłośniczkowe), ale też dla oceny jego ciężkości oraz stopnia upośledzenia funkcji prawej komory w spoczynku. Wykonuje się je z pomiarem średniego ciśnienia w tętnicy płucnej (PAP), indeksu sercowego (cardiac index, CI), naczyniowego oporu płucnego (pulmonary vascular resistance, PVR), średniego ciśnienia w prawym przedsionku (RAPm) i mieszanej saturacji krwi żylnej. Pomiary hemodynamiczne są również podstawą kwalifikacji do leczenia operacyjnego i oceny jego ryzyka. Im bardziej upośledzona jest funkcja prawej komory, tym większe jest ryzyko związane z zabiegiem. Stwierdzenie bardzo wysokiego, nieadekwatnego do ilości materiału zatorowego naczyniowego oporu płucnego (PVR >1000-1200 dyn × s × cm-5) wskazuje na większy stopień zajęcia małych tętnic płucnych procesem chorobowym i większe prawdopodobieństwo powikłań pooperacyjnych.
Kwalifikacja pacjentów do leczenia operacyjnego
Leczenie operacyjne, trombendarterektomię płucną, uznaje się za metodę leczenia z wyboru u chorych z CTEPH. Przed podjęciem decyzji o PEA prowadzone powinno być jednak przynajmniej 3-miesięczne leczenie przeciwzakrzepowe, zwykle antagonistą witaminy K z utrzymaniem INR w granicach 2,0-3,0. Kluczowa dla określenia możliwości przeprowadzenia operacji jest dostępność zmian zakrzepowo-zatorowych dla interwencji kardiochirurgicznej. Nie ma jednak jednoznacznych kryteriów definiujących ją. Przyjęto, że dostępne techniki chirurgiczne pozwalają usuwać zorganizowane skrzepliny zlokalizowane w tętnicach głównych i płatowych, ale bardziej doświadczeni kardiochirurdzy skutecznie przeprowadzają endarterektomię materiału zatorowego z poziomu tętnic segmentalnych.
Klinicznym wskazaniem do PEA jest narastająca duszność wysiłkowa i ograniczenie tolerancji wysiłku określane jako przynajmniej II klasa czynnościowa wg NYHA/WHO. Kryteria hemodynamiczne to naczyniowy opór płucny ≥300 dyn × s × cm-5 przy średnim ciśnieniu w tętnicy płucnej ≥40 mm Hg. Warunkiem rozważania wykonania PEA jest brak ciężkich chorób współistniejących, a u pacjentów z czynnikami ryzyka choroby niedokrwiennej serca należy przed podjęciem decyzji wykonać koronarografię [16].
Diagnostyka CTEPH i wybór metody leczenia powinny być przeprowadzane w ośrodkach doświadczonych w prowadzeniu takich pacjentów. Wybór optymalnej strategii terapeutycznej dla chorego z CTEPH wymaga wielodyscyplinarnej współpracy kardiologiczno-kardiochirurgiczno-anestezjologicznej, ale też wsparcia pneumonologów, radiologów i hematologów.
Endarterektomia płucna i wyniki leczenia operacyjnego
Udowodnioną skuteczność w leczeniu CTEPH ma (tromb)endarterektomia płucna, jeden z najtrudniejszych zabiegów kardiochirurgicznych. Polega ona na usunięciu materiału zatorowego z tętnic płucnych oraz wypreparowaniu i usunięciu zmienionej, zwłókniałej błony wewnętrznej tętnic płucnych do poziomu przynajmniej naczyń segmentalnych. Usunięcie samego materiału zatorowego nie wystarcza do obniżenia naczyniowego oporu płucnego generowanego także przez usztywnione, zmienione tętnice płucne bez zakrzepów.
Opisana przez Jamiesona i wsp. procedura PEA opiera się o 4 zasady [17]. Endarterektomia musi być obustronna, więc przeprowadza się ją z dojścia przez sternotomię. Kluczowa jest identyfikacja właściwej płaszczyzny dyssekcji w każdej tętnicy segmentalnej i subsegmentalnej. Bardzo istotna jest również optymalna wizualizacja, aby bezpiecznie i kompletnie oczyścić jak najbardziej dystalne naczynia. Zabieg przeprowadza się w głębokiej hipotermii 19-20ºC, z zatrzymaniem krążenia, zwykle ograniczonym do 20 minut. PEA rozpoczyna się od okrężnego odseparowywania przydanki od błony wewnętrznej. Materiał jest kruchy i kardiochirurg musi bardzo ostrożnie posuwać się w głąb naczynia, aby nie przerwać ciągłości ściany ani błony wewnętrznej aż do dotarcia do rzeczywistego materiału zatorowego. Następnie kontynuuje zabieg tak, aby nie rozerwać zorganizowanej zwłókniałej skrzepliny i dokończyć endarterektomię w jak najbardziej dystalnym naczyniu. Kiedy zabieg jest wykonany po obu stronach, przywraca się krążenie i ogrzewa pacjenta [17].
Jamieson zaproponował również klasyfikację materiału uzyskanego w czasie PEA. Typ I odpowiada skrzeplinom zlokalizowanym w głównych gałęziach proksymalnych i płatowych z obecnością zmian świeżych lub podostrych. Typ II to zmiany bardziej przewlekłe, zwłókniałe i zlokalizowane w gałęziach proksymalnych, ale bez świeżych skrzeplin. W typie III choroba dotyczy tylko gałęzi segmentalnych lub subsegmenatlnych tętnic płucnych. W typie IV w momencie operacji nie stwierdza się obecności przewlekłej choroby zakrzepowo-zatorowej [17].
Wynik operacji zależy przede wszystkim od prawidłowej kwalifikacji chorych, ale też od doświadczenia ośrodka, w którym wykonuje się PEA. Śmiertelność wewnątrzszpitalna wśród pacjentów, u których przeprowadzono PEA jeszcze w latach 90. XX w. oscylowała, w zależności od ośrodka, między kilkunastoma a ponad 20%. Obecnie jest ona wyraźnie mniejsza. W Europejskim Rejestrze CTEPH w grupie 386 operowanych pacjentów śmiertelność wewnątrzszpitalna w ośrodkach wykonujących <10 zabiegów rocznie wynosiła 7,4%, w ośrodkach operujących 10-50 pacjentów – 4,7%, a w centrach wykonujących >50 operacji rocznie – 3,5% [11].
Niedawno opublikowano dane z San Diego, wiodącego ośrodka na świecie, w którym przeprowadzono ponad 2700 zabiegów PEA. Z analizy 1500 przypadków z lat 1999-2010 wynika, że śmiertelność wewnątrzszpitalna została zredukowana nawet do 2,2% dla ostatnich 500 operacji. Po PEA obserwowano istotne obniżanie naczyniowego oporu płucnego i średniego ciśnienia w tętnicy płucnej średnio do 26±8,4 mm Hg, chociaż w tej grupie chorych zmiany w tętnicach płucnych zlokalizowane były bardziej dystalnie niż u pacjentów operowanych przed 2006 r. Przeżycie w analizowanej grupie wynosiło 82% po 5 latach i 75% po 10 latach obserwacji [18].
W Polsce pierwszy zabieg endarterektomii płucnej został wykonany w 1993 r. przez zespół prof. Religi i prof. Zembali. Obecnie przeprowadza się ją w dwóch ośrodkach: w Zabrzu (zespół prof. Zembali) i Warszawie (zespół prof. Biedermana). Wyniki leczenia operacyjnego obserwowane w ostatnich latach są porównywalne z rezultatami w europejskich ośrodkach referencyjnych. W ośrodku warszawskim 24-miesięczna śmiertelność wśród 130 pacjentów poddanych leczeniu operacyjnemu w latach 1995-2011 wyniosła 6,9%. W Zabrzu śmiertelność pacjentów po PEA utrzymuje się na podobnym poziomie i wynosi 8% po 24 miesiącach od zabiegu [19].
U chorych po przebytej operacji PEA przetrwałe CTEPH rozpoznaje się w 10-15% przypadków. U większości pacjentów obserwuje się natomiast istotną poprawę w zakresie parametrów hemodynamicznych ze spadkiem naczyniowego oporu płucnego i poprawą indeksu sercowego [20].
Analizując dane z ośrodków kardiochirurgicznych, widoczna jest wzrastająca liczba zabiegów skojarzonych z PEA, nie tylko korekcji wad wrodzonych serca, ale również wszczepiania pomostów aortalno-wieńcowych.
Próby stosowania w CTEPH leków dedykowanych tętniczemu nadciśnieniu płucnemu
Nie wszyscy pacjenci z CTEPH mogą zostać zakwalifikowani do operacji PEA. Z danych Europejskiego Rejestru CTEPH z lat 2007-2009 wynika, że ponad 40% nie jest poddawana operacji przede wszystkim z powodu dystalnej lokalizacji zmian zakrzepowo-zatorowych [11].