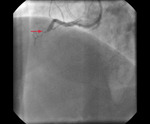
Rotablacja – stosowanie ratunkowe czy rutynowe? Na co szczególnie zwrócić uwagę?
dr n. med. Łukasz Klima1
prof. dr hab. n. med. Leszek Bryniarski2
Ani rutynowe ani ratunkowe stosowanie rotablacji nie jest optymalnym wyborem. Najlepsze jest podejście wykorzystujące przemyślaną strategię zabiegu przy wcześniejszej prawidłowej ocenie jego złożoności i trudności.
Wprowadzenie
Z powodu starzenia się populacji i większej dostępności zabiegów kardiologii inwazyjnej coraz rzadziej przezskórne interwencje wieńcowe (PCI – percutaneous coronary intervention) dotyczą prostych zmianach miażdżycowych u pacjentów bez dodatkowych obciążeń. Znacznie częściej mamy do czynienia ze skomplikowaną charakterystyką kliniczną, która rzutuje na złożoność zmian miażdżycowych. Pacjenci, u których wykonuje się obecnie PCI, są starsi, często z przewlekłą niewydolnością serca, wieloletnią cukrzycą, przewlekłą niewydolnością nerek, a także po wcześniejszych interwencjach wieńcowych, w tym po zabiegach pomostowania aortalno-wieńcowego. Wymagają oni szczególnie dobrze zaplanowanej strategii leczenia z uwzględnieniem zastosowania technik rotablacji zwapniałych zmian, ponieważ takie podejście ma udokumentowaną większą skuteczność i wykonywane przez doświadczonych operatorów jest bezpieczniejsze dla pacjenta.1
Rys historyczny
Technikę aterektomii rotacyjnej (RA – rotational atherectomy), zwanej powszechnie rotablacją, wprowadził w latach 80. ubiegłego wieku David Auth. I choć rotablacja jako strategia stand-alone, czyli leczenia przy użyciu wyłącznie tej techniki (alternatywa dla angioplastyki balonowej czy implantacji stentu), nie przyniosła korzyści, to w erze powszechnego stosowania stentów uwalniających lek (DES – drug-eluting stent) istotnie zmniejsza ryzyko restenozy w stencie2 oraz dyssekcji i zamknięcia naczynia po przygotowaniu zwapniałej zmiany do implantacji stentu. Obecnie nie dążymy do uzyskania optymalnego efektu za pomocą samej rotablacji, jej celem jest przygotowanie zmiany i umożliwienie optymalnej implantacji stentu – tzw. strategia modyfikacji blaszki miażdżycowej (plaque modification).
Budowa
Urządzenie do rotablacji jest produkowane przez firmę Boston Scientific (Marlborough, Massachusetts, Stany Zjednoczone). Podstawowym elementem jest metalowy prowadnik (średnicy 0,009 cala dystalnie i w końcówce 0,014 cala) występujący w dwóch wersjach (miękki – floppy i twardszy – extra support), po którym wprowadzone jest eliptyczne wiertło o średnicy 1,25-2,0 mm pokryte mikrokryształkami diamentu (tzw. bor). Stałym elementem układu jest butla ze sprężonym powietrzem lub azotem, która napędza turbinę i wprowadza wiertło w ruch rotacyjny, najczęściej o prędkości 130 000-180 000 obrotów na minutę. Parametry pracy urządzenia wybiera się na konsoli centralnej, operator zaś uruchamia napęd specjalnym pedałem i przy pomocy urządzenia zwanego advancerem przesuwa wiertło ruchem posuwisto-zwrotnym, najlepiej dziobiącym (pecking motion). Twarda, uwapniona blaszka miażdżycowa zostaje starta przez wirujące wiertło, podczas gdy zdrowa tkanka jest elastyczna, ugina się i pozostaje w zasadzie nietknięta. Blaszka miażdżycowa jest rozdrobniona do cząstek <10 µm, które swobodnie przepływają przez mikrokrążenie.
Do 2007 roku na rynku było dostępne jedynie urządzenie firmy Boston Scientific. W 2007 roku firma Cardiovascular System wprowadziła na rynek urządzenie do tzw. orbitalnej aterektomii (OAS – orbital atherectomy system), które ma podobną zasadę działania, a napęd może być pneumatyczny lub elektryczny.3,4 W najbliższym czasie firma Boston Scientific wprowadzi na rynek modyfikację dotychczasowego systemu, wycofując pedał sterujący prędkością; przycisk z tą funkcją będzie zintegrowany z advancerem, co znacznie uprości obsługę systemu.
Wskazania
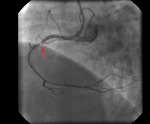
Rycina 2. Obraz naczynia po udrożnieniu i inflacjach balonowych. Brak poszerzenia światła w miejscu okluzji (strzałka) – nie udało się w tym miejscu rozprężyć żadnego cewnika balonowego ze względu na masywne zwapnienia
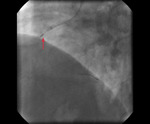
Rycina 3. Po wymianie prowadnika na prowadnik do rotablacji – zabieg rotablacji zwapniałej zmiany (plaque modification), strzałka wskazuje pozycję wiertła
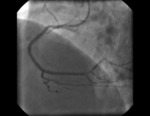
Rycina 4. Efekt końcowy zabiegu po implantacji stentu DES – uzyskano pełne rozprężenie stentu w całym naczyniu, również w miejscu, gdzie przed zabiegiem rotablacji nie było możliwe rozprężenie balonika
Najważniejszym wskazaniem do rotablacji jest obecność masywnych zwapnień w blaszce miażdżycowej. Ogólną zasadą, jaką kierują się operatorzy, kwalifikując pacjenta do RA, jest brak możliwości wprowadzenia najmniejszego balonika i/lub wykonania skutecznej predylatacji przy użyciu wysokich ciśnień. Naszym zdaniem zakwalifikowanie pacjenta do zabiegu aterektomii rotacyjnej nawet bez wcześniejszej próby angioplastyki balonowej jest dopuszczalne, jeśli uprzednio potwierdzono obecność dużego stopnia kalcyfikacji. Właściwa ocena stopnia nasilenia zwapnień jest więc kluczowa dla odpowiedniej kwalifikacji pacjenta i chociaż największą czułość, a także głębokość penetracji będą tutaj miały ultrasonografia wewnątrzwieńcowa (IVUS – intravascular ultrasound) czy optyczna tomografia koherentna (OCT – optical coherence tomography),5,6 to trudno oczekiwać, że w sytuacji gdy nie udaje się przeprowadzić przez zmianę cewnika balonowego o najmniejszym profilu przejścia, uda się przeprowadzić sondę IVUS czy wykonać OCT. Pozostaje więc ocena angiograficzna, która – choć daleka od doskonałości przy stwierdzeniu obecności zwapnień z obu stron naczynia – pozwoli na rozpoznanie kalcyfikacji dużego stopnia. Istnieją różne klasyfikacje zwapnień i rozsądne wydaje się podejście zaproponowane przez Tomeya i wsp.,7 w którym do RA kwalifikuje się chorych jedynie ze zwapnieniami o dużym nasileniu. Takiego pacjenta można zakwalifikować do zabiegu RA ad hoc, niwelując ryzyko dyssekcji, okluzji czy perforacji naczynia (ryc. 1-4). Poza wymienionymi klasycznymi wskazaniami do zabiegu są jeszcze wskazania dodatkowe i niestandardowe, które zostały wymienione w stanowisku grupy ekspertów8 i zebrane w tabeli 1.