VMS Interna 2026 | BEZPŁATNY kongres online już 19-21 maja! 6 sesji - Ponad 20 wykładów - Sesje Q&A | Zapisz się >
Przypadek kliniczny
Martwica skóry wywołana warfaryną
Catherine R. Mungalsingh, specialisation year 1 Jamie Bomford, foundation year 2 Jeremy Nayagam, foundation year 1 Mirella Masiello, foundation year 1
Martwica skóry wywołana warfaryną jest rzadkim, ale poważnym powikłaniem związanym z leczeniem tym powszechnie stosowanym lekiem. W artykule omówiono przypadek pacjenta z rozległą martwicą skóry, która wystąpiła z powodu zbyt długiego stosowania warfaryny i opóźnienia rozpoznania. Krótki opis tego powikłania zwraca uwagę na jego charakterystyczne cechy i czynniki ryzyka.
OPIS PRZYPADKU
82-letnia niedożywiona kobieta została skierowana na szpitalny oddział ratunkowy z powodu rozległej, bolesnej wysypki. Objawy nasiliły się pomimo stosowanego przez 2 tygodnie leczenia z powodu rozpoznania półpaśca. Przed miesiącem pacjentka na krótko odstawiła warfarynę w związku z operacją rzepki. Leczenie warfaryną zostało włączone przed rokiem ze względu na zatorowość płucną, która wystąpiła po zabiegu operacyjnym. W badaniu przedmiotowym stwierdzono rozległe, tkliwe i cuchnące krwotoczne zmiany w postaci rumieniowych blaszek o fiołkowym odcieniu. Uwagę zwracały strupy z martwicą centralną i pęcherze, a zmiany zlokalizowane były w obrębie twarzy, piersi, tułowia i kończyn (ryc. 1).
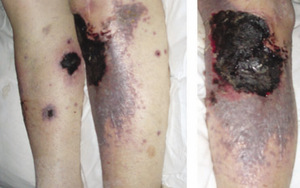
Rycina 1. Mnogie, tkliwe i cuchnące zmiany martwicze zostały stwierdzone w obrębie tułowia, kończyn i twarzy pacjentki.
Z powodu podejrzenia martwicy skóry wywołanej warfaryną (WISN – warfarin-induced skin necrosis) przerwano podawanie warfaryny, zastosowano witaminę K i heparynę drobnocząsteczkową. Zastosowano antybiotyki o szerokim spektrum działania, żywienie dojelitowe i 3-dniowy kurs metyloprednizolonu, ponieważ nie można było wykluczyć zapalenia naczyń jako przyczyny zmian skórnych. W pobranych wycinkach zmian skórnych stwierdzono zmiany typowe dla WISN: skrzepliny w naczyniach, rozsiane ogniska martwicy i świeże krwotoki. Nie wykazano cech charakterystycznych dla zapalenia naczyń. Rumieniowe blaszki stopniowo zostały zastąpione zmianami martwiczymi. Pomimo przedłużonej antybiotykoterapii dożylnej pacjentka zmarła z powodu ciężkiej sepsy i niewydolności wielonarządowej.
Martwica skóry wywołana warfaryną występuje typowo u otyłych kobiet w średnim wieku. Zmiany obserwuje się najczęściej w obrębie części ciała ze zwiększoną ilością podskórnej tkanki tłuszczowej: na klatce piersiowej, pośladkach, udach i brzuchu.1-4 Zazwyczaj pojawiają się 3-6 dni po rozpoczęciu leczenia warfaryną,1,2,4-8 ale opisywane są również przypadki wystąpienia zmian nawet po 3 latach leczenia.5,7 W obrębie zajętej skóry dochodzi do zawałów, a następnie do powstania martwiczych strupów i ścieńczenia.1-4,8 Wywiad kliniczny, rozmieszczenie zmian skórnych i wynik badania histologicznego pomagają odróżnić WISN od innych stanów, takich jak: martwica skóry wywołana heparyną, zespół rozsianego wykrzepiania wewnątrznaczyniowego (DIC – disseminated intravascular coagulation) i martwicze zapalenie powięzi.1
Do mechanizmów etiologicznych WISN należą: niedobór białka C, nadwrażliwość i bezpośrednie toksyczne działanie warfaryny.1,2,8 W badaniu histologicznym typowo stwierdza się rozsianą mikrozatorowość w obrębie naczyń włosowatych skóry i tkanki podskórnej, żyłek i żył głębokich, ponadto uszkodzenie śródbłonka prowadzące do martwicy niedokrwiennej skóry oraz wynaczynienie krwinek czerwonych.1 Brak cech zapalenia okołonaczyniowego i zakrzepicy tętniczek jest cechą różnicującą WISN z innymi waskulopatiami.1,3
Postępowanie jest głównie objawowe. Leczenie polega na odstawieniu warfaryny i odwróceniu jej wpływu na białko C za pomocą podaży witaminy K i preparatów świeżo mrożonego osocza.1-9 Podanie heparyny zapobiega powstawaniu dalszych zmian zakrzepowych w żyłkach pozawłośniczkowych,4 korzystne działanie ma również podanie koncentratu białka C, ale jego zastosowanie jest ograniczone wysokimi kosztami. Pacjenci mogą wymagać opracowania chirurgicznego ran, a w rzadkich przypadkach przeszczepienia skóry lub nawet amputacji.2 Do głównych przyczyn zgonów należą: martwica tkanek głębokich, sepsa wtórna do zakażenia rany i niewydolność wielonarządowa.11
Wnioski
Warfarynę przyjmuje 1% populacji mieszkańców Wielkiej Brytanii.11,12 WISN jest rzadkim, ale istotnym powikłaniem wymagającym dużej podejrzliwości klinicznej i wczesnego rozpoznania. Wdrożenie leczenia w odpowiednim czasie może zapobiec rozległemu zajęciu skóry i zmniejsza ryzyko wystąpienia ciężkiego zakażenia bakteryjnego. Opisany przypadek pokazuje, jak duże znaczenie ma ustalenie okresu leczenia na etapie włączenia terapii przeciwzakrzepowej, a następnie weryfikacja wskazań do jej kontynuacji u każdego pacjenta.
Komentarz
prof. dr hab. med. Krystyna Zawilska
Oddział Hematologii i Chorób Wewnętrznych, Wielospecjalistyczny Szpital Miejski im. J. Strusia w Poznaniu
Martwica skóry należy do rzadko występujących powikłań stosowania warfaryny i innych leków z grupy antagonistów witaminy K (VKA) – odnotowuje się 1-10 przypadków/10 tys. leczonych.1,2 Szczególnie narażeni na to powikłanie są pacjenci z niedoborem białka C lub białka S, u których leczenie rozpoczęto od dużej dawki warfaryny lub acenokumarolu. Efekt przeciwzakrzepowy VKA zależy od związanej z ich okresem półtrwania szybkości wymiany nieaktywnych czynników krzepnięcia (protrombina, czynnik VII, IX i X) na ich aktywne formy karboksylowane. Najkrótszy okres półtrwania (T½ – 7 godzin) ma czynnik VII i zależny również od zachodzącej z udziałem witaminy K karboksylacji naturalny antykoagulant białko C, dlatego w początkowym okresie stosowania VKA może dojść do nadkrzepliwości. Najważniejsze dla działania VKA jest zahamowanie działania czynnika X i protrombiny. Z uwagi na długi czas półtrwania (40 godzin) do zmniejszenia aktywności protrombiny i rozwinięcia pełnego działania przeciwzakrzepowgo VKA dochodzi dopiero po 4-5 dniach leczenia. W związku z tym w początkowym okresie stosowania leku, mimo osiągnięcia terapeutycznej wartości wskaźnika protrombinowego (INR >2,0) uwarunkowanej przez aktywność czynnika VII, efekt przeciwzakrzepowy VKA jest niepełny i może dojść do zachwiania równowagi pomiędzy przeciwzakrzepowym działaniem VKA a „paradoksalnym” działaniem prozakrzepowym wynikającym z wczesnego zahamowania aktywności białka C i białka S. Skutkiem może być tworzenie się skrzeplin i mikrozatorów w naczyniach żylnych skóry i tkanki podskórnej, prowadzące do typowego obrazu martwicy skóry. Powikłanie to rozwija się częściej u osób z wrodzonym lub nabytym niedoborem naturalnych antykoagulantów – białka C i S. Opisywano sporadyczne przypadki martwicy skóry wywołanej warfaryną także u pacjentów z trombofilią związaną z niedoborem antytrombiny, polimorfizmem czynnika V Leiden lub zespołem antyfosfolipidowym.3,4
Zmiany skórne mają początkowo postać bolesnego zaczerwienienia, które w krótkim czasie zmienia barwę na ciemną, a następnie przyjmuje postać odgraniczonych ognisk martwicy. Konieczne może być chirurgiczne usunięcie uszkodzonych tkanek, a nasilenie martwicy jest niekiedy na tyle duże, że stanowi zagrożenie życia. Nie wyjaśniono dotąd, dlaczego zmiany martwicze tworzą się głównie u kobiet i obejmują okolice, gdzie znajduje się gruba warstwa tkanki tłuszczowej – najczęściej piersi, pośladki, uda i brzuch. Istnieje hipoteza wiążąca tę lokalizację z gorszym unaczynieniem tkanki tłuszczowej. W opisanym przypadku zmiany martwicze obejmowały również twarz, co zdarza się rzadko.
W swojej praktyce lekarskiej spotkałam 62-letnią pacjentkę, u której wystąpiła rozległa martwica skóry w obrębie piersi i podbrzusza w przebiegu stosowania acenokumarolu z powodu nawracającej zakrzepicy żył głębokich i żył powierzchownych. Przeprowadzone badania wykazały obniżenie stężenia i aktywności białka C (odpowiednio 59,9% i 63,3% wartości prawidłowej). Aktywność antytrombiny oraz stężenie całkowitego i wolnego białka S były w normie.5,6 W początkowym okresie leczenia zaprzestaliśmy stosowania acenokumarolu, włączyliśmy heparynę w dawkach terapeutycznych i podawaliśmy świeżo mrożone osocze w celu uzupełnienia białka C, co zahamowało progresję zmian skórnych. Ze względu na konieczność stosowania u tej pacjentki leczenia przeciwzakrzepowego na stałe włączyliśmy ponownie acenokumarol w dawce 2 mg/24 h pod osłoną heparyny i koncentratu białka C. Po 6 dniach INR wzrósł do >2,0 i można było zaprzestać stosowania heparyny i koncentratu białka C. Zmiany martwicze skóry i tkanki podskórnej po kilku tygodniach wygoiły się.
W zapobieganiu martwicy skóry wywołanej warfaryną istotne znaczenie ma zebranie szczegółowego wywiadu w celu wykluczenia trombofilii. Obecność trombofilii, a zwłaszcza niedobór białka C lub białka S, wskazuje bowiem na konieczność rozpoczęcia leczenia VKA od małych dawek (5 mg warfaryny lub 2 mg acenokumarolu), z jednoczesnym stosowaniem heparyny drobnocząsteczkowej lub niefrakcjonowanej w dawce terapeutycznej do czasu uzyskania INR >2,0 utrzymującego się przez ≥2 dni.
Bardzo ważne jest wczesne rozpoznanie tego powikłania, natychmiastowe odstawienie warfaryny lub acenokumarolu i „zneutralizowanie” działania tych leków (uzyskanie INR 1,0-1,2) poprzez zastosowanie koncentratu czynników zespołu protrombiny lub świeżo mrożonego osocza. Należy również włączyć lek przeciwzakrzepowy o innym mechanizmie działania. Obecnie oprócz heparyn można stosować fondaparynuks (inhibitor czynnika Xa podawany podskórnie), a także nowy doustny lek przeciwzakrzepowy – dabigatran (bezpośredni inhibitor trombiny). W 2012 r. opublikowano opis przypadku 21-letniej kobiety z ciężkim niedoborem białka C (<1% wartości prawidłowej) i powtarzającymi się od 11. r.ż. epizodami żylnej choroby zakrzepowo-zatorowej, u której w przebiegu przewlekłego leczenia warfaryną dochodziło do nawrotowej martwicy skóry w obrębie ud.7 Po zastąpieniu warfaryny dabigatranem w dawce 2 × 150 mg/24 h zmiany martwicze uległy wygojeniu, leczenie było dobrze tolerowane, a w kontrolnych badaniach po 2 i 6 miesiącach nie stwierdzono ani zmian zakrzepowych, ani martwicy skóry. Istnieje duże prawdopodobieństwo, że dobre wyniki będzie można również uzyskać, stosując doustnie bezpośredni inhibitor czynnika Xa – rywaroksaban, ale nie ma jak dotąd doniesień na ten temat. Wydaje się jednak, że nowe doustne leki (dabigatran, rywaroksaban i apiksaban), których działanie przeciwzakrzepowe jest przewidywalne i nie wymaga laboratoryjnego monitorowania, staną się lekami z wyboru w leczeniu powikłań zakrzepowych u chorych z trombofilią, gdyż cechują się szybkim początkiem działania i nie wywierają wpływu na aktywność białka C i białka S.
Piśmiennictwo:
1. Chan YC, Valenti D, Mansfield AO, et al. Warfarin induced skin necrosis. Br J Surg 2000;87:266-72.
2. Ward CT, Chavalitanonda N. Atypical warfarin –induced skin necrosis. Pharmacotherapy 2006;26:1175-9.
3. McGehee WG, Klotz TA, Epstein DJ, et al. Coumarin necrosis associated with hereditary protein C deficiency. Ann Intern Med 1984;101:59-60.
4. Moreb J, Kitchens CS. Acquired functional protein S deficiency, cerebral venous thrombosis, and coumarin skin necrosis in association with antiphospholipid syndrome: report of two cases. Am J Med 1989;87:207-10.
5. Lewandowski K, Zawilska K. Nowe możliwości leczenia martwicy skóry w przebiegu niedoboru białka C. Pol Arch Med Wewn 1993;89:424-30.
6. Lewandowski K, Zawilska K. Protein C concentrate in the treatment of warfarin-induced skin necrosis in the protein C deficiency. Thromb Haemost 1994;71:395.
7. Hermans C, Eeckhoudt S, Lambert C. Dabigatran etexilate (Pradaxa) for preventing warfarin-induced skin necrosis in a patient with severe protein C deficiency. Thromb Haemost 2012;107:1189-91.