Toksoplazmoza
Toxoplasma gondii to rozpowszechniony na całym świecie pierwotniak bezwzględnie wewnątrzkomórkowy. Jego ostatecznymi żywicielami są zwierzęta z rodziny kotowatych, a do zakażenia ludzi dochodzi na drodze spożycia pokarmów skażonych odchodami kotów lub niedogotowanego mięsa zakażonych zwierząt.
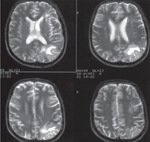
Rozwój odpowiedzi komórkowej po ostrym zakażeniu T. gondii prowadzi do kontroli zakażenia, ale nie całkowitej eradykacji patogenu. Następnie choroba przechodzi w fazę przewlekłą lub latentną i charakteryzuje się przetrwałą obecnością mikroorganizmów w tkankach zakażonej osoby (głównie w tkance mózgowej, mięśniach szkieletowych i w sercu). Tak więc T. gondii stanowi jedną z najczęstszych przyczyn przewlekłego zakażenia patogenem wewnątrzkomórkowym u ludzi. Osoba z przewlekłą postacią zakażenia, u której doszło do upośledzenia odporności komórkowej, jest narażona na reaktywację infekcji. W takim przypadku toksoplazmoza ujawnia się głównie jako toksoplazmowe zapalenie mózgu. Choroba ta jest istotną przyczyną ogniskowych zmian w mózgu u pacjentów zakażonych wirusem HIV (ryc. 3).11
Obraz kliniczny
Cechą charakterystyczną toksoplazmowego zapalenia mózgu jest podostry początek choroby z ogniskowymi zaburzeniami neurologicznymi, którym towarzyszą bóle głowy, zaburzenia świadomości i gorączka. Do najczęstszych objawów ogniskowych zaburzeń neurologicznych należą niedowład i zaburzenia mowy. U pacjentów pojawiają się także drgawki, zaburzenia czynności nerwów czaszkowych, ubytki w polu widzenia, zaburzenia czucia, zaburzenia móżdżkowe, podrażnienia opon mózgowych, zaburzenia chodu oraz objawy neuropsychiatryczne. Toksoplazmoza rzadko przebiega w postaci gwałtownie postępującego rozlanego zapalenia mózgu prowadzącego do śmierci. Rozpoznanie rozlanej formy zapalenia mózgu należy rozważyć u pacjentów z przeciwciałami w klasie IgG skierowanymi przeciwko T. gondii oraz ze stężeniem CD4 <100 komórek/µl, u których występuje choroba neurologiczna o nieznanej etiologii.
U pacjentów zakażonych wirusem HIV może rozwinąć się toksoplazmoza o pozamózgowej lokalizacji z towarzyszącym zapaleniem mózgu lub bez niego. Do najczęstszych postaci pozamózgowych należą toksoplazmoza oczna i płucna. U pacjentów z zapaleniem siatkówki i naczyniówki występują zaburzenia ostrości widzenia, ubytki w polu widzenia, ból lub światłowstręt. Badanie okulistyczne ujawnia wieloogniskowe zmiany w obu gałkach ocznych, bardziej zlewne, pogrubiałe i zmętniałe niż w zaburzeniach wywołanych przez cytomegalowirus. Vitritis może występować łącznie z zapaleniem błony naczyniowej przedniego odcinka oka. T. gondii znacznie rzadziej wywołuje zapalenie siatkówki i naczyniówki u pacjentów zakażonych wirusem HIV niż cytomegalowirus.
Kliniczne objawy płucnej toksoplazmozy mogą być trudne do odróżnienia od pneumocystozowego zapalenia płuc.12 U pacjentów zakażonych wirusem HIV opisywano cechujący się wysoką umieralnością zespół rozsianej toksoplazmozy, który obejmuje: gorączkę, wstrząs septyczny z obniżonym ciśnieniem tętniczym krwi, rozsianym wykrzepianiem wewnątrznaczyniowym, podwyższonym stężeniem dehydrogenazy mleczanowej oraz z obecnością nacieków płucnych.
Diagnostyka
Zakażenie T. gondii rozpoznaje się na podstawie badań serologicznych. Toksoplazmozę, chorobę wywoływaną przez pasożyty, można rozpoznać, wykazując obecność tachyzoitów w bioptacie tkanki lub preparatach cytologicznych z płynów ustrojowych, na podstawie izolacji T. gondii z płynów ustrojowych bądź z krwi, a także poprzez amplifikację DNA patogenu z płynów ustrojowych lub krwi przy zastosowaniu łańcuchowej reakcji polimerazy.
Postępowanie
Odkrycie pirymetaminy (inhibitor reduktazy dihydrofolianowej) stanowiło istotny postęp w leczeniu toksoplazmozy. Stosowanie tego leku w skojarzeniu z sulfadiazyną (inhibitorem syntazy dihydrofolianowej) jest standardem leczenia toksoplazmowego zapalenia mózgu. Pacjenci leczeni pirymetaminą powinni dodatkowo otrzymywać kwas foliowy, by zapobiegać wystąpieniu hematologicznym działaniom niepożądanym.
Pirymetamina w skojarzeniu z klindamycyną w porównaniu z pirymetaminą i sulfadiazyną wykazuje podobną skuteczność w leczeniu ostrej fazy choroby,13 jednak w przypadku tego pierwszego połączenia leków do częstych działań niepożądanych należą wysypka i biegunka. W prospektywnym badaniu przeprowadzonym z randomizacją wykazano, że w terapii toksoplazmowego zapalenia mózgu ko-trymoksazol w porównaniu z pirymetaminą w skojarzeniu z sulfadiazyną są tak samo skuteczne.14
Istnieją ograniczone dane wskazujące, że chorzy na AIDS z pozamózgową postacią toksoplazmozy odpowiadają na leczenie pirymetaminą zarówno w skojarzeniu z sulfadiazyną, jak i klindamycyną. Współczynnik umieralności w grupie pacjentów z toksoplazmozą płucną lub rozsianą może być wyższy niż w grupie chorych z samym toksoplazmowym zapaleniem mózgu. Pacjenci chorujący na toksoplazmozę w przebiegu AIDS powinni być poddawani leczeniu podtrzymującemu po zakończeniu terapii ostrej fazy choroby. Typowe leczenie podtrzymujące polega na podawaniu leków stosowanych w terapii pierwotnej, lecz w zredukowanych dawkach.
Kryptokokoza
Cryptococcus neoformans jest otoczkowym grzybem drożdżopodobnym o okrągłym lub owalnym kształcie, wielkości 4-6 µm, mającym otoczkę polisacharydową, która w warunkach hodowli laboratoryjnej osiąga wymiary od 1 do >30 µm. Grzyb w swoim środowisku naturalnym jest mniejszy i cechuje się słabszą otoczką.
Kryptokokoza stanowi najczęstszą przyczynę zagrażającego życiu zapalenia opon mózgowo-rdzeniowych u chorych na AIDS. Na początku epidemii zakażenie kryptokokowe stwierdzano u 5-8% pacjentów z AIDS. Częstość występowania kryptokokozy, podobnie jak innych zakażeń oportunistycznych, zmniejszyła się od czasu wynalezienia skutecznego leczenia antyretrowirusowego,15 chociaż do redukcji liczby nowych przypadków mogło dojść jeszcze przed wprowadzeniem tej terapii. Inne dane sugerują, że spadek zapadalności wiąże się z rozpowszechnieniem leczenia azolowymi lekami przeciwgrzybiczymi.16
Obraz kliniczny
Kryptokokoza u chorych na AIDS najczęściej przyjmuje postać zapalenia opon mózgowo-rdzeniowych i mózgu. Zazwyczaj obserwuje się jej podostry rozwój przebiegający z bólem głowy i gorączką, rzadziej z zaburzeniami świadomości. Chorobie mogą także towarzyszyć objawy ostrego lub przewlekłego zapalenia opon mózgowo-rdzeniowych. Do najczęściej występujących objawów ocznych u pacjentów z kryptokokowym zajęciem ośrodkowego układu nerwowego należą porażenie nerwów czaszkowych i obrzęk tarczy nerwu wzrokowego. Powikłaniami zakażenia ośrodkowego układu nerwowego są wodogłowie, deficyty sensomotoryczne, zaburzenia móżdżkowe, drgawki oraz otępienie. Rzadko są opisywane uszkodzenia ogniskowe. Bywa, że w tomografii komputerowej lub rezonansie magnetycznym widoczne są wewnątrzmózgowe ziarniniaki wskazujące na cryptococcoma.
U ok. 40% pacjentów chorych na kryptokokowe zapalenie opon mózgowo-rdzeniowych związane z AIDS w badaniu płynu mózgowo-rdzeniowego wykrywa się nieprawidłowości, takie jak pleocytoza, obniżone stężenie glukozy i podwyższone stężenie białka. Niskie stężenie leukocytów w płynie mózgowo-rdzeniowym (<20 leukocytów/μl) wiąże się z niekorzystnym rokowaniem.