Dziesięć głównych prawd, które zdaniem nefrologów powinien znać każdy lekarz podstawowej opieki zdrowotnej
Neil M. Paige, MD, MSHS1
Glenn T. Nagami, MD2
W SKRÓCIE
Choroby nerek są problemem, z którym lekarz podstawowej opieki zdrowotnej ma do czynienia na co dzień. Do najczęstszych należą: nerkopochodne nadciśnienie tętnicze, białkomocz, kamica nerkowa oraz przewlekła choroba nerek. Mimo że choroby te są powszechne, wielu lekarzy nie ma wystarczającej wiedzy potrzebnej do ich rozpoznawania i rozpoczynania leczenia. Tymczasem wczesne rozpoznanie i podjęcie odpowiednich działań mają duże znaczenie dla zwolnienia postępu przewlekłej choroby nerek i zapobiegania jej powikłaniom. Przedstawione w artykule najważniejsze zalecenia oparte na dowodach naukowych pomogą lekarzom podstawowej opieki zdrowotnej ominąć najczęstsze pułapki spotykane podczas rozpoznawania i leczenia chorób nerek, a także ułatwią im podjęcie decyzji o skierowaniu chorego do specjalisty.
Wprowadzenie
Przewlekła choroba nerek (PChN) jest powszechną patologią powodującą znaczącą chorobowość i umieralność. W jej przebiegu może dojść do niewydolności nerek, chorób układu krążenia i przedwczesnego zgonu. Z inicjatywy międzynarodowej grupy Kidney Disease: Improving Global Outcome (KDIGO) zwrócono uwagę na ważne cele, jakimi są nauczenie rozpoznawania PChN w jej najwcześniejszym stadium oraz wskazanie, jakie środki należy podjąć, by zapobiec jej progresji i powikłaniom.1 Dodatkową umiejętnością, którą powinien posiąść lekarz podstawowej opieki zdrowotnej, jest właściwa diagnostyka i postępowanie w przypadku opornego na leczenie nadciśnienia tętniczego oraz kamicy nerkowej. Przedstawione w artykule najważniejsze zalecenia, oparte na dowodach naukowych, ułatwią lekarzom podstawowej opieki zdrowotnej zrozumienie tych zagadnień i pozwolą ominąć częste pułapki, na które mogą się natknąć podczas rozpoznawania i leczenia tych zaburzeń. Pomogą też zdecydować o skierowaniu chorego do specjalisty.
1. Stężenie kreatyniny w surowicy utrzymujące się w granicach normy może nie być prawidłowe
Przyjęte przez poszczególne laboratoria normy stężenia kreatyniny w surowicy różnią się między sobą. Czasem u chorego, którego stężenie kreatyniny w surowicy mieści się w granicach normy, czynność nerek jest znacznie upośledzona. Na przykład u 66-letniego mężczyzny, u którego stężenie kreatyniny w surowicy wynosi 1,4 mg/dl (aby wyrazić je w μmol/l, należy pomnożyć tę wartość przez 88,4), oszacowany wskaźnik przesączania kłębuszkowego (GFR – glomerular filtration rate) osiąga wartość 54 ml/min/1,73 m2. Zatem stężenie kreatyniny, postrzegane jako prawidłowe, odpowiada u niego przewlekłej chorobie nerek 3. stopnia.1 Podobnie tempo zwiększenia stężenia kreatyniny w surowicy lub skłonność do jego zwiększania się mogą przemawiać za występowaniem PChN. Na przykład u 66-letniego mężczyzny ze stężeniem kreatyniny w surowicy 0,8 mg/dl i oszacowanym GFR 103 ml/min/1,73 m2 zmniejszenie tej wartości do <64 ml/min/1,73 m2 powinno sprawić, że stężenie kreatyniny w surowicy osiągnie wartość 1,2 mg/dl. Odpowiada to zmniejszeniu GFR o 40%. GFR można oszacować, tylko opierając się na stabilnych stężeniach kreatyniny. Jeśli stężenia te zmieniają się, nie można ich wykorzystywać w celu dokładnego oszacowania GFR. Gwałtowne zwiększenie się stężenia kreatyniny z 0,8 do 1,2 mg/dl w ciągu 8h u chorego z ostrą niewydolnością nerek może odzwierciedlać zbliżanie się GFR do zera. Interpretacja stężenia kreatyniny w surowicy zależy również od masy mięśniowej, wieku, płci, wzrostu, ma na nią też wpływ amputacja kończyny. U chorego po amputacji może występować zaawansowana PChN mimo prawidłowego stężenia kreatyniny w surowicy. Nie oceniano dotąd wiarygodności wzorów powszechnie stosowanych do szacowania GFR, takich jak wzór z badania Modification of Diet in Renal Disease (dostępnych na stronie www.mdrd.com), u osób z prawidłowym GFR i w rzeczywistości narzędzia te mogą zaniżać aktualne wartości GFR u osób zdrowych.2 Należy więc uświadomić sobie, że rozpoznanie PChN jest bardzo ważne, gdyż umożliwia wykrycie i leczenie odwracalnych przyczyn choroby nerek, zwolnienie jej progresji i zapobieganie powikłaniom, a także wyłonienie chorych mogących wymagać dializacji lub przeszczepienia nerki.1
2. Niektóre leki fałszywie zwiększają stężenie kreatyniny w surowicy
Niejednokrotnie zdarza się, że zwiększenie stężenia kreatyniny w surowicy nie ma odzwierciedlenia w zmianach aktualnej wartości GFR. Dwoma powszechnie stosowanymi lekami zmniejszającymi wydalanie kreatyniny są połączenia trimetoprimu z sulfametoksazolem (kotrimoksazol) oraz antagonista receptorów H2 – cymetydyna. Ich stosowanie może powodować ograniczone i odwracalne zwiększenie stężenia kreatyniny w surowicy o 0,4-0,5 mg/dl (w zależności od wyjściowego). Podobne, choć słabsze działanie mają famotydyna i ranitydyna. Cefoksytyna [antybiotyk z grupy cefamycyn, niedostępny w Polsce – przyp. red.] pozornie zwiększa stężenie kreatyniny w surowicy, zaburzając wyniki próby kolorymetrycznej stosowanej w celu oznaczenia stężenia.3 W obu przypadkach stężenie azotu mocznikowego we krwi (BUN – blood urea nitrogen) zwykle się nie zmienia. Zwiększenie stężenia kreatyniny świadczy zatem o rzeczywistym zmniejszeniu GFR tylko wówczas, gdy współistnieje ze zwiększonym stężeniem BUN.
3. U chorych ze zmniejszonym GFR lub białkomoczem należy ustalić przyczynę tych zmian. Po wykryciu białkomoczu w badaniu moczu za pomocą testu paskowego należy oznaczyć stosunek wydalanego białka do kreatyniny w próbce moczu
Przyjmuje się, że przewlekła choroba nerek to zaburzenia czynności tego narządu trwające ponad 3 miesiące. Może ona występować u osób z prawidłowym GFR, jeśli utrzymują się białkomocz lub krwiomocz pochodzenia nerkowego. Mimo trudności z określeniem wartości nadal jeszcze prawidłowej GFR większość specjalistów zgadza się, że utrzymywanie się GFR <60 ml/min/1,73 m2 może przemawiać za przewlekłą chorobą nerek. Białkomocz wykrywany początkowo podczas badania moczu za pomocą testu paskowego odzwierciedla stężenie albumin w moczu. Ponieważ na wyniki półilościowych oznaczeń za pomocą testu paskowego może wpływać zmienność przepływu i stężenia moczu, konieczne jest przeprowadzenie ilościowego badania białkomoczu.
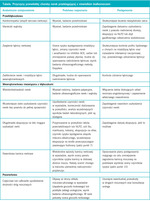
Preferowaną metodą ilościowej oceny wydzielania białka z moczem jest oznaczenie stosunku białka do kreatyniny w próbce moczu, jest to bowiem badanie dokładne i wygodniejsze niż ocena moczu z dobowej zbiórki.4-7 U osób obciążonych ryzykiem wystąpienia białkomoczu (np. chorych na cukrzycę) obliczenie stosunku albumin do kreatyniny w próbce moczu ułatwia wykrycie mikroalbuminurii, a przez to ustalenie dalszego sposobu leczenia. Chorzy na cukrzycę, u których pojawia się mikroalbuminuria, są obciążeni większym ryzykiem rozwoju nefropatii cukrzycowej. Stosunek białka do kreatyniny w moczu ≥1 zwiększa zagrożenie progresją PChN. Zawsze w takim przypadku należy poszukiwać przyczyny zmian w kłębuszkach nerkowych, np. cukrzycy, kolagenowych chorób naczyń (układowego tocznia rumieniowatego), nowotworu złośliwego (np. szpiczaka mnogiego), zakażeń (np. HIV, krętkiem kiły, wirusami zapalenia wątroby typu B lub C), a także w stosowaniu niektórych leków, np. niesteroidowych leków przeciwzapalnych (NLPZ).8 Choroba kłębuszków nerkowych (np. błoniaste zapalenie) może też wystąpić w przebiegu nowotworów litych, ale zwykle są one już wcześniej rozpoznane lub łatwo je wykryć za pomocą badań przesiewowych w kierunku nowotworów, odpowiednich dla wieku, czynników ryzyka oraz płci.9,10 Chorych, u których stwierdzono znaczny białkomocz lub wyraźne zmiany w osadzie moczu, zwłaszcza mogące świadczyć o upośledzeniu czynności nerek, należy kierować do nefrologa w celu dalszej oceny i leczenia. Niewielki białkomocz w przebiegu PChN (na który nie wpływają leki blokujące ukłąd reninowo-angiotensynowy ani antagoniści aldosteronu) przemawia za przyczyną pozakłębuszkową (tabela). W tabeli nie uwzględniono wszystkich przyczyn, ukazuje ona jednak zakres pojęć przybliżających rozpoznanie wielu przyczyn pozakłębuszkowej PChN. Długotrwałe upośledzenie czynności nerek i niewielki białkomocz mogą powstać z przyczyn przednerkowych, nerkowych i pozanerkowych. W ocenie takich chorych kluczową rolę odgrywają dokładny wywiad i badanie przedmiotowe, a następnie badanie ultrasonograficzne nerek z oceną przepływów metodą Dopplera, umożliwiające rozpoznanie zwężenia tętnicy nerkowej, utrudnienia odpływu moczu oraz torbieli.
4. U chorych na PChN we wczesnym stadium zaawansowania należy okresowo podejmować badania i interwencje, by zwolnić progresję choroby nerek i zapobiec jej powikłaniom
U osób z PChN należy dążyć do zwolnienia postępu choroby. Leki nefrotoksyczne, takie jak NLPZ, antybiotyki aminoglikozydowe oraz radiologiczne środki cieniujące, trzeba stosować ostrożnie lub ich unikać. Należy często mierzyć ciśnienie tętnicze i utrzymywać je poniżej 130/80 mmHg. Jeśli choroba przebiega z białkomoczem, konieczne może być uzyskanie jeszcze mniejszych wartości ciśnienia. Okresowo oznacza się stosunek białka do kreatyniny w moczu, a jego wartość ≥1 sugeruje większe zagrożenie progresją PChN.
Inhibitory ACE oraz antagoniści receptorów AT1 dla angiotensyny II (sartany) mogą zwalniać progresję PChN, zwłaszcza u chorych z białkomoczem. Ponadto leki te, obniżając ciśnienie tętnicze, zmniejszają ciśnienie krwi w naczyniach włośniczkowych kłębuszków nerkowych oraz przesączanie białek, co przyczynia się do zwolnienia progresji choroby. Ograniczają też proliferację i włóknienie komórek, w których pośredniczy angiotensyna II.11 Inhibitory ACE i sartany stosowane w terapii skojarzonej silniej hamują białkomocz niż każdy z tych leków osobno, należy jednak starannie śledzić wówczas stężenia kreatyniny i potasu w surowicy, które mogą się zwiększać.11,12 Chorzy z postępującą PChN są obciążeni ryzykiem rozwoju osteodystrofii nerkowej. Wszyscy chorzy na PChN 3. lub 4. stopnia wymagają ścisłego monitorowania stężeń fosforu, wapnia i parathormonu. Przy nieprawidłowych wartościach należy zmniejszyć podaż fosforanów w diecie, podać doustne leki wiążące fosforany lub witaminę D.
Chorzy na PChN są również obciążeni zwiększonym ryzykiem wystąpienia powikłań ze strony układu krążenia, w tym zawału serca.13 Należy podawać im kwas acetylosalicylowy (np. 81 mg/24 h) oraz intensywnie zmniejszać stężenia lipidów, m.in. za pomocą inhibitorów reduktazy 3-hydroksy-3-metyloglutarylo-koenzymu A (statyn), tak by osiągnąć stężenie cholesterolu LDL ≤100 mg/dl (aby wyrazić je w mmol/l, należy pomnożyć tę wartość przez 0,0259). U osób z PChN i współistniejącą chorobą wieńcową niektórzy zalecają zmniejszenie stężenia cholesterolu LDL do ≤70 mg/dl. W kilku opublikowanych ostatnio badaniach sugerowano, że statyny mogą dodatkowo zmniejszać białkomocz.4,13 Określenie, czy dokładniejsza kontrola stężenia cholesterolu LDL przekłada się na zmniejszenie częstości występowania powikłań sercowo-naczyniowych lub progresji schyłkowej niewydolności nerek, wymaga dalszych badań.
Wczesne skierowanie do nefrologa należy rozważyć w sytuacji, gdy następuje progresja PChN lub pojawiają się trudne do opanowania powikłania, takie jak białkomocz o nasileniu zbliżonym do obserwowanego w zespole nerczycowym, oporne na leczenie nadciśnienie tętnicze, niedająca się opanować wtórna nadczynność przytarczyc lub znaczące zmiany w osadzie moczu. Konsultację specjalisty w dziedzinie chorób nerek lub współpracę z nim zaleca się w leczeniu chorych na PChN 3. stopnia (GFR 30-59 ml/min/1,73 m2). Wszystkich chorych z GFR <30 ml/min/1,73 m2 (PChN 4. lub 5. stopnia) należy skierować do nefrologa.9
5. Nie należy automatycznie przerywać leczenia inhibitorem ACE lub sartanem z powodu niewielkiego zwiększenia stężenia kreatyniny lub potasu w surowicy
W leczeniu chorych na PChN ważną rolę odgrywają dwie grupy leków – inhibitory ACE i sartany. W chorobach nerek przebiegających z białkomoczem nie są one stosowane wyłącznie w celu uzyskania optymalnych wartości ciśnienia tętniczego (Joint National Commission VII), ale również w celu leczenia białkomoczu (po dostosowaniu dawek). Stosuje się je również – jako leki z wyboru – aby zapobiegać progresji choroby.12,14,15 U chorych rozpoczynających leczenie inhibitorem ACE lub sartanem, albo zaczynających przyjmować je w większych dawkach niekiedy przejściowo zwiększa się stężenie kreatyniny w surowicy. Zwiększenie o 20-30% można zaakceptować,16 ale ważne jest, aby to podwyższone stężenie ustabilizowało się i nie wzrastało dalej. U niektórych chorych zwiększa się też niekiedy stężenie potasu w surowicy. Jeśli osiąga ono wartość 5,5 mEq/l (aby wyrazić je w mmol/l, należy pomnożyć tę wartość przez 1,0) można je akceptować, dopóki jest stabilne, a chory zdaje sobie sprawę z konieczności ograniczenia zawartości potasu w diecie i nie przyjmuje leków zwiększających hiperkaliemię, np. spironolaktonu. Stężenia kreatyniny i potasu w surowicy należy obserwować przez tydzień. Zwiększenie stężenia kreatyniny o ponad 20-30% lub niedająca się opanować hiperkaliemia wymuszają przerwanie leczenia inhibitorem ACE lub sartanem albo zmniejszenie dawek tych leków. Konieczne jest częste monitorowanie chorych. W leczeniu nadciśnienia tętniczego lub hiperkaliemii w przebiegu PChN przydatne są też leki moczopędne zmniejszające GFR, takie jak furosemid lub metolazon [lek z grupy pochodnych tiazydopodobnych, niedostępny w Polsce – przyp. red.]. Trzeba jednak dodać, że odwodnienie chorego sprzyja zwiększeniu stężenia kreatyniny pod wpływem przyjmowania inhibitora ACE lub sartanu.