IV edycja Kongresu HPV już 12-13 czerwca! Poznaj najnowsze trendy w profilaktyce, diagnostyce i leczeniu raka szyjki macicy i innych schorzeń związanych z HPV | Sprawdź >
Metody badawcze
Zastosowanie metody mikromacierzy tkankowych w onkologii
Dr hab. med. Leszek Gottwald1
Prof. dr hab. med. Jacek Fijuth2
W ostatnich latach obserwowany jest wzrost zainteresowania wykorzystaniem w naukach medycznych jak najmniej kosztownych, a jednocześnie wystarczająco precyzyjnych metod. Z tego powodu coraz większe uznanie w prowadzeniu badań immunohistochemicznych nad nowotworami zyskuje stale unowocześniana metoda mikromacierzy tkankowych (ang. tissue microarray, TMA).[1-7]
W pracy przW pracy przedstawiono obecne poglądy na temat praktycznych aspektów stosowania metody TMA w onkologii. Zwrócono uwagę na nowe możliwości jej wykorzystania w badaniach nad biologią nowotworów.
Metoda TMA w obecnej formie została opisana po raz pierwszy przez Kononena i wsp. w 1998 roku.[7] Jej istotą jest zgromadzenie w pojedynczym bloku parafinowym tkanek z wielu nowotworów, które są następnie oceniane jako pojedynczy preparat mikroskopowy.[8-12] Chociaż główne założenia metody pozostają niezmienione, to jednak nadal wprowadzane są jej modyfikacje.[6,13-17]
Metoda TMA jest stosowana z użyciem tych samych protokołów co w klasycznej metodzie histopatologicznej w badaniach immunohistochemicznych (IHC), do hybrydyzacji fluorescencyjnej in situ (FISH) oraz do hybrydyzacji in situ RNA.[2,3,8,9,18,19] Jest szczególnie użyteczna do prowadzenia badań na dużych grupach przypadków i z licznymi przeciwciałami.[20] Nie wykorzystuje się jej w celu ustalenia rozpoznania choroby nowotworowej, jednak jest ona coraz powszechniej stosowana w badaniach nad biologią nowotworów.[9,11,15,20] Zgodność wyników badań wykonywanych klasyczną metodą histopatologiczną i metodą TMA wynosi 88-100 proc.[5,21]
Za najistotniejsze jej zalety uznaje się redukcję kosztów w wyniku zużycia do badań znacząco mniejszych objętości przeciwciał, substancji pomocniczych i liczby szkiełek mikroskopowych, wykonywanie kolejnych odczynów immunohistochemicznych zawsze na precyzyjnie ustalonym i zawsze tym samym fragmencie guza oraz skrócenie czasu potrzebnego do przeprowadzenia badań.[3,4,9,10,14,16,19-24] W badaniach z wieloma przeciwciałami ograniczenie pola oceny do 1-2 mm zawsze tego samego fragmentu tkanki czyni wyniki porównywalnymi i bardziej wiarygodnymi.[3,4,9,14,16,23,24] Cały proces wytwarzania pojedynczego bloku-biorcy TMA, obejmujący dwukrotną biopsję każdego z 20 bloków-dawców, przenoszenie bioptatów i umieszczanie ich w bloku-biorcy TMA, aż do skompletowania w nim 40 bioptatów o średnicy 2 mm, zajmuje około 2 godzin.[21] Gulmann i wsp. opisali konstrukcję bloku TMA utworzonego z 240 bioptatów o średnicy 0,6 mm w ciągu 6-8 godzin.[11] Dla porównania doświadczonemu technikowi laboratoryjnemu skrojenie preparatów z 80 przypadków klasyczną metodą histopatologiczną i wykonanie w nich odczynów immunohistochemicznych zajmuje około 24 godzin.[11]
Wytwarzanie TMA
Podczas wytwarzania mikromacierzy tkankowych wyróżnić można kilka następujących po sobie etapów. W pierwszym z nich z odpowiednich bloków parafinowych zawierających badane tkanki, tzw. bloków-dawców (ang. donor block), wykonywane są preparaty mikroskopowe w celu znalezienia i zaznaczenia na preparacie miejsc najbardziej reprezentatywnych dla danego rozpoznania.[10,13] W trakcie kolejnego etapu, z miejsc odpowiadających zaznaczonym obszarom na parafinowym bloku-dawcy pobierane są walcowate fragmenty tkankowe o średnicy od 0,6 mm do kilku mm, które następnie są umieszczane w odpowiednich co do średnicy otworach w gotowych blokach-biorcach TMA (ang. recipient block).[7,13,18] Bardzo istotne znaczenie ma układ bioptatów w bloku-biorcy TMA, który musi umożliwiać w sposób jednoznaczny identyfikację poszczególnych próbek tkankowych w preparacie mikroskopowym.[14] Pojedynczy blok-biorca TMA może zawierać tkanki od kilkudziesięciu do nawet kilkuset nowotworów.[9,18] Ostatnim etapem jest zatopienie bloku-biorcy TMA w parafinie. Poprzeczne cięcie tak powstałego TMA pozwala uzyskać do 200 skrawków o grubości 4 µm zawierających tkanki zawsze z tych samych lokalizacji badanych guzów. Uzyskany metodą TMA pojedynczy skrawek umieszczony na szkiełku podstawowym jest barwiony i oceniany jako jeden preparat mikroskopowy.[8,10,14,23] Proces wytwarzania bloku-biorcy TMA oraz przykładowe obrazy mikroskopowe uzyskiwane tą metodą zobrazowano na fot. 1-4.

Ryc. 1. Przykładowe elementy używane do wytwarzania mikromacierzy tkankowych: A – parafinowy blok-dawca, B – preparat histologiczny z bloku-dawcy z zaznaczonym obszarem zajętym przez nowotwór, C – zestaw Tissue-Tek Quick-Ray TMA System, D – parafinowy blok-biorca zawierający 60 otworów o średnicy 2 mm.

Ryc. 2. Wytwarzanie mikromacierzy tkankowych: A – technika biopsji bloku-dawcy, B – pobrany bioptat przed umieszczeniem w bloku-biorcy, C – blok-biorca częściowo wypełniony bioptatami z bloku-dawcy, D – gotowy parafinowy blok-biorca (TMA).
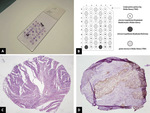
Ryc. 3. A – preparat histologiczny z TMA (H+E), B – przykładowe rozmieszczenie poszczególnych bioptatów w bloku-biorcy, C + D – dwumilimetrowe bioptaty z tkankami gruczolakoraka
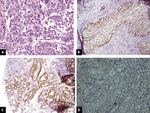
Ryc. 4. Obrazy mikroskopowe gruczolakoraka endometrium w metodzie TMA: A – bawienie H+E (powiększenie 400 x), B – silna ekspresja receptorów estrogenowych (powiększenie 200 x), C – silna ekspresja receptorów progesteronowych (powiększenie 200 x), D – silna ekspresja Ki67 (powiększenie 200 x).
Kontrowersje dotyczące stosowania metody TMA
Pomimo ciągłego doskonalenia metody TMA, niektóre problemy związane z jej stosowaniem nadal pozostają przedmiotem dyskusji.[3,4,6,7,25] Liczne kontrowersje towarzyszą reprezentatywności 1-2-mm fragmentów tkankowych w przypadkach nowotworów o zróżnicowanej budowie morfologicznej.[20,26] Rozwiązaniem tej kwestii może być pobieranie większej liczby biopsji z bloku-dawcy lub zwiększenie średnicy pobieranych fragmentów tkankowych do co najmniej 3 mm.[11,15,26] W obu przypadkach ceną za poprawę efektywności metody TMA jest jednak większe uszkodzenie parafinowego bloku-dawcy. Nie można tego faktu bagatelizować, ponieważ w razie konieczności różnicowania wznowy nowotworu z guzem o podobnej strukturze histologicznej u tej samej chorej, przy braku materiału z pierwotnego rozpoznania, porównanie obu nowotworów nie jest możliwe. Obecnie przyjmuje się, że dwa do czterech bioptatów pobranych z bloku-dawcy i przeniesionych do bloku-biorcy TMA wystarczą do oceny morfologii guza nowotworowego.[2,9-11,15,21,27] Pogląd ten wydaje się słuszny, jednak przy założeniu, że pobrane bioptaty będą miały odpowiednią średnicę.
Średnica pobieranego bioptatu jest jednym z kluczowych czynników warunkujących reprezentatywność pobranego materiału w metodzie TMA. W sprzedaży komercyjnej znajdują się igły do biopsji parafinowych bloków-dawców o średnicy 0,6-5 mm.[4,8,11,27] W piśmiennictwie dostępne są doniesienia mówiące o stosowaniu różnej średnicy igieł TMA w nowotworach ginekologicznych.[27] Przykładowo, Fowler i wsp. wykonali mikromacierze tkankowe z 0,6-mm bioptatami do oceny ekspresji COX-2 i aromatazy w 336 przypadkach raka endometrium (różne typy histologiczne).[3] Z kolei Kim i wsp., podobnie jak ja, wykorzystali do produkcji TMA igły o średnicy 2 mm w grupie 332 chorych z rakiem szyjki macicy.[2] Ci badacze, którzy preferują bioptaty o średnicy 0,6 mm jako wystarczające do oceny histopatologicznej, wskazują na korzyści ekonomiczne takiego rozwiązania. W pojedynczym tak skonstruowanym bloku TMA można bowiem umieścić nawet do kilkuset bioptatów o średnicy 0,6 mm.[13,14,22,24,27] Przeciwnicy stosowania tak małych średnic wskazują, że pobrany w ten sposób materiał z bloku-dawcy może nie być reprezentatywny dla całości nowotworu.[20,26]
W piśmiennictwie szeroko dyskutowany jest problem utraty materiału tkankowego podczas wytwarzania TMA. Utrata materiału tkankowego rozumiana jako sytuacja, gdy materiał jest obecny w bloku-dawcy, a nie ma go na preparacie mikroskopowym przygotowanym z bloku-biorcy, jest szacowana przez różnych autorów na 3-30 proc.[4,26,28] Hernandez i wsp. wykonali TMA z 317 przypadków raka jelita grubego i odbytnicy z efektywnością wynoszącą 90,2 proc.[29] Podobne wyniki uzyskali inni autorzy.[20] Za jedną z przyczyn utraty materiału tkankowego podczas wytwarzania TMA uznaje się niską jakość parafinowego bloku-dawcy.[4] Uważa się, że jeżeli proces utrwalania tkanek pobranych operacyjnie trwał zbyt długo lub blok był zbyt wysuszony podczas przechowywania, istnieje znaczne ryzyko jego pęknięcia i w konsekwencji – nieodwracalnego uszkodzenia.[30] Z kolei w przypadkach, gdy z bloku pobrano już uprzednio wiele wycinków i grubość tkanki w bloku jest niewielka, ilość materiału tkankowego może być niewystarczająca do uzyskania reprezentatywnego fragmentu tkankowego w TMA.[30,31]
Niektórzy autorzy, w tym Kong i wsp. oraz Kajdacsy-Balla i wsp., proponują w takich przypadkach radiograficzną ocenę grubości bloków parafinowych dla danego przypadku i na tej podstawie dokonanie wyboru najbardziej odpowiedniego bloku-dawcy.[31,32] Uważa się, że szczególnie gdy skrawki tkankowe są cienkie, ryzyko zbyt głębokiego lub zbyt płytkiego osadzenia bioptatu w bloku-biorcy znacząco wzrasta.[21] Gulmann i wsp. uważają, że gdy bioptaty osadzone są w bloku-biorcy na różnych głębokościach, tj. zbyt głęboko lub zbyt płytko, reprezentatywność tkanek w kolejnych następujących po sobie skrawkach może być różna.[11] Należy zwrócić również uwagę na znaczenie wielkości obszaru zajmowanego przez nowotwór w bloku-dawcy. Gdy nowotwór zajmuje w nim mały obszar, identyfikacja odpowiedniego miejsca na bloku-dawcy i efektywne pobranie z niego materiału do wytworzenia TMA może być trudne lub wręcz niemożliwe.[21]

