W latach 80. XX wieku w celu uniknięcia niekorzystnych następstw szerokiego wycięcia chirurgiczne usunięcie nowotworu zaczęto łączyć z technikami stosowanymi w chirurgii plastycznej pozwalającymi na modelowanie piersi – ich podnoszenie, zmniejszanie etc. (Jean-Yves Petit, Jean-Yves Bobin, Michel Abbes). Werner Audretsch zaproponował termin „chirurgia onkoplastyczna” (oncoplastic surgery) łączący oba sposoby operowania. Ubytek powstały po wycięciu guza może zostać uzupełniony:
- tkankami przesuniętymi z innej części modelowanej piersi (volume displacement)
- tkankami przesuniętymi spoza piersi w postaci uszypułowanych płatów z zachowanym dopływem krwi (volume replacement).
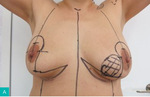
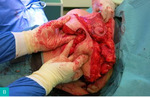
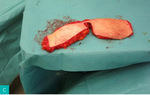
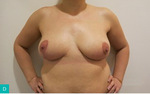
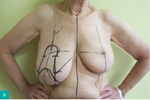
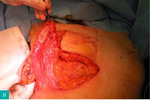
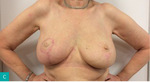
Rycina 4A-D. A. Guz dolnego wewnętrznego kwadrantu lewej piersi. Pierś obrysowana do zabiegu mastoplastyki sposobem płata górno-przyśrodkowego, limfadenektomii pachowej lewostronnej i symetryzacji. B. Wypreparowany płat i preparat obejmujący kwadranty dolne z guzem. C. Preparat obejmujący kwadranty dolne z guzem. D. Efekt po 4 tygodniach od zabiegu
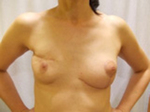
Rycina 5. Pacjentka po wykonanym 9 lat wcześniej zabiegu sposobem szerokiego wycięcia raka prawej piersi, operowana następnie z powodu niezależnego, metachronicznego raka lewej piersi – wykonano mastoplastykę terapeutyczną sposobem dolnego płata
Przykładami pierwszego sposobu (volume displacement) są wycięcie guza położonego powyżej kompleksu brodawka sutkowa–otoczka i uzupełnienie ubytku fragmentem piersi przesuniętym z jej dolnej części (plastyka sposobem dolnego płata szeroko stosowana podczas zabiegu mastopeksji, czyli podniesienia opadającej piersi) oraz operacje wykorzystujące płat górny, górno-przyśrodkowy lub kombinacje wyżej wymienionych płatów. Płat stanowi zdeepitelializowany fragment gruczołu obejmujący kompleks brodawka sutkowa–otoczka przemieszczony w miejsce wyciętej części piersi: w chirurgii plastycznej – nadmiaru gruczołu, a w chirurgii onkologicznej – loży po wycięciu guza. Onkoplastyka łączy oba cele (ryc. 4, 5). Pierś modelujemy zatem podczas zabiegu wycięcia guza.
Przykładem drugiego sposobu (volume replacement) jest zastosowanie tkanek w postaci płatów przesuniętych z sąsiedztwa piersi, np.: z nadbrzusza: płata piersiowo-nadbrzusznego składającego się ze skóry i tkanki podskórnej, zrotowanego w stronę ubytku, płata opartego na perforatorze bocznym tętnicy międzyżebrowej (LICAP – lateral intercostal artery perforator), płata opartego na perforatorze przednim (AICAP – anterior intercostal artery perforator); z pachy z płata opartego na perforatorach piersiowo-grzbietowych (TDAP – thoracodorsal artery perforator) czy płata z mięśnia najszerszego grzbietu (LD – latissimus dorsi) (ryc. 6). Onkoplastyka pozwala na usunięcie dużych zmian bez obaw o zły efekt estetyczny, szczególnie jeśli szacowana objętość preparatu przekracza 20% objętości piersi.
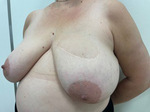
Rycina 6. Stan po zabiegu typu replacement technique wykonanym z powodu mięsaka górnego zewnętrznego kwadrantu lewej piersi (osteosarcoma pozaszkieletowego). Ubytek uzupełniono płatem z mięśnia najszerszego grzbietu (LD)
Inny podział technik onkoplastycznych o znaczeniu praktycznym wyróżnia:
- zabiegi onkoplastyczne poziomu 1 – polegające na podpreparowywaniu skóry i odpreparowywaniu płatów gruczołu od powięzi leżących pod nim mięśni oraz ich rotacji w miejsce loży po wycięciu guza, przesunięciu lub podpreparowaniu kompleksu brodawka sutkowa–otoczka
- zabiegi onkoplastyczne poziomu 2 – operacje uzupełnienia ubytków za pomocą płatów skórno-gruczołowych, których sztandarowymi przykładami są mastoplastyki sposobem dolnego lub górnego płata, wywodzące się z chirurgii plastycznej i opracowane w celu podniesienia oraz zmniejszenia opadających piersi.
Zabiegi z grupy pierwszej znajdują zastosowanie szczególnie w przypadku zmian stanowiących 15-20% objętości piersi, a gdy zachodzi konieczność wycięcia preparatu stanowiącego 20-50% (!) objętości gruczołu, ale u pacjentek zakwalifikowanych do leczenia oszczędzającego, przeprowadza się zabiegi z grupy drugiej6.
Rycina 7A-C. A. Pacjentka z asymetrią piersi po lewostronnej mastoplastyce terapeutycznej sposobem dolnego płata i napromienianiu. B. Dolny płat (zdeepitelializowany). C. Efekt po 4 tygodniach od zabiegu symetryzacji (prawostronnej mastoplastyce zmniejszającej sposobem dolnego płata)
Kolejnym czynnikiem wpływającym na wybór optymalnej metody z wyżej wymienionych grup jest rodzaj utkania piersi. Podział według American College of Radiology (ACR) wyróżnia 4 podstawowe rodzaje utkania: gruczołowy, gruczołowo-tłuszczowy, tłuszczowo-gruczołowy i tłuszczowy. Zabiegi poziomu 1 polegające na odpreparowaniu gruczołu od skóry (np. zabieg sposobem round block) wykonywane u pacjentek z piersiami o przewadze utkania tłuszczowego wiążą się z niekorzystnym efektem estetycznym, który może się pojawić po napromienianiu, i z tego względu należy tych technik unikać u tych chorych. W ich przypadku zastosowanie znajdują operacje polegające na przesuwaniu płatów z innych części piersi, np. mastoplastyka sposobem dolnego, górnego czy górno-przyśrodkowego płata, przemieszczonego z innej części piersi i wypełniającego lożę powstałą po wycięciu guza6. Wybór konkretnej metody plastyki zależy od: lokalizacji guza, jego wymiarów, rozmiarów piersi i jej utkania. Znaczenie mają też czas, organizacja pracy, często poziom refundacji – czy podczas zabiegu usunięcia nowotworu możemy wykonać jednoczesną symetryzację drugiej piersi i czy życzy sobie tego pacjentka. Wykonanie mastoplastyki terapeutycznej i uzyskanie radykalności, dobrego kształtu i wielkości piersi przy pozostawieniu opadającej i asymetrycznej drugiej piersi jest frustrujące dla obu stron (ryc. 7).
Zalety zabiegów onkoplastycznych
Korzyści z zastosowania onkoplastyki nie ograniczają się jedynie do efektu estetycznego. Możliwość wycięcia dużego fragmentu gruczołu bez obaw o spowodowanie deformacji, wykonalna dzięki wypełnieniu ubytku, pozwala na uzyskanie szerokiego marginesu chirurgicznego. Jakkolwiek szerokość marginesu nie koreluje dodatnio z przeżywalnością ani z ryzykiem nawrotu (nie udowodniono, że im większy margines, tym mniejsze ryzyko nawrotu; obowiązujący margines oznacza brak komórek raka inwazyjnego w linii cięcia oznakowanej tuszem, dla przewodowego raka przedinwazyjnego [DCIS – ductal carcinoma in situ] wynosi 2 mm), wycięcie preparatu o dużej objętości (np. części opadającej piersi położonej poniżej fałdu podsutkowego) bez obaw o spowodowanie ubytku prowadzącego do asymetrii pozwala na zmniejszenie ryzyka nieradykalności mikroskopowej.
Kolejność składowych terminu „onkoplastyka” nie jest zatem przypadkowa i nie wynika z chęci zachowania melodyjnej wymowy. Priorytetem jest wyleczenie chorych na potencjalnie śmiertelną chorobę.
Dzięki onkoplastyce spada liczba nawrotów miejscowych oraz ponownych zabiegów poszerzenia marginesu. W metaanalizie Loskena, obejmującej 5494 kobiety zoperowane sposobem szerokiego wycięcia (z 20 badań) i 3165 chorych leczonych w sposób onkoplastyczny (z 41 badań), wykazano odsetek nawrotów miejscowych wynoszący 7% w pierwszej grupie i 4,2% w drugiej. W przypadku średniej wielkości guzów wynoszącej 1,2 cm w grupie szerokiego wycięcia wobec 2,7 cm w grupie onkoplastycznej wielkość preparatów była w drugiej grupie 4-krotnie większa. Brak radykalności mikroskopowej stwierdzono rzadziej w grupie onkoplastycznej (12,3% vs 20,6%). Tym samym reoperacje wykonano odpowiednio u 4% i 14,6% pacjentek, przy czym u chorych poddanych zabiegowi sposobem szerokiego wycięcia ponowna operacja częściej polegała na amputacji piersi. Satysfakcja z uzyskanego efektu estetycznego była większa u kobiet operowanych w sposób onkoplastyczny niż w grupie szerokiego wycięcia (odpowiednio 89,5% vs 82,9%)7.
W badaniu przeprowadzonym w Polsce stwierdzono niższy odsetek zajętych marginesów w grupie kobiet leczonych w sposób onkoplastyczny (59 pacjentek, u których wykonano plastykę B) w porównaniu z grupą chorych operowanych sposobem szerokiego wycięcia (7,4% vs 21,4%), większą objętość preparatów pooperacyjnych (116,48 cm3 [±82,82 cm3] wobec 103,21 cm3 [±64,36 cm3]) oraz wyższą jakość życia w grupie kobiet leczonych za pomocą technik onkoplastycznych8.
W części przypadków guzy zbyt duże, by mogły zostać wycięte z dobrym rezultatem estetycznym, mogą ulec regresji dzięki przedoperacyjnemu leczeniu systemowemu (downstaging). Wówczas rozpoczynamy leczenie od leczenia systemowego zamiast chirurgii. Zabieg wykonywany po uzyskaniu regresji klinicznej polega na wycięciu guza resztkowego lub miejsca zmiany oznakowanego przed rozpoczęciem leczenia znacznikiem wprowadzanym pod kontrolą USG lub niekiedy mammografu stereotaktycznego (w przypadku skupisk mikrozwapnień niewidocznych w USG). Przedoperacyjne leczenie systemowe jest optymalną metodą dla chorych z guzami potrójnie ujemnymi (bez ekspresji trzech pierwszych wyżej wymienionych receptorów) oraz z nadekspresją receptora HER2, większymi niż 2 cm (cT2) oraz w przypadkach klinicznych zajęcia pachowych węzłów chłonnych (cN1), niezależnie od cechy T. Tak prowadzone leczenie wymaga ścisłej współpracy lekarzy różnych specjalności wchodzących w skład zespołów specjalizujących się w leczeniu chorych na raka piersi (Breast Units): chirurgów, chemioterapeutów, radioterapeutów, patomorfologów i radiologów, ustalenia planu leczenia przed jego rozpoczęciem, odpowiedniego poinformowania chorej i koordynacji działań.
Ponadto na wybór optymalnej metody operacyjnej wpływają czynniki zależne od pacjentek, takie jak wskaźnik masy ciała (BMI – body mass index) i styl życia, szczególnie palenie tytoniu, gdyż poprzez wazokonstrykcyjny efekt nikotyny niekorzystnie wpływa ona na gojenie ran oraz zwiększa ryzyko niedokrwienia i martwicy. Do rozpoczęcia leczenia chirurgicznego zabraknie czasu na normalizację masy ciała, ale zdecydowanie warto zalecić całkowite zaprzestanie palenia przed planowaną operacją.