SPECT
Radioznacznikiem najczęściej stosowanym (w Polsce praktycznie jedynym) jest metoksy-izobutylo-izonitryl (MIBI) znakowany technetem Tc-99m. Jest to znacznik perfuzji i żywotności. Jego wychwyt w kardiomiocytach zależy od regionalnego przepływu krwi w warunkach podania (w spoczynku albo podczas maksymalnego wysiłku lub wazodylatacji) oraz od zachowanej ciągłości błon komórkowych.
Ocena niedokrwienia mięśnia sercowego
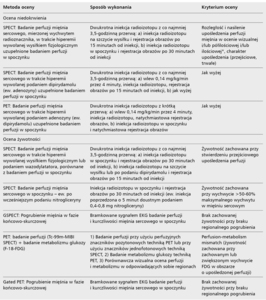
Tabela 2. Metody oceny niedokrwienia oraz żywotności mięśnia sercowego za pomocą badań radioizotopowych
Zwężenia w naczyniach wieńcowych skutkują niejednorodnością przepływu, przekładając się na niejednorodny wychwyt radioznacznika w komórkach mięśnia sercowego. Niejednorodność zwiększa się, gdy rośnie zapotrzebowanie na tlen podczas wysiłku lub – jeśli pacjent nie jest w stanie wykonać wystarczającego wysiłku – po zastosowaniu wazodylatatora (w Polsce stosuje się głównie dipirydamol w dawce 0,14 mg/kg/min przez 4 minuty). W celu wykrycia niedokrwienia wywołanego obciążeniem wymagane są dwa oddzielne podania Tc-99m-MIBI – w spoczynku i obciążeniu (tab. 2).
Podstawowym rodzajem analizy obrazów SPECT jest ocena jakościowa. Upośledzone gromadzenie MIBI w wysiłku przy prawidłowym gromadzeniu w spoczynku (tzw. ubytek przejściowy) odpowiada niedokrwieniu indukowanemu obciążeniem i wiąże się ze zwężeniem naczynia zaopatrującego w krew dany obszar miokardium. Nieprawidłowe (ale większe niż w wysiłku) gromadzenie w spoczynku (tzw. ubytek częściowo przejściowy) wiąże się z krytycznym zwężeniem naczynia, upośledzającym również przepływ spoczynkowy i/lub z obecnością martwych kardiomiocytów w danym obszarze.
Dodatkowo perfuzję powinno się oceniać półilościowo, stosując podział mięśnia LV na 17 segmentów i 5-stopniową skalę upośledzenia wychwytu w segmencie [20-22]. Podejście półilościowe dostarcza sumaryczne wskaźniki niedokrwienia w obciążeniu (summary stress score, SSS) i w spoczynku (summary rest score, SRS). SSS ma istotne znaczenie prognostyczne: im upośledzenie perfuzji wysiłkowej jest większe, tym większe jest ryzyko wystąpienia zdarzeń sercowo-naczyniowych. W europejskich wytycznych dotyczących rewaskularyzacji wskazaniem klasy IB jest udokumentowany duży obszar niedokrwienia (>10% LV) [23]. Wskazanie to oparto głównie na ocenie niedokrwienia za pomocą półilościowej analizy badań SPECT.
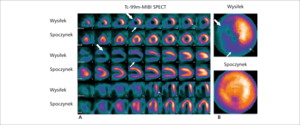
Rycina 3. Wychwyt Tc-99-MIBI w badaniu SPECT perfuzji mięśnia LV serca u pacjenta z chorobą trzech naczyń.
W celu ułatwienia oceny jakościowej dodatkowo stosuje się prezentację wychwytu radioznacznika w postaci zbiorczych map bull’s-eye (ryc. 3). Mapy umożliwiają również dokonywanie uzupełniającej ilościowej oceny badań przez cyfrowe porównanie z mapami uzyskanymi u osób zdrowych.
Nawet po uwzględnieniu ilościowej metody ocena perfuzji w badaniach SPECT ma charakter normatywny – wychwyt w danym obszarze mięśnia sercowego zawsze odnoszony jest do maksymalnego wychwytu w całym mięśniu, który przyjmuje się za wychwyt prawidłowy. Jest to podstawowe ograniczenie: SPECT odzwierciedla jedynie względną niejednorodność przepływu. Brak bezwzględnej ilościowej oceny przepływu w ml/min/g wynika ze zjawisk fizycznych zaburzających proces akwizycji danych.
Wartość diagnostyczna badań SPECT w spoczynku i w wysiłku w ChNW w największej metaanalizie została określona następująco: czułość wykrywania zwężeń ≥50% w angiografii kontrastowej – 87%, swoistość – 73% [24].
Korekta osłabienia promieniowania (wprowadzanego np. przez sutek lub przeponę, które mogą symulować ubytki perfuzji w SPECT), przeprowadzana z wykorzystaniem tomografii komputerowej w ostatnio produkowanych urządzeniach hybrydowych SPECT-CT, prowadzi do poprawy swoistości badań SPECT do 80-90% [25].
Zastosowanie techniki SPECT bramkowanej sygnałem EKG pacjenta (gated SPECT, GSPECT) rejestrującej dane perfuzyjne w 8-16 fazach cyklu serca dostarcza informacje jednocześnie o globalnej i regionalnej frakcji wyrzutowej (EF), objętości późnorozkurczowej (EDV) i późnoskurczowej (ESV) oraz o regionalnej kurczliwości i grubieniu ścian LV. Łączna ocena wyników perfuzji i funkcji ułatwia identyfikowanie artefaktów spowodowanych osłabieniem promieniowania i zwiększa swoistość badań SPECT. Co więcej, GSPECT przez identyfikację zaburzeń kurczliwości zwiększa prawdopodobieństwo identyfikacji nieprawidłowych segmentów u pacjentów z chorobą trzech naczyń o ok. 50% [26].
Wyniki badań perfuzji mają wysoką, niezwykle szeroko udokumentowaną wartość prognostyczną [24,27-29]. Prawidłowy wynik określa pacjentów niskiego ryzyka zdarzeń sercowych (<1% rocznie). Dodatni wynik zwiększa ryzyko zdarzeń kilkakrotnie (u pacjentów z dużym upośledzeniem perfuzji w wysiłku – do 7-9% na rok).
Nowa generacja kamer hybrydowych SPECT-CT, poza wykorzystywaniem transmisyjnych obrazów CT do zoptymalizowanej korekty osłabienia w obrazach SPECT, w kardiologii służy do integracji wyników badań SPECT z CSCT (calcium scoring CT – ocena zwapnień w tętnicach wieńcowych) i (lub) z CTA (angiography CT – nieinwazyjna koronarografia) [19,25]. Jednak swoiście zweryfikowane algorytmy nowoczesnej anatomiczno-czynnościowej diagnostyki ChNW muszą dopiero powstać.
Technika SPECT nie jest wolna od artefaktów związanych z ruchem pacjenta (długi czas rejestracji). Poza tym z definicji badania scyntygrafia perfuzyjna pozwala wykryć tylko te zwężenia w tętnicach wieńcowych, które dają mierzalne zaburzenia perfuzji (może nie wykrywać wczesnych zmian miażdżycowych, które mają znaczenie w prewencji rozwoju ChNW). Ponadto metoda wykorzystuje promieniowanie jonizujące i niesie ze sobą określone (choć małe) ryzyko dla pacjenta. Urządzenia hybrydowe nieznacznie zwiększają to ryzyko.
Ocena żywotności mięśnia sercowego
Komórkowa retencja Tc-99m-MIBI wymaga nienaruszonych procesów błonowych i mitochondrialnych, zatem z definicji radioznacznik ten jest markerem żywotności. W badaniach histopatologicznych potwierdzono, że spoczynkowy miokardialny wychwyt Tc-99m-MIBI wykazuje wysoką odwrotną zależność z ilością fibrozy w ludzkich bioptatach [30,31].
MIBI jest jednak także znacznikiem perfuzyjnym i jego wychwyt zależy od przepływu krwi. Dlatego ocena żywotności może być zaniżona, gdy przepływ krwi jest silnie upośledzony i podaż radiofarmaceutyku znacznie ograniczona.
Podstawowym kryterium oceny żywotności jest ocena przejściowości wysiłkowych ubytków perfuzji – obecność całkowicie przejściowych ubytków oznacza niedokrwienie (i całkowicie zachowaną żywotność kardiomiocytów) (tab. 2, ryc. 3). Ubytek częściowo przejściowy wskazuje, że przynajmniej część tkanki w danym obszarze ma zachowaną żywotność. Brak poprawy (ubytek trwały) zwiększa prawdopodobieństwo martwicy. Na potrzeby oceny żywotności diagnostyka często zostaje uproszczona do badania wyłącznie spoczynkowego wychwytu MIBI – zazwyczaj stosuje się metodę progową, przyjmując, że w dysfunkcjonalnych segmentach wychwyt powyżej 50-60% wychwytu maksymalnego identyfikuje segmenty żywotne [30-32]. Mimo zbliżonego wychwytu spoczynkowego pooperacyjne losy ubytków częściowo przejściowych i ubytków trwałych są jednak odmienne i ujawnienie przejściowości za pomocą badania obciążeniowego dokładniej przewiduje powrót funkcji LV po rewaskularyzacji [33].