
Rycina 1. Rozkład czasu wystąpienia objawów mięśniowych od chwili rozpoczęcia leczenia statyną (wykres po lewej stronie) lub po zwiększeniu dawki statyny (wykres po prawej stronie)
Kliniczny obraz mialgii był różnorodny, a objawy występowały zazwyczaj krótko po rozpoczęciu leczenia dużymi dawkami statyn lub po zwiększeniu dawki (ryc. 1). Mediana czasu, po którym od rozpoczęcia leczenia lub jego intensyfikacji występowały objawy mięśniowe, to miesiąc. Wniosek, że czas wystąpienia objawów mięśniowych był związany (logarytmiczna transformacja danych) z rozpoczęciem leczenia czy też ze zwiększeniem dawek statyn, wskazuje na zależność przyczynowo-skutkową tych dwóch zdarzeń.34 Trzeba zaznaczyć, że u ok. 15% chorych zgłaszających objawy mięśniowe rozpoczęły się one później niż 6 miesięcy od rozpoczęcia leczenia.
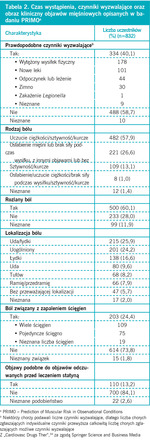
Tabela 2. Czas wystąpienia, czynniki wyzwalające oraz obraz kliniczny objawów mięśniowych opisanych w badaniu PRIMOa
Większość chorych (58,7%) nie potrafiła zidentyfikować żadnego konkretnego czynnika wyzwalającego objawy mięśniowe (tab. 2). Najczęściej odnotowywanymi czynnikami wyzwalającymi były przebyty wytężony wysiłek fizyczny lub zastosowanie nowego leku. Dolegliwości występowały u 60,1% leczonych, z tego 24,2% skarżyła się na ból uogólniony. Ból był częściej zlokalizowany w obrębie kończyn dolnych (w udach i łydkach) niż w obrębie kończyn górnych czy tułowia. Większość chorych (71%) zgłaszała objawy mięśniowe, takie jak uczucie ciężkości, sztywność lub kurcze. U prawie 28% chorych stwierdzono występowanie mialgii podczas wysiłku fizycznego, w tym uczucie osłabienia mięśni lub utratę siły, z obecnością innych objawów (tj. uczucie ciężkości, sztywność, kurcze) lub bez nich.34
Wśród osób z objawami mięśniowymi związanymi ze stosowaniem statyn u 25% stwierdzano ciągły ból mięśniowy, a u 73% ból nawracający. U większości chorych czas trwania dolegliwości wynosił kilka minut lub kilka godzin, a były one niezwiązane lub związane z wysiłkiem. Prawie 40% chorych stosowało leki przeciwbólowe, aby złagodzić ból. Wielu chorym mialgia przeszkadzała w codziennych czynnościach. Choć zaledwie 4% osób z opisanymi dolegliwościami nie mogło wstać z łóżka lub opuściło z tego powodu pracę, to jednak aż 64% uniemożliwiały one wykonanie umiarkowanego (38% osób) lub wytężonego (26% osób) wysiłku. Z powodu wystąpienia mialgii u ok. 57% chorych konieczna była zmiana leczenia hipolipemizującego (głównie na inną statynę lub fibrat), u ok. 20% konieczne było przerwanie leczenia statynami, a u 17% konieczne było zmniejszenie dawki leku.34
Dodatnie wywiady bólu mięśniowego podczas leczenia hipolipemizujacego były najsilniejszym niezależnym czynnikiem ryzyka wystąpienia objawów mięśniowych (iloraz szans [OR] 10,12; 95% CI: 8,23-12,54; p<0,001). W dodatku stosowanie w dużych dawkach zarówno atorwastatyny (p=0,04), jak i simwastatyny (p<0,001) było związane ze znacznie większą częstością wystąpienia objawów mięśniowych w porównaniu ze stosowaniem prawastatyny w dużych dawkach. Natomiast stosowanie fluwastatyny XL wiązało się ze znacznie mniejszym ryzykiem wystąpienia objawów mięśniowych w porównaniu ze stosowaniem prawastatyny (p<0,001).4 Innymi niezależnymi wskaźnikami ryzyka objawów mięśniowych związanych ze stosowaniem statyn w dużych dawkach są: niedoczynność tarczycy, obciążające wywiady zwiększonej aktywności CPK lub niewyjaśnionych kurczy mięśniowych oraz dodatnie wywiady rodzinne w kierunku objawów mięśniowych.34
Z badania PRIMO badacze wyciągnęli kilka ważnych wniosków. Po pierwsze, częstość objawów mięśniowych związanych ze stosowaniem statyn w dużych dawkach oraz ich wpływ na terapię tymi lekami mogą być w badaniach klinicznych opublikowanych przed badaniem PRIMO niedoszacowane. Po drugie, w zoptymalizowaniu leczenia statynami, w tym ustaleniu odpowiedniego dawkowania oraz poprawie przestrzegania planu leczenia przez chorego, lekarzom powinno pomóc zidentyfikowanie silnych czynników ryzyka mialgii związanej ze stosowaniem statyn. Choć w badaniu PRIMO dodatnie wywiady rodzinne bólów mięśniowych podczas leczenia hipolipemizującego miało niewielu chorych, to wykazano, że ten czynnik niemal dwukrotnie zwiększał ryzyko wystąpienia objawów mięśniowych w czasie stosowania statyn. Wyniki te dają nadzieję na zidentyfikowanie określonych genów lub polimorfizmu pojedynczych nukleotydów, których obecność mogłaby zwiększać ryzyko miopatii lub zmniejszyć maksymalną tolerowaną dawkę leku hipolipemizującego. Tego typu informacje mogą w końcu umożliwić dobór dawki leku najwłaściwszej dla danego pacjenta. Choć autorzy badania PRIMO, mając słabe uzasadnienie, zaprzestali rutynowego oznaczania CPK u każdego kandydata do leczenia statynami, to zwiększenie aktywności CPK w przeszłości (miopatia subkliniczna) jest również wskaźnikiem zagrożenia wystąpienia objawów mięśniowych u chorych otrzymujących statyny w dużych dawkach.34
Chorzy, którzy byli bardziej aktywni fizycznie, byli także bardziej narażeni na wystąpienie mialgii, co prawdopodobnie można wytłumaczyć tym, że uszkodzenie mięśni niewielkiego stopnia mogą nasilać statyny.34 W przeciwieństwie do tego, kilka uznanych wcześniej czynników ryzyka,10 w tym zaawansowany wiek (>70 r.ż.) oraz niewydolność nerek, nie prognozowało objawów mięśniowych u uczestników badania PRIMO. Spożycie alkoholu (niewielkie lub umiarkowane), będące dobrze udokumentowanym czynnikiem ryzyka często śmiertelnej rabdomiolizy, nie zwiększało znamiennie ryzyka wystąpienia objawów mięśniowych w tym badaniu.34
Wśród potencjalnych ograniczeń badania było ustalanie związków między leczeniem statynami a mialgią na podstawie chronologii zdarzeń, a nie wszechstronej analizy zależności (np. algorytmu Naranjo). W dodatku nie jest jasne, czy czynniki ryzyka mialgii ustalone w badaniu PRIMO są takie same jak czynniki ryzyka rozwoju rzadkiej, ale potencjalnie śmiertelnej rabdomiolizy. Patofizjologia tych stanów może być różna, a rabdomioliza może występować przy braku objawów mięśniowych.45
Wpływ działań niepożądanych na przestrzeganie przez chorego planu leczenia hipolipemizującego został udokumentowany w kilku innych badaniach. W otwartym badaniu z udziałem 3845 chorych z hiperlipidemią otrzymujących statyny częstość działań niepożądanych ogólnie (23,3% vs 18,2%; p=0,001) oraz samych objawów mięśniowych (6,9% vs 5,2%; p=0,05) była znacznie większa w grupie chorych nieprzestrzegających planu leczenia niż w grupie stosujących się do zaleceń.22 W innym badaniu z udziałem 193 chorych leczonych przynajmniej jednym lekiem hipolipemizującym wykazano odwrotną korelację między zgłaszaniem częstych polekowych działań niepożądanych a przestrzeganiem planu leczenia przez chorego.23 W kilku badaniach kohortowych w ciągu pierwszego roku leczenia stwierdzano przestrzeganie zaleceń (adherence) przez pacjentów w 26-85% z szybkim spadkiem tego odsetka w ciągu kilku pierwszych miesięcy terapii.16-18,21 Nie dziwi to zważywszy, że wielu chorych nie zdaje sobie sprawy z długoterminowych korzyści przewlekłego leczenia, niepowodujących dolegliwości, chorób, którymi są dyslipidemie. Wielu natomiast doświadcza krótkotrwałych mankamentów leczenia statynami (np. polekowe działania niepożądane), które w ich mniemaniu przewyższają korzyści, co prowadzi do załamania realizacji planu leczenia.46
Bez względu na przyczyny suboptymalna realizacja planu leczenia hipolipemizującego prowadzi do zwiększenia ilości zachorowań i zgonów. W West of Scotland Coronary Prevention Study u mężczyzn bez choroby wieńcowej w wywiadach ryzyko zgonu z jakiejkolwiek przyczyny uległo zmniejszeniu o 33% wśród realizujących w co najmniej 75% plan leczenia w porównaniu z osobami przyjmującymi mniej niż 75% przepisanych leków. Ryzyko zawału serca lub zgonu z powodu innych powikłań wieńcowych zostało zredukowane o 38% u osób stosujących się do zaleceń w co najmniej 75%, w porównaniu z redukcją o 31% wśród osób stosujących się do zaleceń w niespełna 75%.47,48 W Lipid Research Clinics Coronary Primary Prevention Trial obniżenie ryzyka powikłań wieńcowych wynosiło 39,3% wśród chorych w pełni realizujących plan leczenia, w porównaniu z redukcją ryzyka o odpowiednio 10,9% i 26,1% wśród chorych realizujących plan leczenia w ok. 25,0% i 50,0%.13,49
Próby kliniczne
Zgodnie z systematycznym przeglądem 21 badań klinicznych, którym objęto wyniki 180 tys. osobolat leczenia statynami lub placebo, mialgia definiowana jako niewielki ból mięśniowy rozwija się u 190 chorych na 100 tys. osobolat; miopatia definiowana jako ból mięśniowy, tkliwość lub osłabienie na tyle silne, że leczony zgłasza się do lekarza lub zaprzestaje przyjmowania statyn, rozwija się u 5 chorych na 100 tys. osobolat; zaś rabdomioliza u 1,6 chorych na 100 tys. osobolat (wszystkie liczby zostały skorygowane w porównaniu ze stosowaniem placebo).31
Na podstawie metaanalizy obejmującej 21 badań i 48 138 pacjentów Kashani i wsp.9 sugerują, że mialgia nie występowała znacząco częściej u osób leczonych statynami w porównaniu z osobami otrzymującymi placebo (względne ryzyko, 0,99; 95% CI: 0,96-1,03). Wśród statyn tylko atorwastatyna powodowała znacząco większe ryzyko mialgii w porównaniu z placebo (5,1% w porównaniu z 1,6%; p=0,04; RD – różnica ryzyka, 1,9%; 95% CI: 2,1%-61,6%). W żadnym z badań nie odnotowano przypadku mialgii w czasie stosowania fluwastatyny w porównaniu z 4 przypadkami wśród otrzymujących placebo (0% w porównaniu z 0,6%; RD –6,4%; 95% CI, –73,1% do 60,2%). Ani zwiększenie aktywności CPK, ani występowanie rabdomiolizy nie było częstsze w grupie stosujących statyny w porównaniu z grupą placebo czy też przy porównywaniu konkretnej statyny z placebo. Podczas stosowania rosuwastatyny częściej obserwowano mialgię oraz zwiększenie aktywności CPK w porównaniu z placebo, ale mała liczba chorych leczonych rosuwastatyną powoduje, że analiza statystyczna ma małą moc i nie można wykluczyć statystycznie istotnego błędu.

Tabela 3. Działania niepożądane oraz uszkodzenia mięśni podczas stosowania statyn: metaanaliza 18 badań obejmująca 301 374 osobolata
Niedawna metaanaliza pomogła w ocenie stosunku ryzyka do korzyści podczas stosowania statyn z uwzględnieniem ryzyka bezwzględnego (tab. 3).50 W analizie obejmującej 18 badań (n=71 108; 301 374 osobolat) w grupie leczonych statynami stwierdzono 316 zdarzeń mięśniowych, na które składały się mialgia, miopatia lub astenia, w porównaniu z 253 w grupie otrzymujących placebo (p<0,001) i 81 przypadków zwiększenia aktywności CPK w grupie leczonych statynami w porównaniu z 64 przypadkami w grupie otrzymujących placebo (p=0,001).50 Rabdomiolizę odnotowano u 9 chorych leczonych simwastatyną, u chorego leczonego lowastatyną i u 5 chorych otrzymujących placebo. Dane te wskazują, że liczba osób, która musi być leczona statynami, aby doszło do przypadku poważnych powikłań ze strony mięśni [NNH – przyp. red.], wynosi 3400; czyli aby zaobserwować 1 przypadek rabdomiolizy lub dziesięciokrotnego zwiększenia aktywności CPK powyżej górnej granicy normy, należy leczyć statynami 3400 chorych. Liczba chorych, których należy leczyć, aby osiągnąć korzyść u jednego z nich, innymi słowy liczba chorych, których należy leczyć statyną, aby zapobiec wystąpieniu jednego zawału serca, rewaskularyzacji, udaru, zgonu z przyczyn sercowo-naczyniowych lub z jakiejkolwiek przyczyny [NNT – przyp. red.] wynosiła 27. Stosunek bezwzględnego ryzyka do korzyści wynosił zatem około 126:1.
Stosowanie fluwastatyny, prawastatyny oraz simwastatyny było związane z wyraźnie rzadszym występowaniem mialgii niż stosowanie atorwastatyny (OR 0,28; 95% CI: 0,18-0,44; p<0,001 dla fluwastatyny w porównaniu z atorwastatyną; OR 0,43; 95% CI: 0,36-0,51; p<0,001 dla prawastatyny w porównaniu z atorwastatyną; OR 0,23; 95% CI: 0,19-0,28; p<0,001 dla simwastatyny w porównaniu z atorwastatyną). Prawastatyna w porównaniu z simwastatyną również rzadziej powoduje mialgię (OR 0,53; 95% CI: 0,44-0,65; p<0,001).50 Opisana metaanaliza dotyczyła jednak bardzo wyselekcjonowanej grupy chorych, a wyniki mogą zależeć od reprezentacji statyn we włączonych do niej badaniach.
Porejestracyjne monitorowanie działań niepożądanych
Baza danych działań niepożądanych FDA dostarczyła informacji, że na milion recept na statyny częstość miopatii waha się od 0,3 do 2,2, a częstości rabdomiolizy od 0,3 do 13,5.30 Śmiertelność z powodu rabdomiolizy związanej ze stosowaniem statyn jest niezmiernie rzadka; powikłanie to jest przyczyną mniej niż 1 zgonu na milion recept.51 Od momentu wprowadzenia na rynek każdej ze statyn do maja 2001 r. odnotowano 1 przypadek zgonu z powodu rabdomiolizy na 23,4 miliona recept na atorwastatynę, 27,1 miliona recept na prawastatynę oraz 8,3 miliona recept na simwastatynę.51 Ani w piśmiennictwie, ani w danych z bazy FDA nie ma żadnego przypadku zgonu z powodu rabdomiolizy w czasie stosowania fluwastatyny od momentu wprowadzenia jej na rynek w 1993 r. do maja 2001 r., tj. w czasie, w którym przepisano ponad 37 milionów recept na ten lek.51
Zgłaszanie działań niepożądanych do bazy danych FDA nie jest obowiązkowe, co może skutkować zaniżeniem ich liczby oraz błędami raportowania, takimi jak efekt oddziaływania rozgłosu medialnego na rozpoznawanie powikłań polekowych, relacjonowanie efektów nowych leków czy długookresowych trendów w raportowaniu działań niepożądanych.30