Badania laboratoryjne
W kilka godzin po ekspozycji obserwuje się przemijającą leukocytozę z neutrofilią i limfocytopenią, niekiedy także z eozynofilią.33 Choć często stwierdzane jest u chorych na alergiczne zapalenie pęcherzyków płucnych zwiększenie innych markerów zapalenia, takie jak OB, CRP, LDH, immunoglobuliny IgG lub IgM, to jednak nie są to zmiany swoiste. Zwykle w surowicy można wykryć precypityny z klasy IgG skierowane przeciwko antygenom, na które chory jest wrażliwy.34 Stwierdzenie tych przeciwciał jest jednym z głównych kryteriów choroby, ale obecne są także u osób jedynie narażonych na dany antygen, które nie zgłaszają żadnych objawów choroby.35 Precypityny można wykryć w surowicy przez wiele lat po zaprzestaniu ekspozycji i nie są patognomoniczne dla tej choroby. Tradycyjne techniki precypitacji coraz częściej zastępowane są bardziej wiarygodnymi, powtarzalnymi, swoistymi i prostszymi testami immunoenzymatycznymi.36 Są one jednak mniej czułe, a dostępne komercyjnie testy służące do badań przesiewowych w kierunku AZPP często dają fałszywie ujemne wyniki, gdyż wykrywają przeciwciała skierowane tylko przeciwko określonym antygenom. U chorych z potwierdzoną w próbie prowokacyjnej reakcją na dany antygen nie zawsze stwierdza się swoiste przeciwciała w surowicy, a wśród osób z rozpoznaniem ustalonym na podstawie oceny histologicznej materiału uzyskanego z biopsji płuca aż u 40% nie udaje się określić antygenu odpowiedzialnego za powstanie choroby.37 Choć opisywano dodatnie wyniki testów skórnych ze swoistymi antygenami (późna reakcja po 72 h), to z powodu braku komercyjnych zestawów nie są one wykorzystywane w praktyce klinicznej.2 Czułą i swoistą metodą jest oznaczanie przeciwciał skierowanych przeciwko immunoglobulinie IgA i składnikowi P2 antygenów gołębi techniką immunoelektrodyfuzji.38 Trudno przewidzieć, na ile przydatne w diagnostyce AZPP okażą się metody molekularne, które pozwalają wykryć materiał genetyczny mikroorganizmów powodujących chorobę, np. grzybów czy promieniowców.39
Badania obrazowe
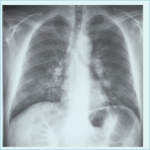
Rycina 1. Zdjęcie przeglądowe klatki piersiowej w projekcji tylno-przedniej chorego na płuco hodowców ptaków...
Klasyczne zdjęcie radiologiczne płuc nie jest czułą metodą w diagnostyce alergicznego zapalenia pęcherzyków płucnych.40 W ostrych postaciach obserwuje się przemijające zagęszczenia miąższowe lub rozlane ogniska szkła mlecznego. Dla podostrych postaci najbardziej typowe są niewielkie guzki lub zmiany siateczkowo-guzkowe z obszarami szkła mlecznego (ryc. 1), a w przewlekłej dominują zmiany siateczkowe z obrazem plastra miodu.
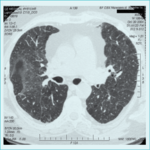
Rycina 2. Tomografia komputerowa o wysokiej rozdzielczości chorego na alergiczne zapalenie pęcherzyków płucnych (AZPP)...
Znacznie większą czułość w wykrywaniu zmian typowych dla AZPP wykazuje tomografia komputerowa o wysokiej rozdzielczości (HRCT).41 Zmiany w obrazie HRCT, podobnie jak na zdjęciu klasycznym, są różne w zależności od postaci choroby i nie są one patognomoniczne dla AZPP. W ostrej postaci najbardziej typowe są ogniska szkła mlecznego, zlokalizowane głównie w środkowo-dolnych polach płuc. W postaci podostrej widoczny jest obraz mozaiki: małe, słabo odgraniczone guzki, ogniska szkła mlecznego i pułapka powietrza (szczególnie dobrze widoczna w fazie wydechu).42 Trudno odróżnić zmiany w ostrej i podostrej postaci od tych, jakie obserwuje się w złuszczającym śródmiąższowym zapaleniu płuc.43 Śródzrazikowe guzki, ogniska szkła mlecznego i pułapki powietrza są szczególnie charakterystyczne dla AZPP (ryc. 2).42
W przewlekłych postaciach mogą występować zmiany siateczkowe o typie włóknienia i ogniska plastra miodu.44 Nieregularne włóknienie płuc, rozstrzenie oskrzeli z pociągania i obraz plastra miodu przypominają zmiany w przebiegu samoistnego włóknienia płuc, choć u chorych na AZPP zwykle oszczędzone są przypodstawne obszary płuc.43 W płucu farmera obserwowano także zmiany rozedmowe.45 W przebiegu choroby stosunkowo często obraz radiologiczny (także HRCT) może być prawidłowy,46,47 a nasilenie zmian radiologicznych nie jest czynnikiem rokowniczym.45 Dla AZPP nietypowe jest powiększenie węzłów chłonnych wnęk lub śródpiersia oraz wysięk w jamie opłucnowej. Badania scyntygraficzne, rezonans magnetyczny i pozytonowa emisyjna tomografia nie znalazły zastosowania w diagnostyce tej choroby.
Badania czynnościowe
Wyniki badań czynnościowych układu oddechowego nie są charakterystyczne dla alergicznego zapalenia pęcherzyków płucnych i są podobne do tych, jakie stwierdza się w przebiegu innych chorób śródmiąższowych płuc. U wielu chorych, zwłaszcza z ostrą postacią, wyniki badań czynnościowych płuc poza okresem ekspozycji na alergen są prawidłowe. W postaci przewlekłej z narastającym włóknieniem płuc obserwuje się restrykcyjny typ zaburzeń wentylacji ze zmniejszeniem pojemności życiowej i całkowitej pojemności płuc.48 U niektórych chorych po ekspozycji na alergen stwierdzano obturację oskrzeli, ze zmniejszeniem wskaźnika FEV1/VC i zwiększeniem objętości zalegającej.49 Z tego względu u chorych na AZPP możliwe jest występowanie zaburzeń zarówno restrykcyjnych (u chorych z włóknieniem płuc), obturacyjnych (u chorych z rozedmą), jak i mieszanych. Często obserwuje się zmniejszenie zdolności dyfuzyjnej płuc dla tlenku węgla.48 Ocena wymiany gazowej wykazuje, początkowo po wysiłku i w miarę postępu choroby także w spoczynku, hipoksemię oraz zwiększony gradient pęcherzykowo-tętniczy tlenu.50 Narastające włóknienie płuc powoduje wzrost ich sprężystości mierzony zmniejszeniem podatności.51 Badanie wysiłkowe po ekspozycji wskazuje na zmniejszenie rezerwy oddechowej oraz zwiększenie czynnościowej przestrzeni martwej i gradientu pęcherzykowo-tętniczego tlenu.52
Płukanie oskrzelowo-pęcherzykowe
Dla alergicznego zapalenia pęcherzyków płucnych charakterystyczny jest znaczący wzrost odsetka limfocytów (>50%) w płynie z płukania oskrzelowo-pęcherzykowego (BALF).53 Skład komórkowy BALF zmienia się w zależności od czasu, jaki upłynął od ekspozycji na antygen, co wykorzystuje się w diagnostyce różnicowej. Zwiększony odsetek limfocytów w BALF obserwuje się u bezobjawowych osób narażonych na antygeny organiczne.54 Kilka godzin po ekspozycji na antygen w BALF przeważają neutrofile i obecne są także plazmocyty oraz mastocyty.55 Limfocyty wzrastają w BALF znacząco po 48 h od narażenia na antygen. Opisywane przed laty zmniejszenie stosunku limfocytów CD4+/CD8+ <156 nie jest już uważane za charakterystyczne dla AZPP.57 Wykazano, że w przewlekłych postaciach choroby, u palaczy, w przypadkach spowodowanych ekspozycją na Mycobacterium avium dochodzi do zwiększenia stosunku CD4+/CD8+.57,58 Nie obserwowano też zmian stosunku CD4+/CD8+ u dzieci chorych na AZPP.59 W zaawansowanych postaciach przewlekłych z dużym włóknieniem płuc zwiększa się odsetek neutrofilów w BALF.60
Podejmowane są próby zastąpienia BAL mniej inwazyjną oceną składu komórkowego w indukowanej plwocinie. Wykazano wprawdzie dużą korelację wyników uzyskanych z BALF i plwociny indukowanej,61 ale metoda ta nie jest jeszcze zalecana w rutynowej diagnostyce chorób śródmiąższowych płuc.
Obraz histopatologiczny
Niewiele jest danych dotyczących zmian morfologicznych w ostrej postaci choroby, która charakteryzuje się naciekiem śródmiąższa głównie przez neutrofile, limfocyty, plazmocyty, wypełnieniem przestrzeni pęcherzykowych i dystalnych dróg oddechowych bezpostaciowym białkowym wysiękiem, obrzękiem lub krwawieniem.62 W postaciach podostrych i przewlekłych typowe jest ziarniniakowe zapalenie pęcherzyków płucnych z charakterystyczną triadą zmian: zapalenie oskrzelików, limfocytarny naciek śródmiąższowy i nieserowaciejące ziarniniaki.63 Podostrą fazę charakteryzuje śródmiąższowy naciek limfocytarny ze słabo odgraniczonymi ziarniniakami oraz naciek z komórek jednojądrowych. W przewlekłej postaci widoczne są ziarniniaki, limfocytarne śródmiąższowe zapalenie pęcherzyków płucnych, zarostowe zapalenie oskrzelików, włóknienie i obraz plastra miodu.64 Stopień włóknienia w śródmiąższu jest bardzo zróżnicowany. Poszczególne typy mogą nieco różnić się morfologicznie. Przykładowo w płucu hodowców gołębi dominują małe, słabo zróżnicowane guzki w śródmiąższu, podczas gdy w płucu farmera widoczne są zmiany proliferacyjne o typie zarostowego zapalenia oskrzelików, zapalenie okołooskrzelikowe i włóknienie płuc.65 Niekiedy widoczne są obszary zmian typowych dla skrytopochodnego organizującego się zapalenia płuc (COP – cryptogenic organizing pneumonia)65 lub nieswoistego śródmiąższowego zapalenia płuc (NSIP – non-specific interstitial pneumonia).66 Tak wielka różnorodność zmian morfologicznych powoduje, że biopsje płuc przezoskrzelowe lub przez ścianę klatki piersiowej nie są dobrą metodą diagnostyczną i konieczne jest wykonywanie otwartej biopsji, z pobraniem kilku wycinków.
Kryteria rozpoznania

Tabela 2. Rozpoznawanie alergicznego zapalenia pęcherzyków płucnych (AZPP) na podstawie kryteriów klinicznych (Schuyler...
Ustalenie rozpoznania alergicznego zapalenia pęcherzyków płucnych jest trudne, gdyż nie określono precyzyjnych kryteriów diagnostycznych. Konieczna jest kompleksowa ocena kliniczna, laboratoryjna, radiologiczna, czynnościowa, środowiskowa i morfologiczna.67 Bardzo istotny jest wywiad określający szczegółowo potencjalne narażenie w pracy lub w domu na organiczne antygeny. Swoiste przeciwciała czy limfocytoza w BALF u bezobjawowych osób narażonych na kontakt z antygenem nie powodują niekorzystnych odległych skutków, a tym bardziej nie są wystarczającymi przesłankami do rozpoznania choroby.68,69 Rozpoznanie opiera się na stwierdzeniu określonych kryteriów dla poszczególnych postaci choroby. W ostrej postaci kluczowe są: stwierdzenie ekspozycji na alergen, występowanie grypopodobnych objawów w kilka godzin po ekspozycji, wykrycie swoistych przeciwciał, zwiększenie odsetka limfocytów i neutrofilów w BALF, poprawa po zaprzestaniu ekspozycji oraz pogorszenie po ponownych kontaktach z antygenem.70 Podostrą postać rozpoznajemy na podstawie wykazania przyczynowo-skutkowych związków występowania objawów z ekspozycją na alergen organiczny, wykrycia swoistych precypityn w surowicy, znacznego odsetka limfocytów w BALF, stwierdzenia rozlanych mikroguzków, pułapek powietrza i ognisk „szkła mlecznego” w obrazie HRCT. Przewlekła postać może przypominać samoistne włóknienie płuc (IPF) lub zaawansowane stadia innych śródmiąższowych chorób płuc. W tych przypadkach ustalenie rozpoznania jest najtrudniejsze. Oprócz kryteriów stosowanych w rozpoznaniu podostrej postaci choroby wykorzystuje się jeszcze otwartą biopsję płuca71 oraz środowiskowy lub laboratoryjny test prowokacji z podejrzanym antygenem.72 Za rozpoznaniem AZPP przemawia gorączka i pogorszenie czynnościowe płuc w kilka godzin po prowokacji. Można również stwierdzić zmiany radiologiczne i zaburzenia w składzie komórkowym w BALF. Najbardziej charakterystyczne dla AZPP jest: narażenie na antygen wywołujący chorobę, wykrycie swoistych przeciwciał precypitujących, występowanie objawów 4-8 h po ekspozycji, chudnięcie i trzeszczenia wdechowe.67 Chorobę można rozpoznać również, jeśli spełnione są cztery duże i dwa małe kryteria diagnostyczne (tab. 2).70
Diagnostyka różnicowa
Alergiczne zapalenie pęcherzyków płucnych może upodabniać się do wielu schorzeń układu oddechowego, szczególnie chorób śródmiąższowych płuc, zakażeń i innych chorób oskrzeli. Trudne jest różnicowanie podostrej postaci z sarkoidozą, a przewlekłej z IPF, NSIP, COP i limfoidalnym śródmiąższowym zapaleniem płuc (LIP).73 Uwzględnić trzeba również inne śródmiąższowe choroby płuc, szczególnie zmiany polekowe, pylice, zmiany płucne w przebiegu chorób tkanki łącznej, a także ziarniniakowe choroby zakaźne (np. gruźlica, histoplazmoza).74 W ostrej postaci często rozpoznaje się błędnie zakażenie układu oddechowego, a ustępowanie objawów po zaprzestaniu ekspozycji na antygen przypisuje się antybiotykoterapii. Trudność może sprawić odróżnienie reakcji alergicznej na pyły organiczne od toksycznej spowodowanej działaniem bakteryjnych endotoksyn lub toksyn grzybiczych.75 W reakcjach toksycznych nie stwierdza się swoistych przeciwciał, zwykle nie są widoczne zmiany radiologiczne w płucach.11

