Farmakologiczne leczenie astmy
Christopher H. Fanta, MD
Wyniki badań, w których rozpoznanie ustalano na podstawie badania lekarskiego, wskazują, że na astmę choruje ok. 7% Amerykanów.1,2 Choroba ta występuje u ludzi wszystkich ras i grup etnicznych na całym świecie, od wieku dziecięcego do starości, i nieznacznie częściej u chłopców niż dziewczynek, a po okresie pokwitania częściej u kobiet niż mężczyzn. W ostatnich dekadach obserwuje się dramatyczny wzrost częstości występowania atopii i astmy w krajach zachodnich,3 a ostatnio również w krajach rozwijających się.4 Ocenia się, że na całym świecie na astmę choruje aż 300 mln ludzi.5
W Stanach Zjednoczonych liczba ciężkich zaostrzeń astmy (określanych jako wizyty w ośrodkach pomocy doraźnej i hospitalizacje z powodu astmy) oraz zgonów z powodu tej choroby gwałtownie wzrosła w latach 70. i 80. XX w. Najnowsze dane wskazują natomiast, że mimo dużej częstości występowania choroby wyniki leczenia są coraz lepsze: zmniejsza się roczna liczba hospitalizacji z powodu napadów astmy oraz zgonów spowodowanych tą chorobą.6 Na tendencję tę wpływa prawdopodobnie m.in. coraz powszechniejsze prewencyjne stosowanie wziewnych kortykosteroidów i wprowadzenie w ostatnich 10-15 latach nowych leków o dużej skuteczności oraz nowych udoskonalonych postaci leków stosowanych w terapii astmy.
Obturacja oskrzeli w astmie i wynikające z niej objawy: kaszel, duszność, ucisk w klatce piersiowej i świsty, spowodowane są współwystępowaniem skurczu mięśni gładkich dróg oddechowych i zapalenia oskrzeli. Skurcz oskrzeli może mieć ciężki przebieg i prowadzić do zagrażającego życiu zwężenia i zamknięcia dróg oddechowych, nawet bez towarzyszącego zatkania przez czopy śluzu. Do zjawiska tego przyczyniają się nadmierna kurczliwość mięśni gładkich7 i ich zwiększona masa.8 Objawami zapalenia dróg oddechowych w astmie są: obrzęk błony śluzowej, podśluzowej i przydanki; naciek komórkowy składający się głównie z eozynofili (a w niektórych przypadkach neutrofili) i komórek tucznych oraz aktywowanych limfocytów pomocniczych T,9 które (w odróżnieniu od komórek tucznych w innych eozynofilowych chorobach oskrzeli) naciekają pęczki mięśni gładkich;10 zwiększona produkcja wydzieliny w drogach oddechowych, w której znajduje się śluz, złuszczone komórki wyściełające drogi oddechowe oraz eozynofile; wzrost łożyska naczyń włosowatych; przerost mięśni gładkich, a także odkładanie nadmiaru kolagenu, szczególnie bezpośrednio pod błoną podstawną nabłonka.11,12
Leki stosowane w terapii astmy tradycyjnie były klasyfikowane w zależności od głównego mechanizmu działania, którym był rozkurcz mięśni gładkich oskrzeli (leki rozszerzające oskrzela) lub zwalczanie zapalenia dróg oddechowych (leki przeciwzapalne). Nowe leki (np. leki przeciwleukotrienowe) i połączenia leków (np. kortykosteroidy wziewne i długodziałający agoniści receptorów adrenergicznych β) mają podwójne działanie i nie poddają się temu tradycyjnemu dychotomicznemu podziałowi. Aktualna klasyfikacja leków przeciwastmatycznych uwzględnia ich rolę w całościowym leczeniu astmy (leczenie doraźne lub długotrwała kontrola). Model ten jest szczególnie przydatny w rozmowie z pacjentami na temat leków stosowanych w terapii choroby.
Wszyscy chorzy na astmę powinni mieć przy sobie szybkodziałający lek rozszerzający oskrzela, który mogliby stosować w razie potrzeby. W konsensusach zaleca się, aby w przypadkach, gdy szybkodziałające leki rozkurczowe stosowane są w celu opanowania objawów astmy częściej niż 2 razy w tygodniu (lub częściej niż 2 razy w miesiącu z powodu nocnych objawów astmy wybudzających ze snu), stosować leki kontrolujące przebieg choroby.2,13
Leczenie doraźne
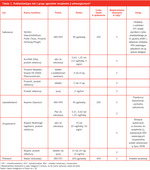
Najskuteczniejszą terapię, która umożliwia szybkie zniesienie obturacji oskrzeli i ustąpienie objawów astmatycznych, zapewniają szybkodziałające leki z grupy agonistów receptorów adrenergicznych β podawane drogą wziewną. Najczęściej stosuje się krótkodziałające leki z grupy agonistów receptorów β2 [nazywane również β2-mimetykami – przyp. tłum.], do których należą: salbutamol (w USA nazywany albuterolem), lewosalbutamol [lewalbuterol niezarejestrowany w Polsce – przyp. red.] i pirbuterol [niezarejestrowany w Polsce – przyp. red.] (tab. 1). Orcyprenalina (metaproterenol) w postaci inhalatora ciśnieniowego z dozownikiem niedawno została wycofana z amerykańskiego rynku [w Polsce orcyprenalina nie jest dostępna w postaciach parenteralnych – przyp. red.].
Krótkodziałające β-mimetyki zaczynają działać najpóźniej po 5 minutach od podania, efekt maksymalny uzyskuje się po 30-60 minutach, a całkowity czas działania wynosi od 4 do 6 godzin.14 Regularne stosowanie leku rozszerzającego oskrzela (co najmniej 4 razy dziennie) nie zmniejsza jego skuteczności (mierzonej zmianą maksymalnego przepływu wydechowego), ale powoduje niewielkie skrócenie czasu działania.15,16 Udowodniono, że regularne stosowanie tych leków 4 razy dziennie w porównaniu z ich podawaniem w razie potrzeby17 nie poprawia wyników leczenia (a u pacjentów z pewnymi wariantami genotypu receptora β może mieć nawet działanie niekorzystne)18,19 i dlatego krótkodziałające β-mimetyki zaleca się przyjmować tylko w razie potrzeby, aby doraźnie zmniejszyć objawy astmy, lub przed przewidywaną ekspozycją na znane czynniki wywołujące reakcję astmatyczną, a szczególnie przed wysiłkiem. Za zbędne uznano stosowanie krótkodziałającego β-mimetyku przed podaniem wziewnego kortykosteroidu zalecane w celu zwiększenia dystrybucji kortykosteroidu do dolnych dróg oddechowych.20 Nie ma również potrzeby zachowania 10-15-sekundowego odstępu między kolejnymi inhalacjami, jeśli zalecana dawka jednorazowa wynosi dwa lub więcej wdechów.21
Stwierdzono, że u chorych z umiarkowaną bądź ciężką obturacją oskrzeli wykres zależności dawka–efekt rozkurczu oskrzeli przy podawaniu bardzo dużych dawek krótkodziałającego β-mimetyku (do 4000 μg salbutamolu z inhalatora ciśnieniowego z dozownikiem) przybiera postać krzywej logarytmicznej. Często występują zależne od dawki działania niepożądane typu sympatykomimetycznego, takie jak: drżenie, niepokój, kołatanie serca i tachykardia (ale nie nadciśnienie), a w surowicy stwierdza się niewielkie, ale wykrywalne zmniejszenie stężenia potasu i magnezu. Przy stosowaniu zwykłych dawek (dwie dawki wziewne przy jednym podaniu) objawy niepożądane występują jednak rzadko. Leki rozszerzające oskrzela z grupy β-mimetyków nie są przeciwwskazane u pacjentów przyjmujących jednocześnie β-adrenolityki, choć skuteczność ich działania może być nieco mniejsza.22,23
Decyzja o wyborze jednego z wielu dostępnych krótkodziałających agonistów receptorów β-adrenergicznych w dużej mierze opiera się na kosztach oraz preferencjach pacjenta i lekarza. Jedynym lekiem dostępnym w USA w postaci inhalatora proszkowego jest pirbuterol [w Polsce: salbutamol – przyp. red.]. Zastosowanie tego urządzenia pozwala na optymalną dystrybucję leku, gdyż dawka uwalniana jest z inhalatora dopiero po rozpoczęciu wdechu przez pacjenta. W celu wyeliminowania działań niepożądanych, które – jak twierdzą niektórzy badacze – towarzyszą wyłącznie podaniu lewoskrętnego izomeru salbutamolu, wprowadzono do lecznictwa prawoskrętny izomer, lewosalbutamol (lewalbuterol).24 Okazało się jednak, że lewosalbutamol podawany za pomocą inhalatora ciśnieniowego z dozownikiem ma taki sam profil skuteczności i działań niepożądanych jak mieszanina racemiczna cząsteczek w salbutamolu.25 Salbutamol dostępny jest w postaci inhalatorów niezawierających chlorofluorokarbonów (CFC), natomiast inhalatory, które je zawierają, zostały wycofane z rynku z dniem 31 grudnia 2008 r.26 Alternatywny nośnik, hydrofluoroalkan (HFA) jest, podobnie jak CFC, gazem obojętnym dla dróg oddechowych, ale w odróżnieniu od nich nie powoduje zmniejszenia warstwy ozonowej w stratosferze. Więcej informacji o inhalatorach zawierających HFA można znaleźć w załączniku „Supplementary Appendix” dostępnym z pełną wersją tego artykułu na stronie internetowej NEJM.org. Materiał wideo, dostępny także pod adresem NEJM.org wraz z artykułem Hendelesa i wsp.,26 zawiera prezentację stosowania salbutamolu w postaci inhalatora typu HFA. Inhalatory typu HFA są równoważne w stosunku do inhalatorów z nośnikiem CFC,27 mogą być używane z zaopatrzonymi w zastawki komorami do inhalacji (spejserami) stosowanymi u pacjentów, którzy mają problem z prawidłowym wykonaniem inhalacji,28 i powodują rozkurcz oskrzeli podobny do tego uzyskanego po zastosowaniu salbutamolu w nebulizacji, pod warunkiem podania wystarczającej liczby dawek wziewnych i dobrej techniki inhalacji.29
Nie należy zalecać stosowania krótkodziałających agonistów receptorów β w postaci tabletek lub roztworu do stosowania doustnego, mimo że wydają się wygodne do aplikacji (szczególnie u bardzo małych dzieci). Początek ich działania następuje później, wykazują mniejszą siłę działania i w porównaniu z wziewnymi β-mimetykami częściej wywołują działania niepożądane.30 Do doraźnego leczenia objawów astmatycznych nie zaleca się również leków cholinolitycznych rozszerzających oskrzela, np. ipratropiumu (nie są one też zarejestrowane przez amerykańską Food and Drug Administration – FDA). Początek ich działania następuje później (po 20-30 min) i powodują słabszy efekt rozkurczowy niż wziewne leki z grupy agonistów receptorów β.31 Leki cholinolityczne należy stosować w tych rzadkich przypadkach, gdy pacjent nie toleruje żadnych leków rozkurczowych z grupy β-mimetyków, lub w leczeniu ciężkich napadów astmy32 bądź napadów astmy wywołanych β-adrenolitykami.2
Innowacyjne podejście do leczenia astmy, niewprowadzone jeszcze w USA, polega na połączeniu krótkodziałającego β-mimetyku z wziewnym kortykosteroidem w jednym inhalatorze, którego używa się na żądanie w przypadku nasilenia objawów. Wykazano, że wyniki leczenia z zastosowaniem tego urządzenia u chorych na astmę łagodną były lepsze niż doraźnego podania samego salbutamolu.33 W podobny sposób używa się połączenia w jednym inhalatorze długodziałającego β-mimetyku o szybkim początku działania (formoterol) z kortykosteroidem wziewnym zarówno do leczenia przewlekłego, jak i doraźnego.34,35 Bezpieczeństwo takiej metody terapii musi zostać potwierdzone w dużej i zróżnicowanej populacji chorych na astmę.
Przewlekła kontrola astmy
Warunkiem osiągnięcia dobrej długotrwałej kontroli astmy (rzadkie występowanie objawów astmatycznych, niezaburzony poziom funkcjonowania, prawidłowe lub nieznacznie odbiegające od normy parametry czynnościowe płuc, rzadko występujące napady astmy wymagające leczenia w ośrodku pomocy doraźnej) jest wielokierunkowe podejście uwzględniające: unikanie czynników środowiskowych, które mogą prowokować skurcz oskrzeli oraz ostre i przewlekłe zapalenie oskrzeli, kontrolowanie zmian aktywności choroby, a w niektórych przypadkach – immunoterapia i leczenie farmakologiczne. Dawki leków kontrolujących przebieg choroby powinny być zwiększane do momentu uzyskania dobrej kontroli, m.in. zmniejszenia częstości napadów astmatycznych wymagających podawania kortykosteroidów ogólnoustrojowo do mniej niż jednego epizodu rocznie. Grupą leków, które w największym stopniu przyczyniają się do osiągnięcia dobrej kontroli astmy, są kortykosteroidy wziewne.
Kortykosteroidy wziewne
Kortykosteroidy ze względu na swoje wielokierunkowe działanie przeciwzapalne, w tym znaczny wpływ na transkrypcję licznych genów (zarówno poprzez ich aktywację, jak i inaktywację), okazały się skutecznymi lekami w leczeniu astmy i wielu innych chorób o podłożu zapalnym.36,37 Po zbadaniu wycinków pobranych z oskrzeli chorych na astmę, którzy przewlekle stosowali kortykosteroidy, stwierdzono ustępowanie zmian histologicznych charakterystycznych dla astmy. Obejmowały one zmniejszenie liczby komórek tucznych, eozynofili, limfocytów T oraz komórek dendrytycznych w błonie śluzowej i podśluzowej,38 redukcję hiperplazji komórek sygnetowatych i cech uszkodzenia komórek nabłonka,39 a także zmniejszenie sieci naczyniowej.40
Zahamowaniu zapalenia dróg oddechowych typowo towarzyszy dwu-, a nawet czterokrotne zmniejszenie nieswoistej nadreaktywności oskrzeli.41 Pozytywnym klinicznym wykładnikiem tych zmian jest złagodzenie objawów astmy, poprawa czynności układu oddechowego, poprawa jakości życia u chorych na astmę i zmniejszenie liczby zaostrzeń astmy, w tym ciężkich napadów, które prowadzą do hospitalizacji42 lub zgonu.43 W przeciwieństwie do tych optymistycznych doniesień nie ma wystarczających dowodów na to, że długotrwałe stosowanie kortykosteroidów wziewnych może zapobiec postępującemu pogorszeniu czynności płuc obserwowanemu u części chorych na astmę.44,45 Stosowanie steroidów wziewnych tłumi zapalenie w przebiegu astmy, ale go nie leczy. Po blisko dwóch tygodniach od zaprzestania podawania kortykosteroidów wziewnych u chorych w stabilnym okresie choroby dochodzi do nawrotu wskaźników zapalenia dróg oddechowych (np. stężenie tlenku azotu w wydychanym powietrzu, eozynofilia plwociny) i nadreaktywności oskrzeli do poziomu wyjściowego.46,47