Program edukacyjny: choroby płuc
Rozpoznawanie śródmiąższowych chorób płuc
Jay H. Ryu,1, MD Craig E. Daniels,1 MD, Thomas E. Hartman,2 MD, Eunhee S. Yi,3 MD
W SKRÓCIE
Śródmiąższowe choroby płuc to heterogenna grupa chorób miąższu płucnego, które można podzielić na jednostki o znanej i nieznanej etiologii. W ostatnich latach pojawiło się sporo zmian dotyczących zarówno ich definicji, jak i sposobów rozpoznawania. Co prawda opisano ponad sto różnych jednostek, ale z klinicznego punktu widzenia największe znaczenie ma kilka podstawowych chorób, takich jak samoistne włóknienie płuc, sarkoidoza oraz choroby śródmiąższowe związane z układowymi chorobami tkanki łącznej. Po ustaleniu wstępnego rozpoznania choroby śródmiąższowej lekarz powinien spróbować określić przyczynę zaburzeń lub zespołu objawów klinicznych. Wstępnych informacji na temat możliwych przyczyn choroby może dostarczyć dokładne badanie kliniczne i analiza wyników badań obrazowych. Niezmiernie przydatnym narzędziem diagnostycznym jest tomografia komputerowa wysokiej rozdzielczości klatki piersiowej. W części przypadków rozpoznanie o dużej dozie prawdopodobieństwa może być ustalone na podstawie łącznej analizy obrazu tomografii komputerowej wysokiej rozdzielczości i danych klinicznych. U części chorych przydatne mogą być również badania serologiczne. Często do ustalenia ostatecznego rozpoznania konieczne jest badanie histopatologiczne wycinków pobranych podczas bronchoskopii lub chirurgicznej biopsji płuca. Ocena rokowania oraz wybór najodpowiedniejszej metody leczenia są uzależnione przede wszystkim od właściwego rozpoznania. Dzięki postępowi w zakresie zrozumienia przyczyn i patomechanizmów śródmiąższowych chorób płuc ustalenie właściwego rozpoznania stało się nieco łatwiejsze.
Śródmiąższowe choroby płuc (ILDs – interstitial lung diseases), określane również mianem rozsianych zmian naciekowych, to heterogenna grupa chorób, których wspólną cechą jest objęcie procesem chorobowym przede wszystkim miąższu płucnego. Poszczególne jednostki chorobowe mogą się istotnie różnić etiologią, obrazem klinicznym, radiologicznym, histopatologicznym oraz przebiegiem.1-4 W większości przypadków choroby śródmiąższowe dotyczą osób dorosłych, jednak niektóre z nich, np. alergiczne zapalenie pęcherzyków płucnych i samoistne śródmiąższowe zapalenie płuc, spotyka się również u dzieci.5 Charakterystyczną cechą tych chorób jest naciekanie tkanki śródmiąższowej płuc materiałem komórkowym i bezkomórkowym. Z anatomicznego punktu widzenia zmiany chorobowe mogą dotyczyć nie tylko tkanki śródmiąższowej, ale również przestrzeni pęcherzykowej, naczyń krwionośnych oraz końcowej części dróg oddechowych.1-6 Mimo dokładnego opisania zmian histopatologicznych i ustalonej definicji śródmiąższowej choroby płuc różnicowanie pomiędzy poszczególnymi chorobami śródmiąższowymi oraz innymi chorobami płuc może niekiedy być bardzo trudne. Najistotniejszym następstwem śródmiąższowej choroby płuc są zaburzenia wymiany gazowej. Progresja zmian śródmiąższowych może zatem prowadzić do pogłębiającej się niewydolności oddechowej, a w konsekwencji do zgonu.
Podział śródmiąższowych chorób płuc
Jak dotąd nie opracowano powszechnie akceptowanego schematu podziału śródmiąższowych chorób płuc. Istnieje kilka propozycji klasyfikacji tych chorób, które opierają się na parametrach klinicznych (np. przebieg ostry v. przewlekły), charakterze zmian histopatologicznych, obrazie radiologicznym oraz odpowiedzi na terapię glikokortykosteroidami (jednostki chorobowe reagujące lub niereagujące na podanie leków tej grupy). Wydaje się, że z praktycznego punktu widzenia dla lekarzy najprzydatniejszym podziałem śródmiąższowych chorób płuc jest schemat uwzględniający etiologię zaburzeń, czyli podział na jednostki chorobowe o znanej i nieznanej etiologii (tab. 1). Taki sposób klasyfikacji tych chorób odzwierciedla cały proces diagnostyczny, podczas którego lekarz na podstawie wyników badania podmiotowego, przedmiotowego i zaplanowanych badań dodatkowych dąży przede wszystkim do ustalenia czynnika etiologicznego choroby. Do znanych czynników, które mogą wywoływać śródmiąższowe choroby płuc, należą: wdychanie niektórych związków organicznych i nieorganicznych, leki, promieniowanie oraz część chorób układowych, np. układowe choroby tkanki łącznej.
Etiologia niektórych chorób śródmiąższowych, takich jak samoistne włóknienie płuc czy sarkoidoza, mimo dość dobrze określonego obrazu kliniczno-patologicznego, nadal nie została wyjaśniona. W większości przypadków śródmiąższowych chorób płuc o nieznanej etiologii głównym elementem wykorzystywanym do opisu jednostki chorobowej jest charakter zmian histopatologicznych. Tak więc jeżeli nie można jednoznacznie ustalić etiologii choroby, konieczne może być wykonanie biopsji płuca. Warto pamiętać, że niektóre zmiany pojawiające się w przebiegu śródmiąższowych chorób płuc, np. organizujące się zapalenie płuc czy nieserowaciejące ziarniniaki, nie są charakterystyczne. Ponieważ zmiany histopatologiczne nie zawsze pozwalają jednoznacznie ustalić rozpoznanie, badania tego typu zawsze należy rozpatrywać w połączeniu z wynikami badania klinicznego i obrazem radiologicznym.
W ostatnich latach rozpoznanie śródmiąższowej choroby płuc stało się jeszcze bardziej skomplikowane, co częściowo wynika ze zmian w definicji i kryteriach diagnostycznych wielu chorób śródmiąższowych, m.in. samoistnego śródmiąższowego zapalenia płuc.7,8 Stało się tak w następstwie postępu w rozumieniu etiologii, patogenezy i zależności między obrazem radiologicznym a przebiegiem klinicznym śródmiąższowych chorób płuc. Do poszerzenia wiedzy na temat tych chorób przyczyniło się również udoskonalenie technik badań histopatologicznych wycinków tkanki płucnej oraz zastosowanie nowych technik obrazowania, m.in. tomografii komputerowej wysokiej rozdzielczości (HRCT – high-resolution computed tomography). Na przykład samoistne włóknienie płuc, rozpoznawane niezbyt dokładnie na podstawie tradycyjnych kryteriów, w rzeczywistości stanowi heterogenną grupę śródmiąższowych chorób płuc różniących się rokowaniem i odpowiedzią na glikokortykosteroidy.8-10 Jest to szczególnie istotne w odniesieniu do wcześniejszych badań poświęconych tej chorobie, do których prawdopodobnie kwalifikowano chorych na nieswoiste śródmiąższowe zapalenie płuc – jednostkę znacznie lepiej reagującą na leczenie glikokortykosteroidami i o lepszym rokowaniu niż samoistne włóknienie płuc rozpoznawane zgodnie z obowiązującymi obecnie wytycznymi.9 Uznawanie podobnych zespołów za jedną jednostkę chorobową może utrudnić rozpoznawanie chorób, które mogą różnić się patogenezą, odpowiedzią na zastosowane leczenie i przebiegiem klinicznym.
Znanych jest ponad sto różnych chorób śródmiąższowych, jednak w codziennej praktyce klinicznej spotyka się tylko kilka z nich. Najczęstszą chorobą jest samoistne włóknienie płuc, zwane również kryptogennym włókniejącym zapaleniem pęcherzyków płucnych, stanowi ono 25-35% wszystkich przypadków śródmiąższowych chorób płuc.8,10-12 Z naszego doświadczenia wynika, że u ok. 3/4 pacjentów z chorobami śródmiąższowymi rozpoznaje się samoistne włóknienie, sarkoidozę lub śródmiąższową chorobę płuc związaną z układową chorobą tkanki łącznej.
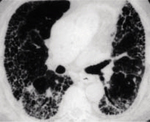
Rycina 1. Tomografia komputerowa wysokiej rozdzielczości płuc 67-letniego mężczyzny z samoistnym włóknieniem płuc/zwykłym śródmiąższowym zapaleniem płuc (IPF/UIP). Rycina przedstawia obraz narządów klatki piersiowej na wysokości oskrzela pośredniego. Widoczne są obustronne rozległe obszary plastra miodu, co potwierdza rozpoznanie UIP. W okolicach podopłucnowych widoczne są również zmiany siateczkowate wraz z obszarami o wyglądzie szkła mlecznego oraz rozstrzenia oskrzeli z pociągania w tylnych częściach dolnych płatów
Zgodnie z obowiązującymi obecnie kryteriami do pewnego rozpoznania samoistnego włóknienia płuc konieczne jest histopatologiczne potwierdzenie w bioptatach tkanki płucnej obrazu zwykłego śródmiąższowego zapalenia płuc i współistnienie typowego obrazu klinicznego i radiologicznego, tj. rozsianej choroby płuc przy jednoczesnym braku innego wytłumaczenia dla dolegliwości zgłaszanych przez chorego.7,8,11 Terminu „zwykłe śródmiąższowe zapalenie płuc” używa się w odniesieniu do histopatologicznego obrazu uszkodzenia tkanki płucnej charakteryzującego się obecnością rozsianych ognisk włóknienia kolagenowego i bliznowacenia tworzących w obwodowych i podopłucnowych częściach płuc obszary o typie plastra miodu. Charakter zmian histopatologicznych odpowiadających zwykłemu śródmiąższowemu zapaleniu płuc nie jest swoisty dla samoistnego włóknienia płuc i może również pojawić się w przebiegu chorób śródmiąższowych rozwijających się na tle układowych chorób tkanki łącznej, azbestozy, chorób układu oddechowego wywołanych przez leki oraz przewlekłej postaci alergicznego zapalenia pęcherzyków płucnych.7 Prawdopodobne rozpoznanie samoistnego włóknienia płuc można ustalić bez chirurgicznej biopsji płuca, jeżeli typowemu obrazowi tomografii komputerowej wysokiej rozdzielczości miąższu płucnego towarzyszy charakterystyczny przebieg kliniczny. Przykładem może być pojawienie się cech śródmiąższowej choroby płuc o nieznanej etiologii u osoby w średnim wieku lub starszej zgłaszającej stopniowo narastającą duszność wysiłkową, u której u podstawy obu płuc stwierdza się obecność trzeszczeń wdechowych (w piśmiennictwie anglojęzycznym określanych jako trzeszczenia velcro ze względu na duże podobieństwo do dźwięku powstającego podczas odpinania zapięć typu rzep), a w wynikach badań czynnościowych obserwuje się zmiany restrykcyjne lub zaburzenia wymiany gazowej.8 W obrazie uzyskanym za pomocą tomografii komputerowej wysokiej rozdzielczości typowe dla samoistnego włóknienia płuc jest występowanie obustronnych, obwodowych zmian o charakterze siateczkowym oraz podopłucnowych zmian typu plaster miodu rozwijających się szczególnie często w podstawnych częściach płuc (ryc. 1).8,13 Istnieje silna korelacja między zmianami w tomografii komputerowej wysokiej rozdzielczości a wynikami badań histopatologicznych wycinków pobranych podczas chirurgicznej biopsji płuca.14,15 Bioptaty tkanki płucnej pobrane podczas bronchoskopii nie powinny być wykorzystywane do potwierdzenia rozpoznania samoistnego włóknienia płuc, ponieważ do właściwej oceny charakteru zmian histopatologicznych wymagany jest większy fragment tkanki płucnej niż uzyskiwany podczas bronchoskopii.8
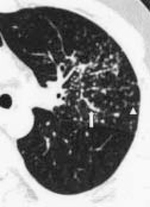
Rycina 2. Tomografia komputerowa wysokiej rozdzielczości płuc 41-letniego mężczyzny chorego na sarkoidozę. Rycina przedstawia obraz lewego płuca na poziomie ostrogi głównej. Widoczne są guzki układające się wzdłuż naczyń limfatycznych, co jest bardzo charakterystyczne dla sarkoidozy. Guzki są widoczne wzdłuż pęczków oskrzelowo-naczyniowych (strzałka), przegród międzyzrazikowych (wskaźnik) oraz wzdłuż szczelin
Drugą co do częstości występowania chorobą śródmiąższową jest sarkoidoza – wielonarządowa choroba o nieustalonej etiologii charakteryzująca się występowaniem nieserowaciejących ziarniniaków z komórek nabłonkowatych.16 W przeciwieństwie do samoistnego włóknienia płuc sarkoidoza częściej rozwija się u osób w wieku <40 lat.16 W tomografii komputerowej wysokiej rozdzielczości stwierdza się obecność zmian guzkowych o rozkładzie perylimfatycznym występujących głównie w górnych i środkowych polach płucnych (ryc. 2).17 Perylimfatyczna dystrybucja zmian guzkowych dotyczy obszaru wokół pęczków oskrzelowo-naczyniowych, przegród międzypłatowych i powierzchni opłucnej. Wynika z tego, że zarówno charakter zmian śródmiąższowych, jak i ich lokalizacja różnią się w istotnym stopniu w przypadku sarkoidozy i samoistnego włóknienia płuc. Do częstych zmian w sarkoidozie należy również obustronne powiększenie węzłów chłonnych wnęk i śródpiersia. Przed wykluczeniem innych możliwych przyczyn ziarniniakowych zmian zapalnych, przede wszystkim zakażenia, nie powinno się rozpoznawać sarkoidozy. Aby potwierdzić obecność nieserowaciejących ziarniniaków, trzeba uzyskać materiał biopsyjny z zajętej tkanki; najczęściej pobiera się go podczas bronchoskopii.
Do najistotniejszych czynników odpowiedzialnych za rozwój zmian śródmiąższowych o znanej etiologii należą układowe choroby tkanki łącznej, substancje wziewne obecne w środowisku oraz różnego rodzaju leki. Co prawda część autorów ma wątpliwości, czy chorobę śródmiąższową rozwijającą się u pacjenta z układową chorobą tkanki łącznej można nazwać zaburzeniem o znanej etiologii, wydaje się jednak, że wykrycie współistniejącej choroby układowej ma bardzo duże znaczenie dla rozpoznania, leczenia i rokowania u chorego na ILD. Dolegliwości ze strony układu oddechowego u tych osób występują dość często i mogą wynikać z zajęcia miąższu płucnego, opłucnej, dróg oddechowych, naczyń krwionośnych lub mięśni oddechowych. Zmiany śródmiąższowe pojawiające się w przebiegu chorób układowych tkanki łącznej mogą mieć różny charakter, często podobny do obserwowanych w przebiegu samoistnych śródmiąższowych zapaleń płuc.7,18 Może być to obraz podobny do niespecyficznego śródmiąższowego zapalenia płuc, samoistnego organizującego się zapalenia płuc, zwykłego śródmiąższowego zapalenia płuc, limfocytarnego śródmiąższowego zapalenia płuc czy zespołów rozlanego uszkodzenia pęcherzykowego.
Charakter zmian histopatologicznych wydaje się mieć podobną wartość prognostyczną zarówno dla chorych ze zmianami śródmiąższowymi na tle chorób układowych tkanki łącznej, jak i tych z idiopatycznymi śródmiąższowymi zapaleniami płuc.18-23 Na przykład organizujące się zapalenie płuc związane z układowymi chorobami tkanki łącznej oraz niespecyficzne śródmiąższowe zapalenie płuc charakteryzują się lepszą reakcją na leczenie glikokortykosteroidami niż zwykłe śródmiąższowe zapalenie płuc i rozlane uszkodzenie pęcherzyków płucnych. Należy jednak pamiętać, że w chorobie śródmiąższowej płuc wywołanej przez układową chorobę tkanki łącznej rokowanie w konkretnym przypadku nie wynika wyłącznie z charakteru zmian histopatologicznych, ale zależy także od samej choroby śródmiąższowej – zajęcia innych narządów poza układem oddechowym, wieku pacjenta i innych chorób współistniejących.18
Wdychanie cząsteczek pyłów nieorganicznych, takich jak krzem i azbest, powoduje pylicę płuc.24 Jeżeli dane kliniczne są wystarczające, tj. można w sposób niebudzący wątpliwości określić ekspozycję, np. na związki krzemu, to na podstawie charakteru zmian radiologicznych można ustalić rozpoznanie pylicy płuc.24,25 Zmiany widoczne w tomografii komputerowej wysokiej rozdzielczości klatki piersiowej w dużym stopniu zależą od typu pylicy i często pozwalają ustalić rozpoznanie.25
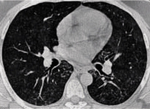
Rycina 3. Tomografia komputerowa wysokiej rozdzielczości 47-letniego chorego z podostrą postacią alergicznego zapalenia pęcherzyków płucnych obrazująca rozsiane zmiany o wyglądzie szkła mlecznego. Część tych zmian ma charakter drobnych guzków położonych w centralnej części zrazika w obrębie zmian przypominających szkło mleczne; w innych częściach płuc obszary szkła mlecznego mają bardziej zlewny charakter
Termin „alergiczne zapalenie pęcherzyków płucnych” odnosi się do choroby płuc zależnej od mechanizmów immunologicznych, w której przebiegu u osoby uczulonej – w następstwie powtarzających się inhalacji szkodliwego czynnika – dochodzi do uszkodzenia miąższu płuc i końcowego odcinka dróg oddechowych.26,27 W USA do najczęstszych postaci tej choroby należą: płuco hodowców gołębi, płuco rolnika i płuco osób korzystających ze spa.26-28 W badaniu tomograficznym wysokiej rozdzielczości do najbardziej typowych cech alergicznego zapalenia pęcherzyków płucnych należy obecność guzków w środkowej części zrazika, zmian o charakterze szkła mlecznego, mozaikowa wentylacja, zjawisko pułapki powietrznej w fazie wydechu oraz różnego rodzaju kombinacje tych zmian (ryc. 3).29-30 U większości chorych, aby ostatecznie ustalić rozpoznanie, podczas bronchoskopii lub zabiegu chirurgicznego wykonuje się biopsję płuca.
W układzie oddechowym wiele działań niepożądanych, w tym zmiany śródmiąższowe, mogą wywoływać leki. Do rozwoju śródmiąższowej choroby płuc najczęściej prowadzą chemioterapeutyki (np. bleomycyna), leki stosowane w terapii chorób sercowo-naczyniowych (np. amiodaron) i antybiotyki (np. nitrofurantoina).31,32 Zmiany polekowe mogą przyjmować różną postać histopatologiczną, co daje duże zróżnicowanie nieprawidłowości stwierdzanych w tomografii komputerowej wysokiej rozdzielczości.32,33 Może to być obraz rozlanego uszkodzenia pęcherzyków płucnych, nieswoiste śródmiąższowe zapalenie płuc, eozynofilowe zapalenie płuc lub krwawienie pęcherzykowe.33 Wykazano, że ten sam lek u różnych chorych może wywoływać odmienne reakcje ze strony układu oddechowego.34 Przykładowo nitrofurantoina może powodować zmiany histopatologiczne odpowiadające organizującemu się zapaleniu płuc, nieswoistemu śródmiąższowemu zapaleniu płuc, złuszczającemu zapaleniu płuc lub olbrzymiokomórkowemu zapaleniu płuc.35 Wiele leków może wywoływać reakcję histologiczną o podobnym charakterze. W większości chorób śródmiąższowych wywołanych przez leki zmiany histopatologiczne nie są swoiste, a do ustalenia właściwego rozpoznania konieczne jest łączne przeanalizowanie obrazu mikroskopowego z przebiegiem klinicznym oraz wykluczenie innych przyczyn.
Palenie tytoniu może mieć istotny związek z wieloma chorobami śródmiąższowymi, m.in. z zapaleniem oskrzelików związanym z chorobą śródmiąższową, złuszczającym śródmiąższowym zapaleniem płuc, płucną postacią histiocytozy z komórek Langerhansa oraz ostrym eozynofilowym zapaleniem płuc.36-38 Palenie tytoniu jest również czynnikiem ryzyka rozwoju samoistnego włóknienia płuc. Zaobserwowano, że do rozwoju 80-100% przypadków płucnej histiocytozy z komórek Langerhansa, złuszczającego śródmiąższowego zapalenia płuc i choroby śródmiąższowej związanej z zapaleniem oskrzelików oddechowych dochodzi właśnie u chorych palących tytoń.36 Natomiast wśród chorych na ostre eozynofilowe zapalenie płuc palacze stanowią tylko nieznaczną część.38-41 Śródmiąższowa choroba płuc związana z zapaleniem oskrzelików oddechowych oraz złuszczające śródmiąższowe zapalenie płuc charakteryzują się zróżnicowanym nasileniem odpowiedzi układu oddechowego na szkodliwe działanie dymu tytoniowego. Poszczególne cechy radiologiczne tych dwóch jednostek chorobowych mogą się na siebie nakładać, a najbardziej typowym obrazem jest występowanie zmian o charakterze szkła mlecznego.42 Płucna histiocytoza z komórek Langerhansa cechuje się proliferacją tych komórek w układzie oddechowym, co prowadzi do destrukcji miąższu płucnego (zmiany torbielowate widoczne w tomografii komputerowej wysokiej rozdzielczości) i zaburzeń architektury układu oddechowego.43,44 W przebiegu histiocytozy może również dojść do zajęcia innych układów i narządów: kości, skóry, ślinianek, wątroby, węzłów chłonnych oraz gruczołu tarczowego.37,43,44
