Oświadczenie
Dr Ellenbogen jest konsultantem firm Boston Scientific i Sorin Biomedical, otrzymał granty na badania naukowe od firm Medtronic, Boston Scientific i St. Jude Medical, a także honoraria od firm Medtronic, Boston Scientific, St. Jude Medical i Biotronik.
Translated and reproduced with permission from Mayo Clinic Proceedings.
Piśmiennictwo:
1. Gregoratos G, Abrams J, Epstein AE, et al. ACC/AHA/NASPE 2002 Guideline Update for Implantation of Cardiac Pacemakers and Antiarrhythmia Devices – summary article: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/NASPE Committee to Update the 1998 Pacemaker Guidelines). J Am Coll Cardiol 2002;40(9):1703-1719.
2. Chandler D, Rosenbaum J. Severe Adams-Stokes syndrome treated with isuprel and an artificial pacemaker. Am Heart J 1955;49(2):295-301.
3. Bernstein AD, Parsonnet V. Survey of cardiac pacing and defibrillation in the United States in 1993. Am J Cardiol 1996;78(2):187-196.
4. Bernstein AD, Daubert JC, Fletcher RD, et al. The revised NASPE/BPEG generic code for antibradycardia, adaptive-rate, and multisite pacing. Pacing Clin Electrophysiol 2002;25(2):260-264.
5. Lau CP, Butrous GS, Ward DE, Camm AJ. Comparison of exercise performance of six rate-adaptive right ventricular cardiac pacemakers. Am J Cardiol 1989;63(12):833-838.
6. Baig MW, Boute W, Begemann M, Perrins EJ. One-year follow-up of automatic adaptation of the rate response algorithm of the QT sensing, rate adaptive pacemaker. Pacing Clin Electrophysiol 1991;14(11, pt 1):1598-1605.
7. Landman MA, Senden PJ, van Rooijen H, van Hemel NM. Initial clinical experience with rate adaptive cardiac pacing using two sensors simultaneously. Pacing Clin Electrophysiol 1990;13(12, pt 1):1615-1622.
8. Mond H, Strathmore N, Kertes P, et al. Rate responsive pacing using a minute ventilation sensor. Pacing Clin Electrophysiol 1988;11(11, pt 2):1866-1874.
9. Ovsyshcher I, Guldal M, Karaoguz R, et al. Evaluation of a new rate adaptive ventricular pacemaker controlled by double sensors. Pacing Clin Electrophysiol 1995;18(3, pt 1):386-390.
10. Lewalter T, MacCarter D, Jung W, et al. The “low intensity treadmill exercise” protocol for appropriate rate adaptive programming of minute ventilation controlled pacemakers. Pacing Clin Electrophysiol 1995;18(7):1374-1387.
11. Lamas GA, Lee KL, Sweeney MO, et al. Mode Selection Trial in Sinus-Node Dysfunction. Ventricular pacing or dual-chamber pacing for sinus-node dysfunction. N Engl J Med 2002;346(24):1854-1862.
12. Lamas GA, Orav EJ, Stambler BS, et al. Pacemaker Selection in the Elderly Investigators. Quality of life and clinical outcomes in elderly patients treated with ventricular pacing as compared with dual-chamber pacing. N Engl J Med 1998;338(16):1097-1104.
13. Ellenbogen KA, Kapadia K, Walsh M, Mohanty PK. Increase in plasma atrial natriuretic factor during ventriculoatrial pacing. Am J Cardiol 1989;64(3):236-237.
14. Ellenbogen KA, Thames MD, Mohanty PK. New insights into pacemaker syndrome gained from hemodynamic, humoral and vascular responses during ventriculo-atrial pacing. Am J Cardiol 1990;65(1):53-59.
15. Gallik DM, Guidry GW, Mahmarian JJ, et al. Comparison of ventricular function in atrial rate adaptive versus dual chamber rate adaptive pacing during exercise. Pacing Clin Electrophysiol 1994;17(2):179-185.
16. Reiter MJ, Hindman MC. Hemodynamic effects of acute atrioventricular sequential pacing in patients with left ventricular dysfunction. Am J Cardiol 1982;49(4):687-692.
17. Rosenqvist M, Isaaz K, Botvinick EH, et al. Relative importance of activation sequence compared to atrioventricular synchrony in left ventricular function. Am J Cardiol 1991;67(2):148-156.
18. Sulke N, Dritsas A, Bostock J, et al. “Subclinical” pacemaker syndrome: a randomised study of symptom free patients with ventricular demand (VVI) pacemakers upgraded to dual chamber devices. Br Heart J 1992;67(1):57-64.
19. Grimm W, Langenfeld H, Maisch B, Kochsiek K. Symptoms, cardiovascular risk profile and spontaneous ECG in paced patients: a five-year follow-up study. Pacing Clin Electrophysiol 1990;13(12, pt 2):2086-2090.
20. Hesselson AB, Parsonnet V, Bernstein AD, Bonavita GJ. Deleterious effects of long-term single-chamber ventricular pacing in patients with sick sinus syndrome: the hidden benefits of dual-chamber pacing. J Am Coll Cardiol 1992;19(7):1542-1549.
21. Rosenqvist M, Brandt J, Schuller H. Long-term pacing in sinus node disease: effects of stimulation mode on cardiovascular morbidity and mortality. Am Heart J 1988;116(1, pt 1):16-22.
22. Zanini R, Facchinetti AI, Gallo G, et al. Morbidity and mortality of patients with sinus node disease: comparative effects of atrial and ventricular pacing. Pacing Clin Electrophysiol 1990;13(12, pt 2):2076-2079.
23. Adomian GE, Beazell J. Myofibrillar disarray produced in normal hearts by chronic electrical pacing. Am Heart J 1986;112(1):79-83.
24. Lee MA, Dae MW, Langberg JJ, et al. Effects of long-term right ventricular apical pacing on left ventricular perfusion, innervation, function and histology. J Am Coll Cardiol 1994;24(1):225-232.
25. van Oosterhout MF, Prinzen FW, Arts T, et al. Asynchronous electrical activation induces asymmetrical hypertrophy of the left ventricular wall. Circulation 1998;98(6):588-595.
26. Andersen HR, Nielsen JC, Thomsen PE, et al. Long-term follow-up of patients from a randomised trial of atrial versus ventricular pacing for sicksinus syndrome. Lancet 1997;350(9086):1210-1216.
27. Rosenqvist M, Brandt J, Schuller H. Atrial versus ventricular pacing in sinus node disease: a treatment comparison study. Am Heart J 1986;111(2):292-297.
28. Santini M, Alexidou G, Ansalone G, et al. Relation of prognosis in sick sinus syndrome to age, conduction defects and modes of permanent cardiac pacing. Am J Cardiol 1990;65(11):729-735.
29. Sweeney MO, Hellkamp AS, Ellenbogen KA, et al. MOde Selection Trial Investigators. Adverse effect of ventricular pacing on heart failure and atrial fibrillation among patients with normal baseline QRS duration in a clinical trial of pacemaker therapy for sinus node dysfunction. Circulation 2003 Jun 17;107(23):2932-2937. Epub 2003 Jun 2.
30. Thambo JB, Bordachar P, Garrigue S, et al. Detrimental ventricular remodeling in patients with congenital complete heart block and chronic right ventricular apical pacing. Circulation 2004 Dec 21;110(25):3766-3772. Epub 2004 Dec 6.
31. DAVID Trial Investigators. Dual-chamber pacing or ventricular backup pacing in patients with an implantable defibrillator: the Dual Chamber and VVI Implantable Defibrillator (DAVID) Trial. JAMA 2002;288(24):3115-3123.
32. Gammage MD, Marsh AM. Randomized trials for selective site pacing: do we know where we are going? Pacing Clin Electrophysiol 2004;27(6, pt2):878-882.
33. Sweeney MO, Bank AJ, Nsah E, et al. Search AV Extension and Managed Ventricular Pacing for Promoting Atrioventricular Conduction (SAVE PACe) Trial. Minimizing ventricular pacing to reduce atrial fibrillation in sinus-node disease. N Engl J Med 2007;357(10):1000-1008.
34. Baldasseroni S, Opasich C, Gorini M, et al. Italian Network on Congestive Heart Failure Investigators. Left bundle-branch block is associated with increased 1-year sudden and total mortality rate in 5517 outpatients with congestive heart failure: a report from the Italian Network on Congestive Heart Failure. Am Heart J 2002;143(3):398-405.
35. Shamim W, Francis DP, Yousufuddin M, et al. Intraventricular conduction delay: a prognostic marker in chronic heart failure. Int J Cardiol. 1999;70(2):171-178.
36. Prinzen FW, Hunter WC, Wyman BT, McVeigh ER. Mapping of regional myocardial strain and work during ventricular pacing: experimental study using magnetic resonance imaging tagging. J Am Coll Cardiol 1999;33(6):1735-1742.
37. Breithardt OA, Sinha AM, Schwammenthal E, et al. Acute effects of cardiac resynchronization therapy on functional mitral regurgitation in advanced systolic heart failure [published correction appears in J Am Coll Cardiol 2003;41(10):1852]. J Am Coll Cardiol 2003;41(5):765-770.
38. Xiao HB, Lee CH, Gibson DG. Effect of left bundle branch block on diastolic function in dilated cardiomyopathy. Br Heart J 1991;66(6):443-447.
39. Shaw DB, Holman RR, Gowers JI. Survival in sinoatrial disorder (sicksinus syndrome). Br Med J 1980;280(6208):139-141.
40. Alboni P, Menozzi C, Brignole M, et al. Effects of permanent pacemaker and oral theophylline in sick sinus syndrome: the THEOPACE study: a randomized controlled trial. Circulation 1997;96(1):260-266.
41. Andersen HR, Thuesen L, Bagger JP, et al. Prospective randomised trial of atrial versus ventricular pacing in sick-sinus syndrome. Lancet 1994;344(8936):1523-1528.
42. Connolly SJ, Kerr CR, Gent M, et al. Canadian Trial of Physiologic Pacing Investigators. Effects of physiologic pacing versus ventricular pacing on the risk of stroke and death due to cardiovascular causes. N Engl J Med 2000;342(19):1385-1391.
43. Dretzke J, Toff WD, Lip GY, et al. Dual chamber versus single chamber ventricular pacemakers for sick sinus syndrome and atrioventricular block. Cochrane Database Syst Rev 2004(2):CD003710.
44. Toff WD, Camm AJ, Skehan JD; United Kingdom Pacing and Cardiovascular Events (UKPACE) Trial Investigators. Single-chamber versus dualchamber pacing for high-grade atrioventricular block. N Engl J Med 2005;353(2):145-155.
45. Healey JS, Toff WD, Lamas GA, et al. Cardiovascular outcomes with atrial-based pacing compared with ventricular pacing: meta-analysis of randomized trials, using individual patient data. Circulation 2006 Jul 4;114(1):11-17. Epub 2006 Jun 26.
46. Castelnuovo E, Stein K, Pitt M, et al. The effectiveness and cost-effectiveness of dual-chamber pacemakers compared with singlechamber pacemakers for bradycardia due to atrioventricular block or sick sinus syndrome: systematic review and economic evaluation. Health Technol Assess 2005;9(49):1-246.
47. Benditt DG, Petersen M, Lurie KG, et al. Cardiac pacing for prevention of recurrent vasovagal syncope. Ann Intern Med 1995;122(3):204-209.
48. Petersen ME, Chamberlain-Webber R, Fitzpatrick AP, et al. Permanent pacing for cardioinhibitory malignant vasovagal syndrome. Br Heart J 1994;71(3):274-281.
49. Sheldon R, Koshman ML, Wilson W, et al. Effect of dualchamber pacing with automatic rate-drop sensing on recurrent neurally mediated syncope. Am J Cardiol 1998;81(2):158-162.
50. Sutton R, Brignole M, Menozzi C, et al. Vasovagal Syncope International Study (VASIS) Investigators. Dual-chamber pacing in the treatment of neurally mediated tilt-positive cardioinhibitory syncope: pacemaker versus no therapy: a multicenter randomized study. Circulation 2000;102(3):294-299.
51. Ammirati F, Colivicchi F, Santini M. Syncope Diagnosis and Treatment Study Investigators. Permanent cardiac pacing versus medical treatment for the prevention of recurrent vasovagal syncope: a multicenter, randomized, controlled trial. Circulation 2001;104(1):52-57.
52. Connolly SJ, Sheldon R, Roberts RS, Gent M. Vasovagal Pacemaker Study Investigators. The North American Vasovagal Pacemaker Study (VPS): a randomized trial of permanent cardiac pacing for the prevention of vasovagal syncope. J Am Coll Cardiol 1999;33(1):16-20.
53. Connolly SJ, Sheldon R, Thorpe KE, et al. VPS II Investigators. Pacemaker therapy for prevention of syncope in patients with recurrent severe vasovagal syncope: Second Vasovagal Pacemaker Study (VPS II): a randomized trial. JAMA 2003;289(17):2224-2229.
54. Brignole M, Menozzi C, Lolli G, et al. Long-term outcome of paced and nonpaced patients with severe carotid sinus syndrome. Am J Cardiol 1992;69(12):1039-1043.
55. Kenny RA, Richardson DA, Steen N, et al. Carotid sinus syndrome: a modifiable risk factor for nonaccidental falls in older adults (SAFE PACE). J Am Coll Cardiol 2001;38(5):1491-1496.
56. Hochleitner M, Hörtnagl H, Ng CK, et al. Usefulness of physiologic dual-chamber pacing in drug-resistant idiopathic dilated cardiomyopathy. Am J Cardiol 1990;66(2):198-202.
57. Brecker SJ, Xiao HB, Sparrow J, Gibson DG. Effects of dual-chamber pacing with short atrioventricular delay in dilated cardiomyopathy [published correction appears in Lancet 1992;340(8833):1482]. Lancet. 1992;340(8831):1308-1312.
58. Gold MR, Feliciano Z, Gottlieb SS, Fisher ML. Dual-chamber pacing with a short atrioventricular delay in congestive heart failure: a randomized study. J Am Coll Cardiol 1995;26(4):967-973.
59. Nishimura RA, Hayes DL, Holmes DR Jr, Tajik AJ. Mechanism of hemodynamic improvement by dual-chamber pacing for severe left ventricular dysfunction: an acute Doppler and catheterization hemodynamic study. J Am Coll Cardiol 1995;25(2):281-288.
60. Farwell D, Patel NR, Hall A, et al. How many people with heart failure are appropriate for biventricular resynchronization? Eur Heart J 2000;21(15):1246-1250.
61. Cazeau S, Leclercq C, Lavergne T, et al. Multisite Stimulation in Cardiomyopathies (MUSTIC) Study Investigators. Effects of multisite biventricular pacing in patients with heart failure and intraventricular conduction delay. N Engl J Med 2001;344(12):873-880.
62. Kass DA, Chen CH, Curry C, et al. Improved left ventricular mechanics from acute VDD pacing in patients with dilated cardiomyopathy and ventricular conduction delay. Circulation 1999;99(12):1567-1573.
63. Butter C, Auricchio A, Stellbrink C, et al. Pacing Therapy for Chronic Heart Failure II Study Group. Effect of resynchronization therapy stimulation site on the systolic function of heart failure patients. Circulation 2001;104(25):3026-3029.
64. Bristow MR, Saxon LA, Boehmer J, et al. Comparison of Medical Therapy, Pacing, and Defibrillation in Heart Failure (COMPANION) Investigators. Cardiac-resynchronization therapy with or without an implantable defibrillator in advanced chronic heart failure. N Engl J Med 2004;350(21):2140-2150.
65. Cleland JG, Daubert JC, Erdmann E, et al. Cardiac Resynchronization–Heart Failure (CARE-HF) Study Investigators. The effect of cardiac resynchronization on morbidity and mortality in heart failure. N Engl J Med. 2005 Apr 14;352(15):1539-1549. Epub 2005 Mar 7.
66. Gras D, Mabo P, Tang T, et al. Multisite pacing as a supplemental treatment of congestive heart failure: preliminary results of the Medtronic Inc. InSync Study. Pacing Clin Electrophysiol 1998;21(11, pt 2):2249-2255.
67. Kuhlkamp V; InSync 7272 ICD World Wide Investigators. Initial experience with an implantable cardioverter-defibrillator incorporating cardiac resynchronization therapy. J Am Coll Cardiol 2002;39(5):790-797.
68. Linde C, Leclercq C, Rex S, et al. Long-term benefits of biventricular pacing in congestive heart failure: results from the MUltisite STimulation in cardiomyopathy (MUSTIC) study. J Am Coll Cardiol 2002;40(1):111-118.
69. Stellbrink C, Breithardt OA, Franke A, et al. PATH-CHF (PAcing THerapies in Congestive Heart Failure) Investigators; CPI Guidant Congestive Heart Failure Research Group. Impact of cardiac resynchronization therapy using hemodynamically optimized pacing on left ventricular remodeling in patients with congestive heart failure and ventricular conduction disturbances.J Am Coll Cardiol 2001;38(7):1957-1965.
70. Abraham WT, Fisher WG, Smith AL, et al. MIRACLE Study Group. Cardiac resynchronization in chronic heart failure. N Engl J Med 2002;346(24):1845-1853.
71. Young JB, Abraham WT, Smith AL, et al. Multicenter InSync ICD Randomized Clinical Evaluation (MIRACLE ICD) Trial Investigators. Combined cardiac resynchronization and implantable cardioversion defibrillation in advanced chronic heart failure: the MIRACLE ICD Trial. JAMA 2003;289(20):2685-2694.
72. Summary of Safety and Effectiveness Original PMA P010012 CONTAK CD CRT-D System and EASYTRAK Coronary Venous Steroid-Eluting Single-Electrode Pace/Sense Lead, Models 4510, 4511, 4512, 4513. US Food and Drug Administration Web site. www.fda.gov/cdrh/pdf/P010012b.pdf. Accessed August 19, 2008.
73. McAlister FA, Ezekowitz J, Hooton N, et al. Cardiac resynchronization therapy for patients with left ventricular systolic dysfunction: a systematic review. JAMA 2007;297(22):2502-2514.
74. Baranowski B, Civello KC Jr, Wilkoff BL, et al. Lack of echocardiographic evidence of dyssynchrony predicts poor relative survival following cardiac resynchronization therapy [abstract AB33-4]. Heart Rhythm 2006;3(5)(suppl 1):S69.
75. Gorcsan J III, Tanabe M, Bleeker GB, et al. Combined longitudinal and radial dyssynchrony predicts ventricular response after resynchronization therapy. J Am Coll Cardiol 2007 Oct 9;50(15):1476-1483. Epub 2007 Sep 24.
76. Bleeker GB, Kaandorp TA, Lamb HJ, et al. Effect of posterolateral scar tissue on clinical and echocardiographic improvement after cardiac resynchronization therapy. Circulation 2006 Feb 21;113(7):969-976. Epub 2006 Feb 13.
77. Gasparini M, Mantica M, Galimberti P, et al. Is the left ventricular lateral wall the best lead implantation site for cardiac resynchronization therapy? Pacing Clin Electrophysiol 2003;26(1, pt 2):162-168.
78. Heist EK, Fan D, Mela T, et al. Radiographic left ventricular-right ventricular interlead distance predicts the acute hemodynamic response to cardiac resynchronization therapy. Am J Cardiol 2005;96(5):685-690.
79. Jansen AH, Bracke FA, van Dantzig JM, et al. Correlation of echo-Doppler optimization of atrioventricular delay in cardiac resynchronization therapy with invasive hemodynamics in patients with heart failure secondary to ischemic or idiopathic dilated cardiomyopathy. Am J Cardiol 2006 Feb 15;97(4):552-557. Epub 2006 Jan 4.
80. Porciani MC, Dondina C, Macioce R, et al. Echocardiographic examination of atrioventricular and interventricular delay optimization in cardiac resynchronization therapy. Am J Cardiol 2005;95(9):1108-1110.
81. Beshai JF, Grimm RA, Nagueh SF, et al. RethinQ Study Investigators. Cardiac-resynchronization therapy in heart failure with narrow QRS complexes. N Engl J Med 2007 Dec 13;357(24):2461-2471. Epub 2007 Nov 6.
Komentarz
dr hab. med. Jerzy K. Wranicz, dr med. Michał Chudzik
Zakład Elektrokardiologii i Klinika Kardiologii I Katedry Kardiologii
i Kardiochirurgii UM, Łódź, Uniwersytecki Szpital Kliniczny im. dr. S. Sterlinga, Łódź
dr hab. med. Jerzy K. Wranicz
Elektrostymulacja serca nie tylko dla lekarza podstawowej opieki zdrowotnej
dr med. Michał Chudzik
Artykuł, którego współautorem jest Ellenbogen – jeden z największych autorytetów na świecie w dziedzinie elektroterapii serca – stanowi niezwykle ciekawe opracowanie dotyczące elektrostymulacji.
Elektroterapia serca w ostatnim okresie stale się rozwija, pojawiają się nowe wskazania, nowe rozwiązania technologiczne. W związku z tym tę wąską i specjalistyczną wiedzę należy popularyzować, ponieważ cały czas zwiększa się liczba chorych ze stymulatorami serca. Obecnie także lekarz rodzinny stosunkowo często ma do czynienia z tą grupą pacjentów. Komentowana praca stanowi zatem wartościowe kompendium wiedzy z dziedziny elektrostymulacji zarówno dla lekarza kardiologa, jak i lekarza podstawowej opieki zdrowotnej.
We wstępie autorzy podkreślają rosnącą liczbę wszczepialnych urządzeń w USA. W ostatnich latach w Polsce również nastąpił bardzo duży wzrost ilości implantowanych stymulatorów serca. W roku 2008 implantowano w naszym kraju 27 251 stymulatorów (714/1 mln mieszkańców), co oznacza, że osiągnęliśmy średnią europejską.1
W Polsce preferowaną metodą implantacji jest chirurgiczna preparacja żyły odpromieniowej. Stosowana alternatywnie w niektórych ośrodkach metoda wprowadzenia elektrody przez żyłę podobojczykową przez kaniulację „na ślepo” pozwala na szybsze przeprowadzenie zabiegu, ale zwiększa ryzyko groźnych powikłań (np. odma, nakłucie tętnicy podobojczykowej). Coraz częściej podkreśla się, że metoda ta istotnie zwiększa ryzyko uszkodzenia elektrody przez jej zmiażdżenie między obojczykiem a pierwszym żebrem (tzw. crush syndrome). Wydaje się, że najlepszą metodą wprowadzenia elektrody jest kaniulacja żyły pachowej, która pozwala uniknąć wyżej wymienionych powikłań. Niestety, jej skuteczność nawet w bardzo doświadczonych ośrodkach nie przekracza 60-80%.2
Autorzy artykułu dokładnie omawiają tryby stymulacji oraz ich zastosowanie w poszczególnych wskazaniach klinicznych. Należy podkreślić, że według ostatnich wskazań European Society of Cardiology (ESC) z 2007 r. brak prawidłowego chronotropizmu, czyli zdolności do osiągnięcia 85% maksymalnej częstości rytmu serca dla danego wieku pacjenta, jest wskazaniem klasy I do implantacji stymulatora serca. Analizując objawy pacjenta – np. duszność wysiłkową – należy ocenić również wydolność chronotropową serca.
W artykule opisano dostępne w stymulatorach sensory pozwalające na odpowiednią zmianę częstości stymulacji, zależnie od aktywności fizycznej pacjenta. Obiecujący wydaje się nowo wprowadzany system, który nie został wymieniony w pracy – tzw. Closed Loop Stimulation (CLS) analizujący aktywność układu autonomicznego i w zależności od jego aktywacji regulujący częstość stymulacji. Dzięki temu można w sposób bardziej fizjologiczny dostosowywać częstość rytmu stymulatora do aktualnego obciążenia serca.
Współczesne stymulatory to urządzenia, które zapewniają zapisywanie i przechowywanie ogromnej ilości informacji zarówno z własnej pracy serca, jak i z czynności stymulatora. Aby te dane były wiarygodne, stymulator musi prawidłowo działać i być odpowiednio zaprogramowany.3 Dodatkowym elementem wspierającym naszą wiedzę o zaburzeniach rytmu jest możliwość zapisywania w pamięci stymulatora EKG wewnątrzsercowego, tzw. IEGM (intracardiac electrogram). Niestety, ograniczeniem jest maksymalny czas zapisu – ok. 200 sekund – co nie pozwala zastąpić rutynowego 24-godzinnego monitorowania EKG metodą Holtera.
Aktualne wskazania do stymulacji serca, zawarte w standardach ESC z roku 2007, rzucają nowe światło na problem, kiedy i u kogo implantować stymulator.4 Bardzo mocny nacisk, szczególnie w chorobie węzła zatokowego, położono na objawy kliniczne – zarówno te, które już wcześniej były uznanymi wskazaniami do implantacji stymulatora (pełne lub poronne zespoły Morgagniego–Adamsa–Stokesa), jak również nowe, takie jak objawy niewydolności serca, omdlenia, upośledzenie funkcji mentalnych. Przy ustalaniu wskazań do implantacji należy wykazać, że są one skorelowane z wolną pracą serca. Jednocześnie autorzy standardów nie definiują ostrej granicy w pauzach w pracy serca zarejestrowanej w EKG, która niezależnie od nasilenia objawów byłaby bezwzględnym wskazaniem do implantacji.
W chorobie węzła zatokowego wśród ekspertów panuje pełna zgodność, że nie należy implantować stymulatora komorowego (VVI). Różnice w poglądach dotyczą tego, czy należy stosować stymulacje wyłącznie przedsionkowe (AAI) – tak uważa większość autorów w Europie – czy od razu dwujamową (DDD), co sugerują lekarze amerykańscy.4
Niezależnie od tych różnic musimy uznać, że stymulacja AAI to jedyna stymulacja najbardziej zbliżona do fizjologicznej. Pozwala również na ocenę niedokrwienia w zapisie EKG, która jest znacząco utrudniona przy stymulacji dwujamowej (komorowej), nawet w okresie rytmu własnego, z uwagi na zmiany odstępu ST-T określane mianem pamięci elektrycznej.
Obecnie w Polsce, mimo braku ewidentnych korzyści ze stosowania stymulacji DDD w porównaniu z VVI w zaburzeniach przewodzenia przedsionkowo-komorowego, staramy się zawsze implantować stymulator dwujamowy – DDD.
Z uwagi na udowodniony niekorzystny wpływ stymulacji z wierzchołka prawej komory zaleca się, aby zawsze umieszczać elektrodę w miejscach alternatywnych do tej lokalizacji (droga odpływu prawej komory, środkowa przegroda międzykomorowa lub najtrudniejszy sposób – stymulacja pęczka Hisa). Niestety, ta lokalizacja wymusza stosowanie elektrod o tzw. aktywnej fiksacji, co wpływa na większe ryzyko powikłań w postaci perforacji mięśnia sercowego. W związku z tym zawsze u pacjenta po zabiegu, nawet wiele miesięcy, takie objawy jak niespecyficzne bóle w klatce piersiowej czy utrata skutecznej stymulacji w zapisie EKG nakazują dokładną diagnostykę tych nieprawidłowości.
W zespole wazowagalnym o typie kardiodepresyjnym decyzja o implantacji stymulatora zgodnie z aktualnymi rekomendacjami ESC musi być bardzo ostrożna. Jedynie u osób po 40. r.ż. i po wyjaśnieniu, że implantacja stymulatora może nie prowadzić do redukcji epizodów utraty przytomności, można rozważyć ten sposób leczenia (zalecenie klasy IIA ). Natomiast u osób przed 40. r.ż. nie jest to zalecana metoda terapii (zalecenie klasy IIB).4
Resynchronizacja serca to dziś w pełni uznana metoda terapii niewydolności serca u wybranych pacjentów bez wskazań do klasycznej stymulacji serca, a pozostających w III lub IV klasie NYHA pomimo stosowania optymalnej terapii farmakologicznej.
W artykule szczególnie warto zwrócić uwagę na tabelę 7. Poza klasycznymi wskazaniami do terapii resynchronizującej serce zgodnymi z aktualnymi wytycznymi ESC przedstawiono w niej inne klinicznie ważne kryteria, które nie znalazły jeszcze miejsca w aktualnych zaleceniach. Ocenia się, że 30-40% pacjentów po implantacji stymulatora resynchronizującego serce spełniających typowe kryteria do zabiegu nie odnosi spodziewanych korzyści z tej metody terapii. Stanowią oni grupę tzw. non-responders. Dlatego uwzględnienie tych dodatkowych parametrów może wpłynąć na redukcję ryzyka braku korzystnej odpowiedzi na stosowane leczenie. Nasze doświadczenie w pełni potwierdza zalecenia przedstawione w tym opracowaniu.
Istotną różnicę w kwalifikacji pacjentów do terapii resynchronizującej serce między Polską a USA stanowi możliwość implantacji urządzeń z funkcją kardiowersji-defibrylacji (CRT-D). W USA stosuje się je powszechnie prawie u wszystkich chorych ze wskazaniami do resynchronizacji (podobne wskazania wg ACC/AHA/ESC do CRT i CRT-D). Niestety, z uwagi na istotnie wyższy koszt tych urządzeń oraz limitowanie świadczeń w ramach NFZ niejednokrotnie musimy ograniczyć się do implantacji tylko samego stymulatora resynchronizującego bez funkcji kardiowersji-defibrylacji. Podobne problemy dostrzega ESC, dając temu wyraz w wydanych przez siebie rekomendacjach.
W odróżnieniu od USA i Kanady w Polsce kontrole pacjenta ze stymulatorem nadal odbywają się w czasie jego bezpośredniej wizyty w specjalistycznej poradni. System tele-EKG opisywany przez autorów artykułu w Polsce w przypadku pacjenta ze stymulatorem serca nie jest wykorzystywany. Co prawda takie postępowanie potencjalnie jest możliwe, ale z uwagi na aktualne zalecenia ESC, które rekomendują kontrolę pacjenta w specjalistycznej poradni, oraz brak takiej procedury (telekontrola pacjenta ze stymulatorem) w katalogu świadczeń NFZ metoda ta nie może być powszechnie stosowana.
Uważamy, że w najbliższej przyszłości system tele-EKG (z wykorzystaniem zewnętrznych modułów) lub telemonitoring stymulatora powinny stanowić uzupełnienie rutynowej kontroli pacjenta. Telemonitoring to technologia, która w najbliższym czasie znacząco przyczyni się do lepszego kontrolowania i leczenia naszych pacjentów. Współczesne stymulatory mogą bezpośrednio przesyłać nie tylko EKG wewnątrzsercowe, ale również wszystkie parametry urządzenia i wiele funkcji statystycznych ułatwiających ocenę stanu klinicznego pacjenta.5,6
Współczesne układy stymulujące serca to urządzenia o bardzo małej awaryjności. Niemniej jednak są to bardzo złożone układy, o wielu algorytmach, co wpływa na ryzyko wystąpienia różnorodnych zaburzeń w ich pracy.
Lekarz, który nie ma dostępu do specjalistycznego sprzętu – programatora do kontroli stymulatora serca – nie ma możliwości przeprowadzenia pełnej diagnostyki oraz zmiany parametrów urządzenia.
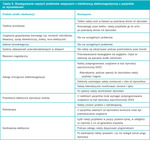
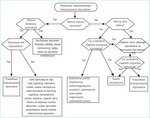
Podczas każdej wizyty pacjenta z wszczepionym stymulatorem lekarz powinien zwrócić uwagę na:
Objawy kliniczne
Tak jak opisują autorzy, pełne bądź niepełne utraty przytomności, kołatania serca, nasilenie objawów niewydolności serca, ból w okolicy loży stymulatora, stany gorączkowe powinny po wyeliminowaniu innych przyczyn być wskazaniem do kontroli układu stymulującego w specjalistycznym ośrodku.
Badanie podmiotowe
Przy każdej wizycie pacjenta lekarz bezwzględnie musi obejrzeć lożę stymulatora. Do objawów nakazujących konsultację w ośrodku specjalistycznym należą: obrzęk loży stymulatora, objawy zapalenia, ropienie, wyłonienie stymulatora.
Zapis EKG
Należy go analizować z uwzględnieniem aktualnych parametrów stymulatora, które powinien mieć przy sobie pacjent.
Każdy zwolniony rytm serca w zapisie EKG poniżej zaprogramowanej częstości podstawowej stymulatora (rytm podstawowy, basic interval) powinien być bezwzględnym wskazaniem do konsultacji w trybie pilnym w ośrodku specjalistycznym.
Przyspieszony rytm serca nie zawsze oznacza złe funkcjonowanie stymulatora. Może on wynikać z arytmii i wówczas wymagane jest leczenie choroby podstawowej. Sporadycznie w takich przypadkach konieczna jest zmiana parametrów, dlatego też należy skonsultować pacjenta w ośrodku specjalistycznym w trybie zależnym od objawów klinicznych (pilnym bądź planowym).
Coraz częściej stosowane są układy stymulujące o tzw. dwubiegunowej stymulacji (bipolarnej). Powoduje to, że w zapisie EKG możemy nie widzieć iglic stymulacji, co może znacząco utrudnić prawidłowe różnicowanie i rozpoznanie zaburzeń sterowania lub stymulacji.
Lekarz podstawowej opieki zdrowotnej powinien pamiętać, że nie wszystkie zabiegi i procedury medyczne mogą być bezpiecznie wykonywane u pacjenta ze stymulatorem. Wykonywanie badania metodą rezonansu magnetycznego jest generalnie przeciwwskazane w tej grupie chorych, chociaż pojawiają się stymulatory, które umożliwiają jego przeprowadzenie.7
Przed skierowaniem pacjenta na badania dodatkowe, w których wykorzystywane jest pole elektromagnetyczne, oraz przed zabiegami rehabilitacji związanymi z elektroterapią, zabiegami operacyjnymi, radioterapią w przebiegu choroby nowotworowej należy dokonać indywidualnej oceny chorego wyłącznie po konsultacji w ośrodku specjalistycznym.
W swojej praktyce lekarz podstawowej opieki zdrowotnej coraz częściej ma do czynienia z pacjentami z wszczepionym stymulatorem. Niezbędna jest podstawowa wiedza o aktualnych wskazaniach do implantacji układów stymulujących oraz umiejętność oceny klinicznej i elektrokardiograficznej pacjenta ze stymulatorem serca. Tym celom służą publikacje oraz szkolenia i konferencje organizowane m.in. pod patronatem Sekcji Rytmu Serca i Sekcji Elektrokardiologii Nieinwazyjnej i Telemedycyny Polskiego Towarzystwa Kardiologicznego. Komentowany artykuł stanowi cenny wkład w upowszechnianie podstaw wiedzy w zakresie elektrostymulacji serca, nie tylko wśród lekarzy podstawowej opieki zdrowotnej.
Piśmiennictwo:
1. Opolski G. Późne powikłania stymulacji – wiemy, gdzie jesteśmy, i dokąd idziemy. Kardiologia po Dyplomie 2008;9:23.
2. Burri H, Sunthorn H, Dorsaz PA, Shah D. Prospective study of axillary vein puncture with or without contrast venography for pacemaker and defibrillator lead implantation. Pacing Clin Electrophysiol. 2005;28 Suppl 1:280-283.
3. Vardas PE, Auricchio A, Blanc JJ et al. Guidelines for cardiac pacing and cardiac resynchronization therapy: The Task Force for Cardiac Pacing and Cardiac Resynchronization Therapy of the European Society of Cardiology. Developed in collaboration with the European Heart Rhythm Association. Eur Heart J 2007;28:2256-95.
4. Nowak B, Mcmeekin J, Knops J. On behalf of the Stored EGM in PulsarMax II and Discovery II Study Group. Validation of Dual-Chamber Pacemaker Diagnostic Data Using Dual-Channel Stored Electrograms. Pacing and Clinical Electrophysiol 2005;28:620-628.
5. Lazarus A. Remote, wireless, ambulatory monitoring of implantable pacemakers, cardioverter defibrillators, and cardiac resynchronization therapy systems: analysis of a worldwide database. Pacing Clin Electrophysiol 2007;30:S2-S12.
6. Jung W, Rillig A, Birkemeyer R, Miljak T, Meyerfeldt U. Advances in remote monitoring of implantable pacemakers, cardioverter defibrillators and cardiac resynchronization therapy systems. J Interv Card Electrophysiol 2008;23:73-85.
7. Naehle CP, Zeijlemaker V, Thomas D, et al. Evaluation of Cumulative Effects of MR Imaging on Pacemaker Systems at 1.5 Tesla. Pacing Clin Electrophysiol 2009;30:1543.