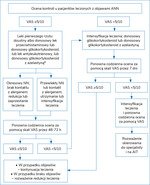
Rycina 2. Algorytm (typu step-up) postępowania u pacjentów leczonych z powodu ANN, z użyciem VAS (młodzież i osoby dorosłe)7
Oprócz ww. metod terapeutycznych wytyczne ARIA-GRADE dopuszczają krótkie zastosowanie glikokortykosteroidów doustnych. Przy nieskuteczności kontrolowania objawów z wykorzystaniem opisanych grup leków należy rozważyć skierowanie pacjenta na immunoterapię swoistą7. Zgodnie z rekomendacjami ARIA-GRADE proponowane jest postępowanie terapeutyczne oparte na algorytmie MASK, którego podstawę stanowi wizualna skala analogowa (VAS – Visual Analogue Scale). Algorytm ten wykorzystuje strategię intensyfikacji leczenia (step-up) i redukcji leczenia (step-down) w zależności od nasilenia objawów (ryc. 1 i 2)7,12.
Łączona terapia donosowa glikokortykosteroidem i lekiem przeciwhistaminowym
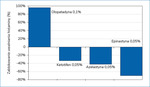
Strategia łączenia donosowych leków przeciwhistaminowych z donosowymi glikokortykosteroidami znajduje silne potwierdzenie w dostępnych danych naukowych. Jak już wspomniano, dotychczas na rynku dostępny był jeden preparat złożony zawierający donosowy glikokortykosteroid z lekiem przeciwhistaminowym (Dymista®). Zawiera on 137 µg azelastyny i 50 µg flutykazonu13. Od 2021 r. dostępna jest kolejna opcja terapeutyczna połączenia donosowego glikokortykosteroidu z lekiem przeciwhistaminowym – preparat Ryaltris®14. W jego składzie znajdziemy 25 µg mometazonu i 600 µg olopatadyny (OloMtz). Olopatadyna ma wyjątkowe cechy jako lek przeciwhistaminowy. W badaniach ex vivo wykazano, że nie tylko blokuje receptory histaminowe, lecz także stabilizuje komórki tuczne i hamuje ich aktywację oraz uwalnianie mediatorów z ziarnistości komórek tucznych. Tym samym zasadne jest przeanalizowanie danych z badań klinicznych nowo zarejestrowanego leku i odniesienie ich do uprzednio dostępnych doniesień (ryc. 3).
Patel i wsp. w podwójnie zaślepionym i podwójnie symulowanym badaniu klinicznym porównali kombinację OloMtz (w dawce 25/665 µg) do kombinacji AzeFlu (w dawce 50/137 µg) w zakresie łagodzenia objawów alergicznego nieżytu nosa po eksperymentalnych prowokacjach pyłkami traw (ambrozja). Do finalnych ramion badania włączono 144 pacjentów, 36 w każdej z grup. Pacjenci byli oceniani z wykorzystaniem skal instantaneous Total Nasal Symptom Score (iTNSS) i instantaneous Total Ocular Symptom Score (iTOSS). W porównaniu z placebo kombinacja OloMtz stosowana raz dziennie i dwa razy dziennie przynosiła istotną statystycznie poprawę w obu objawowych skalach w okresie 6-godzinnej obserwacji po prowokacjach. W porównaniu z kombinacją AzeFlu różnice te nie były istotne statystycznie zarówno w zakresie skuteczności w całym okresie obserwacji, jak i szybkości wystąpienia poprawy16.
Kolejne badanie preparatu OloMtz pod kątem jego skuteczności w leczeniu objawów sezonowego ANN przeprowadził Gross i wsp.17. Wykorzystano skale iTNSS oraz reflective Total Nasal Symptom Score (rTNSS), przy czym za pomocą tej drugiej mierzono nasilenie objawów rano i wieczorem. Dodatkowo analizowano objawy oczne, szybkość działania preparatu i jakość życia. W badaniu utworzono cztery ramiona: placebo, mometazon (dawka), olopatadyna (dawka) i kombinacja OloMtz (dawka), a w każdym z nich znalazło się 294 pacjentów (badanie ukończyło 97,5% jego uczestników). Interwencja terapeutyczna w każdym przypadku trwała 14 dni. Badana kombinacja OloMtz była skuteczniejsza w zakresie redukcji objawów w porównaniu z każdą pozostałą interwencją. W porównaniu z placebo, olopatadyną i mometazonem średnia redukcja w skali rTNSS wyniosła odpowiednio 1,09, 0,44 i 0,47. Co ważne, istotna statystycznie redukcja objawów była obserwowana w każdej składowej skali (wyciek z nosa, zatkanie i swędzenie nosa, kichanie, natychmiastowo i długotrwale). Czas do zaobserwowania istotnej statystycznie redukcji objawów dla OloMtz wynosił 15 minut, podobnie jak dla samej olopatadyny. Redukcja objawów utrzymywała się przez cały okres badania. W zakresie redukcji nasilenia objawów ocznych (ocena z wykorzystaniem skal iTOSS i rTOSS) kombinacja OloMtz była istotnie skuteczniejsza niż placebo i mometazon, nie wykazano zaś istotnych różnic w porównaniu z samą olopatadyną. Poprawa jakości życia związanej z ANN, mierzona za pomocą kwestionariusza Rhinoconjunctivitis Quality of Life Questionnaire (RQLQ), była istotnie większa dla badanej kombinacji w porównaniu z placebo i olopatadyną, jednak nie w porównaniu z samym mometazonem.
Ważnym aspektem wprowadzenia nowego preparatu w farmakoterapii alergicznego nieżytu nosa jest obserwacja dotycząca długofalowych efektów terapeutycznych i profilu bezpieczeństwa. W badaniu klinicznym III fazy autorstwa Segalla i wsp.18 ocenie poddano 601 pacjentów (cierpiących na alergiczny nieżyt nosa z powodu uczulenia na byliny) zakwalifikowanych w stosunku 4:1:1 do interwencji terapeutycznej (665 µg olopatadyny i 25 µg mometazonu) oraz dwiema formulacjami wektora badanego leku o charakterze placebo z pH 3,7 i 7,0. W ciągu 52 tygodni obserwacji nie zaobserwowano istotnych statystycznie różnic w zakresie częstotliwości występowania działań niepożądanych wynikających z leczenia. Występowały one z częstością 51,7%, 41,4% i 53,5% odpowiednio w kolejnych grupach badawczych. Przez cały okres obserwacji interwencja terapeutyczna istotnie statystycznie obniżała objawy kliniczne choroby (mierzone skalami rTNSS i iTNSS) w porównaniu z placebo. Istotna statystycznie poprawa jakości życia była obserwowana podczas wizyty w 30 tygodniu, lecz już nie w 52.
Chen i wsp. w niedawno opublikowanej metaanalizie podsumowali wyniki badań klinicznych (w tym także tych omówionych powyżej) nad kombinacją OloMtz19. Na podstawie 5 dostępnych badań klinicznych wskazali we wnioskach na wysoką skuteczność tej kombinacji w zakresie łagodzenia objawów nosowych (redukcja w skali rTNSS o średnio 0,99 pkt, iTNSS o średnio 1,05 pkt) i na dobrą skuteczność w łagodzeniu objawów ocznych (redukcja w skali rTOSS o średnio 0,5 pkt i w skali iTOSS o 0,64 pkt). Zwrócono jednak uwagę na brak istotnej statystycznie różnicy w zakresie długotrwałej poprawy jakości życia (mierzonej za pomocą skali RQLQ), co jest tłumaczone między innymi ograniczeniem w długotrwałej kontroli choroby. Niestety, problem trudności w poprawie jakości życia pacjentów z alergicznym nieżytem nosa występuje szeroko i jest obserwowany w większości badań klinicznych dotyczących tej choroby.
Produkt leczniczy Ryaltris® ma rejestrację w leczeniu umiarkowanego i ciężkiego ANN u dorosłych i dzieci od 12 lat. Preparat w postaci aerozolu należy podawać, stosując po dwie dawki do każdego otworu nosowego. Jego aplikacja, podobnie jak innych leków zawierających donosowy glikokortykosteroid, jest przeciwwskazana przy występowaniu nieleczonych, miejscowych zakażeń błony śluzowej nosa, np. opryszczki pospolitej. Przeciwwskazaniem czasowym jest także niedawny zabieg chirurgiczny w okolicy nosa lub uraz nosa. Ze względu na obserwowane w innych badaniach przypadki perforacji przegrody nosa u pacjentów stosujących donosowe leki przeciwhistaminowe nie zaleca się stosowania ww. leku w tej grupie chorych. Lek należy też stosować ze szczególną ostrożnością w przypadku immunosupresji oraz braku w wywiadzie szczepienia przeciw ospie wietrznej i odrze lub ich przechorowania.
Inne aspekty praktyczne terapii alergicznego nieżytu nosa
Alergiczny nieżyt nosa jako choroba nawracająca i nierzadko przewlekła ma niebagatelny wpływ na jakość życia pacjentów. Niestety, jak w wielu obszarach medycyny tak i w tym przypadku szeroko jest obserwowany niedostateczny poziom zabezpieczenia terapeutycznego choroby w społeczeństwie. Wynika to w dużym stopniu z niedostatecznego przestrzegania zaleceń przez pacjentów z alergicznym nieżytem nosa. Co więcej, znaczny odsetek chorych z tym schorzeniem próbuje się leczyć samodzielnie, bez wsparcia ze strony profesjonalistów ochrony zdrowia. Znaczną przeszkodę w osiąganiu długotrwałej kontroli choroby stanowi stosowanie leków przez pacjentów głównie w okresie występowania objawów przy jednoczesnym pomijaniu dawek w okresie bezobjawowym lub skąpoobjawowym. Choć algorytmy postępowania w leczeniu ANN sugerują intensyfikację leczenia przy niepowodzeniu terapeutycznym z wykorzystaniem jednego leku lub niewielkich jego dawek, dane z badań typu real-life pokazują, że wraz z intensyfikacją leczenia spada poziom kontroli choroby. Może to niestety wskazywać na ograniczenia dotychczas dostępnych metod leczenia ANN w cięższych przypadkach choroby. Niemniej autorzy wytycznych ARIA-GRADE jednoznacznie stwierdzają, że leczenie kombinacją donosowy glikokortykosteroid + lek przeciwhistaminowy (na razie na przykładzie kombinacji AzeFlu) jest skuteczniejsze niż stosowanie samego glikokortykosteroidu. Można się spodziewać, że w niedalekiej przyszłości w wytycznych zostaną uwzględnione kolejne warianty kombinacji INCS + INAH, takie jak Olo-Mtz7.
Podsumowanie
Jak pokazują omówione powyżej doniesienia z badań klinicznych, terapia kombinacją OloMtz jest efektywna i, co istotne, wykazuje wyższą skuteczność w porównaniu ze stosowaniem którejkolwiek z tych dwóch substancji osobno. Obserwacja ta wskazuje na zasadność włączania kombinacji donosowego glikokortykosteroidu i leku przeciwhistaminowego do terapii alergicznego nieżytu nosa. Wprowadzenie na rynek nowego preparatu Ryaltris® stanowi więc ważne poszerzenie możliwości terapeutycznych dla pacjentów, u których pojedynczy lek jest nieskuteczny. Niezaprzeczalną korzyścią ze stosowania dwóch substancji w jednym aplikatorze jest minimalizowanie potencjalnych błędów w sposobie przyjmowania leku oraz podniesienie poziomu przestrzegania zaleceń terapeutycznych. Jak wykazano już w wielu badaniach, nie tylko w alergicznym nieżycie nosa zlecanie kombinacji lekowych (np. wziewnych, doustnych) przynosi korzyści właśnie w zakresie systematyczności leczenia. Nierzadko efekt terapeutyczny stosowania łączonych preparatów przewyższa sumę korzyści z przyjmowania dwóch leków w osobnych aplikatorach, inhalatorach bądź tabletkach.
Zgodnie z rekomendacjami ARIA opartymi na wynikach badań zarówno randomizowanych, jak i typu real-life oraz na danych pochodzących z rzeczywistej praktyki klinicznej należy podkreślić, że skuteczność połączenia donosowego glikokortykosteroidu z donosowym lekiem przeciwhistaminowym jest większa niż samego donosowego glikokortykosteroidu. Stosowanie terapii z użyciem preparatu złożonego, dostępnego w jednym aplikatorze jest uzasadnione w przypadku niewystarczająco skutecznej monoterapii prowadzonej za pomocą glikokortykosteroidu u pacjentów z ciężką postacią alergicznego nieżytu nosa lub u pacjentów, którzy oczekują szybkiego działaniu leku. Pojawienie się na rynku nowego leku złożonego zawierającego nowoczesny glikokortykosteroid i skuteczny lek przeciwhistaminowy hamujący aktywację mastocytów istotnie więc zwiększa możliwości terapeutyczne w alergicznym nieżycie nosa.