Co znajdziesz w artykule?
- Udowodniono, że 1,8-cyneol może kontrolować przyczynę nadmiernego uwalniania mediatorów zapalnych, działa mukoaktywnie, antyoksydacyjnie, skraca czas trwania przeziębienia, łagodzi objawy zapalenia zatok oraz zapalenia oskrzeli, kontroluje również aktywność przewlekłego procesu zapalnego w astmie i przewlekłej obturacyjnej chorobie płuc, a tym samym zapobiega zaostrzeniom. 1,8-cyneol jest przenikającą biofilm cząsteczką o znanym potencjale przeciwdrobnoustrojowym
- W opracowaniu zaprezentowano najbardziej aktualny stan wiedzy na temat pełnego profilu działania związku, bezpieczeństwa jego stosowania oraz wyniki badań klinicznych wykonanych z zastosowaniem czystego 1,8-cyneolu
Spis treści
Po raz pierwszy 1,8-cyneol (dawniej znany jako eukaliptol) został opisany przez Cloeza w 1870 r. 1 Jest dobrze scharakteryzowanym, naturalnym, bicyklicznym terpenoidem, dostępnym w wielu krajach europejskich od 1995 r. Stanowi jedną z głównych składowych olejków eterycznych ekstrahowanych z liści różnych gatunków eukaliptusa 2, 3, 4, 5 .
1,8-cyneol został sklasyfikowany przez World Health Organization jako lek wykrztuśny (kod: R05CA13), wspomagający objawowe leczenie ostrego, nieropnego
zapalenia zatok, zapalnych chorób dróg oddechowych oraz jako środek wykrztuśny w produktywnym kaszlu 6, 7 . Warto zwrócić uwagę, że jego podstawowy mechanizm działania jest odmienny od pozostałych leków w tej grupie, co zostanie zaprezentowane w dalszej części artykułu (tab. 1). 1,8-cyneol jest substancją aktywną, obecną w lekach dostępnych bez recepty (OTC – over the counter) i sprzedawaną w postaci kapsułek dojelitowych miękkich. Taka formuła, w przeciwieństwie do postaci płynnych olejków eukaliptusowych, zapobiega ulatnianiu się związku, pozwala dokładniej kontrolować ilość przyjmowanej substancji i tym samym zwiększa bezpieczeństwo stosowania 1,8-cyneolu 8 .
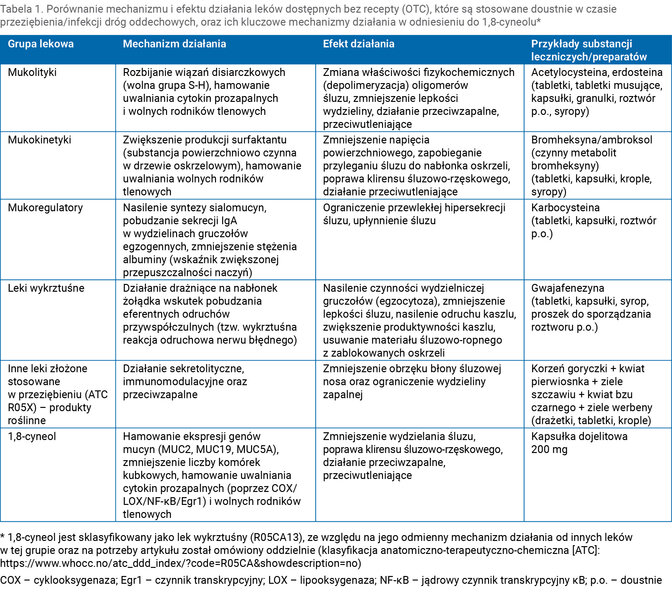
Tabela 1. Porównanie mechanizmu i efektu działania leków dostępnych bez recepty (OTC), które są stosowane doustnie w czasie przeziębienia/infekcji dróg oddechowych, oraz ich kluczowe mechanizmy działania w odniesieniu do 1,8-cyneolu*
W aktualnych wytycznych dla lekarzy POZ dotyczących leczenia wybranych infekcji oraz stanów zapalnych dróg oddechowych zaleca się, o ile stan chorego na to pozwala, włączanie w pierwszej kolejności leczenia objawowego bez wprowadzania antybiotyku 9 . Przebadany w randomizowanych i kontrolowanych placebo badaniach klinicznych 1,8-cyneol można stosować w infekcji jako element strategii tzw. czujnego wyczekiwania (watchfull waiting). Wczesne zastosowanie preparatu na bazie 1,8-cyneolu w ostrym zapaleniu błony śluzowej nosa i zatok przynosowych może ograniczać dokuczliwe objawy ze strony układu oddechowego, poprawiać samopoczucie chorych, a przy tym redukować w dobie szerzącej się antybiotykooporności liczbę niepotrzebnie przepisywanych antybiotyków 10 . Oczywiście należy podkreślić, że w przypadku szybko postępującego zakażenia utrzymującego się >5 dni lub zakażenia zagrażającego życiu najwłaściwszym działaniem będzie szybkie podanie antybiotyku, ale wówczas także można rozważyć dołączenie preparatu o działaniu objawowym. Zgodnie z niemieckimi wytycznymi dotyczącymi leczenia przewlekłej obturacyjnej choroby płuc (POChP) 1,8-cyneol jest zalecany jako dodatek do mukolityków ze względu na jego działanie wykrztuśne w zmienionym chorobowo śluzie. W wytycznych rekomenduje się stosowanie substancji o działaniu przeciwzapalnym i przeciwutleniającym w celu zmniejszenia zaostrzeń u pacjentów z POChP 11 .
Metabolizm 1,8-cyneolu
Po przyjęciu doustnym w formie kapsułek dojelitowych 1,8-cyneol jest wchłaniany z jelita cienkiego, a następnie metabolizowany w wątrobie z udziałem izoenzymów układu cytochromu P450. 1,8-cyneol ulega przekształceniu do dwóch głównych metabolitów: 2α-hydroksy- oraz 3α-hydroksy-1,8-cyneolu, które są sprzęgane z kwasem glukuronowym, a następnie wydalane z moczem (odpowiednio w ilości 20,9% oraz 10,6%) (ryc. 1) 12, 13, 14 .
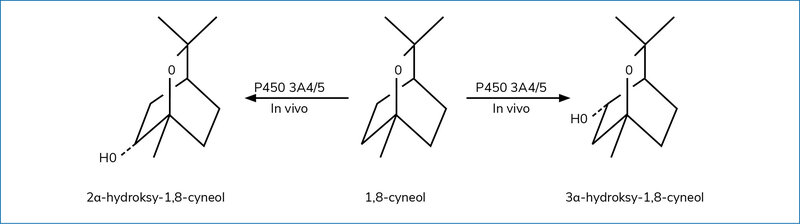
Rycina 1. Metabolizm 1,8-cyneolu (na podstawie 12 pozycji piśmiennictwa, zmodyfikowano)
Główną izoformą CYP odpowiedzialną za tworzenie 2α-hydroksy-1,8-cyneolu jest CYP3A4 15 . Oprócz ogólnoustrojowej dostępności we krwi 1,8-cyneol dzięki wymianie gazowej krew–płuca trafia do pęcherzyków płucnych i obwodowych dróg oddechowych, do których nie mają dostępu obecnie stosowane w POChP i astmie terapie wziewne, a następnie jest wydychany z powietrzem 16 . W ten sposób drogi oddechowe, a także zatoki mogą być w pełni eksponowane na przeciwzapalne i sekretolityczne działanie 1,8-cyneolu 17, 18 .
Metabolity 1,8-cyneolu są również wydzielane do mleka matki. 1,8-cyneol w pojedynczej dawce doustnej odpowiadającej jednej kapsułce 100 mg był podawany matkom karmiącym. W niewielkiej ilości mleka wykryto obecność 10 metabolitów cyneolu 19, 20 . Dotychczas nie zgłaszano problemów u niemowląt karmionych piersią kobiet przyjmujących 1,8-cyneol 6 .
Interakcje 1,8-cyneolu
Dokonano oceny in vitro wpływu 1,8-cyneolu na poziomy izoenzymów CYP układu cytochromu P450. Zaobserwowano zależny od dawki spadek aktywności następujących izoform CYP: 1A2, 2C8, 2C9, 2C19 i 3A4, zwłaszcza dla związku w stężeniach 100 i 500 µg/ml 21 .
Wiele leków stosowanych w lecznictwie jest metabolizowanych z udziałem izoenzymu CYP3A4, zatem przynajmniej w teorii istniało ryzyko, że 1,8-cyneol może wchodzić w interakcję z preparatami, które są substratami dla tego izoenzymu. Nie można wykluczyć, że duże dawki 1,8-cyneolu mogą redukować skuteczność innych produktów leczniczych oraz wpływać na czas ich działania. W praktyce odnotowano, że ryzyko interakcji ściśle zależy od dawki. 1,8-cyneol stosowany w standardowej, maksymalnej dawce dobowej (3 × 200 mg) jest słabym modulatorem (inhibitorem lub induktorem) izoenzymów cytochromu P450, zwłaszcza CYP3A4, dlatego nie zaobserwowano istotnych klinicznie interakcji lekowych w trakcie jego długoletniej obecności na rynku 22 .
Dotychczas opublikowano niewiele doniesień na temat interakcji leków z 1,8-cyneolem. Badania przeprowadzone z udziałem pięciu zdrowych ochotników, którzy otrzymywali 1,8-cyneol w aerozolu przez 10 minut w ciągu 10 kolejnych dni, wykazały wzrost klirensu osoczowego stosowanego równocześnie aminofenazonu u 4 z 5 pacjentów. Na tej podstawie autorzy sugerują, że 1,8-cyneol podawany wziewnie jest induktorem enzymów CYP w wątrobie 18 . Natomiast w badaniach przedklinicznych frakcji mikrosomalnej wątroby samic szczurów Wistar leczonych fenobarbitalem 1,8-cyneol hamował aktywność izoenzymu CYP2B1 23 , który jest homologiczny do ludzkiego izoenzymu CYP2B6 24 metabolizującego powszechnie stosowane leki (m.in. cyklofosfamid, statyny, antagonistów kanałów wapniowych, tiazolidynodiony), co może budzić obawy o ryzyko interakcji 25 . Niemniej już dwie dekady obecności 1,8-cyneolu na rynku nie potwierdziły tego typu interakcji lekowych u ludzi. Według zasad monitorowania bezpieczeństwa farmakoterapii potrzeba minimum 5 lat obserwacji porejestracyjnej, aby lek można było uznać za względnie bezpieczny lub nie.
Profil bezpieczeństwa 1,8-cyneolu
1,8-cyneol jest związkiem dobrze tolerowanym w zestawieniu z innymi preparatami OTC obecnymi na rynku, stosowanym w opanowywaniu infekcji zapalnych (tab. 2).
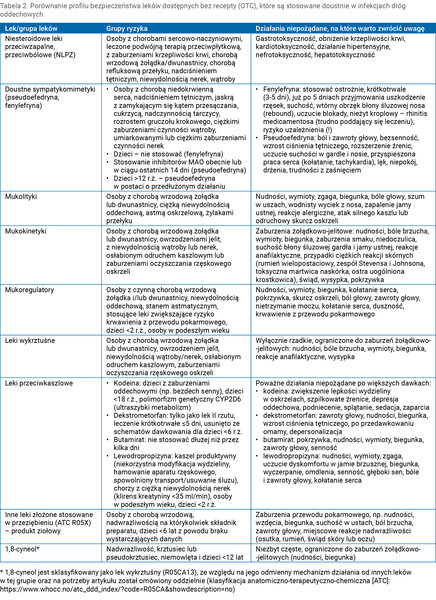
Tabela 2. Porównanie profilu bezpieczeństwa leków dostępnych bez recepty (OTC), które są stosowane doustnie w infekcjach dróg oddechowych
1,8-cyneol w przeciwieństwie do niesteroidowych leków przeciwzapalnych i przeciwbólowych (NLPZ) oraz mukolityków (NAC – acetylocysteina) nie uszkadza błony śluzowej przewodu pokarmowego (tab. 2). Może działać ochronnie na przewód pokarmowy, wykazano to między innymi w wielu przedklinicznych modelach: uszkodzenia okrężnicy 26 , uszkodzenia wątroby 27 , uszkodzenia żołądka 28 , ostrego zapalenia trzustki 29 , niealkoholowego stłuszczeniowego zapalenia wątroby 30 . Lepszy profil 1,8-cyneolu w tym zakresie wynika z tego, że NLPZ poprzez swój kwasowy charakter oraz hamowanie cyklooksygenazy 1 (COX1) działają gastrotoksycznie (blokują syntezę ochronnych prostaglandyn w układzie pokarmowym). Z kolei mukolityki typu NAC mają zdolność do depolimeryzacji śluzu, także tego ochronnego, w układzie pokarmowym, a w połączeniu z NLPZ potęgują ryzyko gastrotoksyczności i nie powinny być stosowane razem 31 . Natomiast 1,8-cyneol nie jest kwasem, nie ma wolnych grup sulfhydrylowych, które rozbijają mostki disiarczkowe i upłynniają/depolimeryzują ochronny śluz również w układzie pokarmowym, nie wpływa na pH żołądka, dlatego w połączeniu z NLPZ nie nasila ich gastrotoksycznego potencjału. W badaniu Caldas i wsp. 32 podawanie 1,8-cyneolu w dawce 100 mg/kg wręcz znacząco zwiększyło produkcję ochronnego śluzu w przewodzie pokarmowym (średnio o 89,3%). Autorzy badania zasugerowali działanie gastroprotekcyjne związku 32 . Z tego względu nie ma przeciwwskazań do podawania 1,8-cyneolu pacjentom z grupy ryzyka gastroenterologicznego (tj. choroba refluksowa przełyku, nadżerki, wrzód żołądka czy dwunastnicy, krwawienia z przewodu pokarmowego w wywiadzie, zakażenie Helicobacter pylori itp.). Nie ma także przeciwwskazań do łączenia 1,8-cyneolu z lekami z grupy NLPZ (tab. 2).
W badaniach przedklinicznych wykazano też, że 1,8-cyneol z Artemisia vulgaris L. zapobiega hepatotoksyczności po paracetamolu, przyspieszając nietoksyczny metabolizm leku w wyniku dwóch mechanizmów:
- ograniczenia ekspresji izoenzymu CYP2E1, co zmniejsza osoczowe stężenie toksycznego metabolitu paracetamolu – N-acetylo-p-benzochinonoiminy (NAPQI)
- zwiększenia aktywności czynnika jądrowego Nrf2-Keap1, co z kolei nasila ekspresję enzymów szlaku detoksykacji (dysmutazy ponadtlenkowej [SOD], glutationu [GSH], katalazy [CAT] i peroksydazy glutationowej [GPx]) oraz enzymów fazy II (sulfotransferazy [SULT] i UDP-glukuronylotransferazy [UGT]) 33 .
Mimo że 1,8-cyneol został sprawdzony pod kątem działania ochronnego na układ pokarmowy w licznych badaniach podstawowych, nadal nie dysponujemy dowodami z badań klinicznych 8 .
W przeciwieństwie do olejków eukaliptusowych, znanych z właściwości pobudzających na komórki, 1,8-cyneol wykazuje niewielkie ryzyko drażniącego działania na układ oddechowy 34 . Olejki częściej powodują negatywne efekty u pacjentów z astmą, zwłaszcza u osób z nadreaktywnością oskrzeli na zapachy (www.naturalstandard.com). Ponadto mogą powodować alergię kontaktową i reakcję skórną, a także dysfunkcję strun głosowych. Uczulający potencjał zgłaszano na przykład dla jednego z monoterpenów olejku eukaliptusowego – α-pinenu, który wzmacniał skurcz oskrzeli i działał drażniąco na tkanki 35 . Niepożądane reakcje na olejek eukaliptusowy są prawdopodobnie związane z podwójnymi wiązaniami nienasyconych składników takiej mieszaniny 35, 36 . Takie składniki mają tendencję do wiązania tlenu i tworzenia nadtlenków wodoru. Podczas enzymatycznej redukcji tych substancji powstają wolne rodniki tlenowe, które mogą uszkadzać tkanki oraz aktywować mediatory prozapalne, prowadząc do zwiększonego wydzielania śluzu w drogach oddechowych u osób z astmą 37 . Nie należy zatem zestawiać profili bezpieczeństwa czystego 1,8-cyneolu z olejkami eukaliptusowymi. Czysty monoterpen – 1,8-cyneol, jak wynika z wielu badań klinicznych, ze względu na swoją nasyconą strukturę jest bardzo dobrze tolerowany i wypada korzystniej pod kątem bezpieczeństwa niż olejek eukaliptusowy 34, 37, 38, 39, 40, 41, 42, 43 . W związku z powyższym stosowanie czystego 1,8-cyneolu powinno być preferowane w stosunku do olejków eukaliptusowych 44, 45 . Zapobiegawczo warto jednak wcześniej przeprowadzić wywiad i zachować szczególną ostrożność u pacjentów z nadwrażliwością dróg oddechowych.
Mimo dobrej tolerancji nie należy przyjmować 1,8-cyneolu w sposób nieograniczony. Brakuje szczegółowych danych na temat objawów jego przedawkowania. Dysponujemy wyłącznie danymi dotyczącymi zatrucia wysokimi dawkami olejku eukaliptusowego o nieokreślonym stopniu czystości i zawartości cyneolu. Średnia dawka śmiertelna po doustnym podaniu 20 g powoduje zaburzenia ośrodkowego układu nerwowego, takie jak zaburzenia świadomości, zmęczenie, osłabienie kończyn, zwężenie źrenic i w poważniejszych przypadkach śpiączkę oraz zaburzenia oddychania. Można się spodziewać szybkiego ustąpienia objawów i powrotu do zdrowia ze względu na szybką eliminację substancji z organizmu 6 . W badaniach toksyczności u szczurów i myszy trwających 4 tygodnie, w których stosowano 1,8-cyneol w dawce doustnej 1200 mg/kg/24 h, nie wykryto żadnego organu o skumulowanym stopniu zatrucia, w tym nie wykazano toksycznego wpływu na wątrobę. Nie ma również dowodów na istnienie potencjału mutagennego 1,8-cyneolu. Krótkoterminowe badania karcynogenności dały wynik negatywny 6 .
Działanie 1,8-cyneolu w drogach oddechowych
W ciągu ostatnich 15 lat pojawia się coraz więcej dowodów wskazujących na działanie przeciwzapalne, przeciwutleniające (antyoksydacyjne) oraz sekretolityczne 1,8-cyneolu, a według opinii niektórych autorów jest to związek, który może działać nie tylko objawowo, lecz także przyczynowo 46 .
Działanie mukoaktywne, sekretolityczne, spazmolityczne
Nadprodukcja śluzu w drogach oddechowych inicjuje nadmiarowe skurcze mięśni gładkich oskrzeli (nadreaktywność oskrzeli). Dochodzi do zmiany właściwości reologicznych śluzu, który staje się gęsty i lepki, a przy niewydolnym aparacie śluzowo-rzęskowym bardzo trudny do usunięcia. Prowadzi to do wzrostu zapalenia w drogach oddechowych i obturacji dróg oddechowych – powszechnego objawu takich chorób zapalnych, jak: przeziębienie, zapalenie zatok przynosowych, zapalenie oskrzeli, POChP lub astma. Jest to zwykle marker częstych, nawracających zaostrzeń w POChP, które mogą wywoływać progresję choroby oraz indukują steroidooporność, pośrednio prowadząc do wzrostu zachorowalności i śmiertelności 12, 47 . Leczenie tego typu stanów zapalnych wymaga skutecznego ograniczania nadprodukcji śluzu. Stosowanie 1,8-cyneolu może zmniejszyć indukowaną przez stan zapalny nadprodukcję śluzu i zredukować częstość nawracających zaostrzeń.
W badaniach klinicznych potwierdzono, że 1,8-cyneol poprawia częstotliwość uderzeń rzęsek błony śluzowej (tzw. klirens śluzowo-rzęskowy), usprawnia ewakuację nagromadzonego śluzu i wykazuje działanie sekretolityczne 48, 49, 50 . Nadprodukcja śluzu jest również wynikiem metaplazji i zwiększenia liczby komórek kubkowych oraz przerostu gruczołów podśluzówkowych. Udowodniono, że 1,8-cyneol wpływa na zmniejszenie liczby komórek kubkowych w zapalnie zmienionym nabłonku 51 .
1,8-cyneol wykazuje ponadto efekt spazmolityczny na mięśniówkę gładką oskrzeli. Hamuje skurcze mięśni gładkich prowokowane histaminą uwalnianą z komórek tucznych, co wskazuje, że jest konkurencyjnym antagonistą receptora histaminowego H1 52 . Może dodatkowo ograniczać IgE-zależną reakcję zapalną związaną z wyrzutem histaminy przez mastocyty, co ma miejsce w chorobach o podłożu zapalnym, np. w alergii, astmie 52 . 1,8-cyneol ogranicza również skurcze mięśni gładkich tchawicy indukowane przez jony K+ i wpływa na kanały wapniowe typu L bramkowane napięciem (VGCC – voltage-gated Ca+ channels) w mięśniu gładkim tchawicy 53, 54 .
1,8-cyneol ma nieco inny mechanizm działania niż powszechnie stosowane mukolityki, jak NAC czy erdosteina, jest raczej mukoaktywnym związkiem przeciwzapalnym (tab. 1). Można zaryzykować twierdzenie, że łączy w sobie profil działania mukokinetyków (tj. bromheksyna, ambroksol) oraz mukoregulatorów (tj. karbocysteina) (tab. 1), a także leków przeciwzapalnych (NLPZ czy glikokortykosteroidów [GKS]) 46 . Takie mukolityki, jak NAC czy erdosteina, depolimeryzują mukopolisacharydy i rozrzedzają zalegający w drogach oddechowych wyprodukowany śluz. 1,8-cyneol normalizuje powstawanie śluzu na bardzo wczesnych etapach jego produkcji, wpływając na ekspresję genów dla wybranych mucyn (MUC2, MUC19, MUC5A). Na skutek tego ich wytwarzanie zostaje zablokowane już na etapie transkrypcji genów, jeszcze zanim nastąpi pełna hipersekrecja śluzu przez komórki kubkowe 51 .
Wpływ 1,8-cyneolu na kontrolowanie nadmiernego wydzielania śluzu zbadano, wykorzystując model ex vivo eksperymentalnego zapalenia błony śluzowej nosa. Wykazano spadek liczby komórek kubkowych wypełnionych śluzem oraz zmniejszenie poziomu ekspresji genów mucyn MUC2 i MUC19 w połączeniu ze znacznie obniżonym poziomem jądrowego czynnika transkrypcyjnego κB (NF-κB – nuclear factor κB). Dodatkowo 1,8-cyneol nasilał aktywność antywirusowego czynnika transkrypcyjnego, interferonowego czynnika regulacyjnego 3 (IRF3 – interferon regulatory factor 3), który również ma związek z rozwojem stanu zapalnego, zwłaszcza na podłożu infekcji wirusowej 55, 56 .
Działanie przeciwzapalne
Reakcja zapalna stanowi z kolei linię obrony układu immunologicznego przed infekcjami i urazami. W przypadku nadmiernej lub niewłaściwej odpowiedzi zapalnej szkody zaczynają jednak przewyższać korzyści, co możemy zaobserwować w przebiegu chorób alergicznych oraz przewlekłych chorób o podłożu zapalnym. W przypadku zakażenia drobnoustrojami nadmierna stymulacja układu odpornościowego może się przyczynić do rozwoju sepsy i wstrząsu septycznego 57 .
Mechanizm przeciwzapalnego działania 1,8-cyneolu jest bardzo szeroki w zestawieniu z NLPZ, dlatego bywa on porównywany nawet do działania GKS. Zarówno 1,8-cyneol, jak i GKS mają strukturę podobną do terpenu, sugerowany jest zatem tzw. steroidopodobny sposób działania 1,8-cyneolu, który obejmuje hamowanie fosfolipazy A2 i COX2 46 . Odnotowano, że 1,8-cyneol (w stężeniu terapeutycznym 10−8 M) w drogach oddechowych ma potencjał przeciwzapalny porównywalny do budezonidu 44, 45 . Natomiast w badaniach in vitro na ludzkich monocytach wykazano, że dodanie 1,8-cyneolu do budezonidu potęguje jego aktywność antyoksydacyjną 58, 59 . Jego potencjał wynika z dwóch kluczowych mechanizmów.
Pierwszy to mechanizm niewybiórczego hamowania obydwu ścieżek: szlaku AA 5-lipooksygenazy (LOX) wraz z syntezą leukotrienów LTB4 oraz szlaku cyklooksygenazy (COX) z syntezą prostaglandyny E2 (PGE2) i tromboksanu B2 (TxB2). 1,8-cyneol działa zarówno jako inhibitor COX1, jak i COX2 z niższym (30%) powinowactwem do enzymu COX2 46 . 1,8-cyneol dwukrotnie silniej hamuje ścieżkę COX niż LOX, przez co mocniej oddziałuje na większość prostanoidów i cytokin niż LTB4. 1,8-cyneol szczególnie silnie ogranicza produkcję czynnika martwicy nowotworu (TNFα – tumor necrosis factor α). Potencjał hamujący przedstawiał się następująco: TNFα (–98,8%) > TxB2 (–91%) > IL1β (–74%) > LTB4 (–47,6%) 44, 45, 60, 61 . Warto dodać, że prostanoidy szlaku COX biorą udział w wydzielaniu śluzu w drogach oddechowych, zwężeniu oskrzeli, indukcji mediatorów stanu zapalnego z innych komórek oraz wywołują kaszel 62 . LTB4 natomiast to główny chemoatraktant dla neutrofili/leukocytów, który prowadzi do adhezji tych komórek do śródbłonka naczyniowego, intensyfikując reakcję zapalną, co zwiększa ryzyko zwężenia oskrzeli 63, 64 . Już w 1998 r. wskazano, że 1,8-cyneol zmniejsza wytwarzanie czynników prozapalnych w monocytach 44, 45 , a także w limfocytach o ponad 60% 65 . 1,8-cyneol, hamując limfocyty Th2, blokuje również produkcję IL4 i IL5, dlatego może działać przeciwalergicznie, kontrolując proces zapalny lub alergiczną odpowiedź ze strony układu immunologicznego w alergicznym zapaleniu IgE-zależnym oraz różne fenotypy astmy i POChP zależne od Th1/2 60, 61, 66 .
Drugim mechanizmem odpowiedzialnym za przeciwzapalne działanie 1,8-cyneolu, poza ingerencją w ścieżki COX i LOX, jest kontrola czynników transkrypcyjnych Egr1 (early growth response factor 1) oraz NF-κB 67 . 1,8-cyneol ingeruje w ścieżkę IκBα, hamując w ten sposób translokację podjednostki NF-κB p65 z cytoplazmy do jądra, i osłabia poziom ekspresji prozapalnych genów. Dodatkowo 1,8-cyneol osłabia aktywację NF-κB p65, co skutkuje zmniejszeniem liczby komórek zapalnych, sekrecji cytokin i stresu oksydacyjnego 67 . Czynnik transkrypcyjny NF-κB został dobrze opisany jako zaangażowany w wiele różnych chorób zapalnych u ludzi, w tym tych ściśle związanych z drogami oddechowymi (np. astma), ale również w infekcje ogólnoustrojowe, a nawet wstrząs septyczny 67 . Dzięki temu 1,8-cyneol bardzo silnie hamuje TNFα uwalniany przez monocyty, a także ogranicza pulę wielu innych mediatorów zapalnych (cytokin, chemokin, cząstek adhezyjnych) oraz ingeruje w ścieżki działania GKS na poziomie ekspresji genów, czyli na wczesnym etapie reakcji zapalnej 67, 68, 69 .
Działanie przeciwutleniające
Pozytywny wpływ 1,8-cyneolu na choroby zapalne dróg oddechowych jest dodatkowo wspierany przez jego działanie antyoksydacyjne (przeciwutleniające). Dzięki niemu 1,8-cyneol może bezpośrednio kontrolować nadprodukcję śluzu w drogach oddechowych, ograniczać skurcz oskrzeli i zapobiegać zaostrzeniom. 1,8-cyneol hamuje powstawanie reaktywnych form tlenu (ROS – reactive oxygen species), redukuje aktywność SOD i powstawanie jonów O2– oraz H2O2 58, 59 . Działanie antyoksydacyjne ma szczególne znaczenie w przewlekłej obturacyjnej chorobie płuc i astmie, gdyż ROS odpowiadają za zaostrzenia w POChP oraz powodują transformację astmy kontrolowanej w niekontrolowaną, nierzadko wymagającą leczenia ogólnoustrojowymi GKS 70, 71 . W badaniach in vitro na ludzkich monocytach wykazano, że dodanie 1,8-cyneolu potęguje aktywność antyoksydacyjną jednego z silniejszych GKS – budezonidu 58, 59 .
Działanie przeciwbakteryjne
Do działania przeciwbakteryjnego 1,8-cyneolu przyczynia się jego zdolność blokowania szlaku, który stanowi system komunikacji między drobnoustrojami a środowiskiem zewnętrznym za pomocą różnych substancji chemicznych (autoinduktorów) 72 . Szlak komunikacji odgrywa też ważną rolę w procesie tworzenia i funkcjonowania biofilmu bakteryjnego chroniącego mikroorganizmy przed szkodliwym wpływem czynników zewnętrznych. Dzięki temu 1,8-cyneol może oddziaływać np. na zjadliwość bakterii chorobotwórczych, działać bakteriobójczo lub bakteriostatycznie. W badaniach in vitro metodą mikrorozcieńczania 1,8-cyneol wykazywał aktywność bakteriostatyczną w zakresie 4-7 μg/ml i bakteriobójczą w stężeniach 4-9 μg/ml 73 .
Wyniki niedawno przeprowadzonego badania na dwóch niezależnych modelach in vitro przewlekłego zapalenia zatok przynosowych wskazują na zdolność 1,8-cyneolu do ograniczania biofilmu bakteryjnego i hamowania patogenów zaangażowanych w proces zapalny (Streptococcus aureus, Escherichia coli, Moraxella catarrhalis) 74 . Często progresja stanu zapalnego zatok przynosowych jest wywoływana przez infekcje bakteryjne i/lub zmianę mikrobiomu, jak również tworzenie biofilmu. Staphylococcus aureus występuje w dużej ilości w jamie nosowej pacjentów, z częstością od 40% 75 do 68% 76 . Bakterie Gram(–) E. coli i M. catarrhalis oraz Gram(+) S. aureus zaangażowane w stany zapalne zatok dobrze reagują na leczenie 1,8-cyneolem. Jest to o tyle istotne, że większość bakterii Gram(–) słabo odpowiada na hamujące działanie olejków eterycznych. Fakt ten ma również ogromne znaczenie kliniczne, także ze względu na ograniczone działanie antybiotyków na bakterie Gram(–) 77 . W zjawisku lekooporności pośredniczy głównie błona zewnętrzna bakterii Gram(–), która działa jako pierwsza linia obrony przed wieloma hydrofobowymi cząsteczkami. Błona zewnętrzna okazuje się niewystarczającą barierą dla małej, niepolarnej cząsteczki 1,8-cyneolu, która może ją pokonywać bez przeszkód przez poryny – białka błonowe tworzące kanały 78 . Składniki olejków eterycznych, w tym 1,8-cyneol, mają wysoki współczynnik dyfuzji, co sprawia, że pod względem potencjału do penetracji i eliminacji biofilmu przewyższają zwykłe antybiotyki 79 .
Wykazano również hamujący wpływ 1,8-cyneolu na tworzenie biofilmu i ograniczenie wzrostu zarówno planktonicznej, jak i osiadłej formy E. coli i M. catarrhalis 74 . Dalsze badania ujawniły jego hamujący wpływ na transkrypcję genów agrA, SarA i σB, co zakłóca wewnątrzkomórkowe szlaki sygnałowe w komórkach bakterii, niezbędne do tworzenia biofilmu 74 . 1,8-cyneol oddziałuje również na biofilm bakteryjny S. aureus, który jest oporny na metycylinę (MRSA – methicillin-resistant S. aureus). Pod tym kątem zbadano olejek eteryczny z Eucalyptus globulus, którego głównym składnikiem jest 1,8-cyneol. Badanie wykazało, że 67,8% testowanych szczepów MRSA było wrażliwych zarówno na olejek eteryczny, jak i na czysty 1,8-cyneol. Proces tworzenia biofilmu został zahamowany na poziomie 74-91%, a obydwie substancje w stężeniu 0,048 mg/ml wykazywały aktywność przeciwko większości izolatów bakteryjnych 80 .
Różne olejki eukaliptusowe oceniano pod kątem minimalnego stężenia hamującego (MIC – minimum inhibitory concentration) i minimalnego stężenia bakteriobójczego (MBC – minimum bactericidal concentration) potrzebnego do zabicia 99,4% bakterii po inkubacji trwającej 18-24 h. W badaniu 1,8-cyneol (zawartość 42-70,4%) wykazywał działanie przeciwbakteryjne na poziomie 8,1-27,4% wobec szczepów: Haemophilus influenzae, Klebsiella pneumoniae, Pseudomonas aeruginosa, Staphylococcus aureus, Streptococcus agalactiae i Streptococcus pneumoniae. Dla porównania: aktywność przeciwbakteryjna antybiotyków była na poziomie 19,9-37,5% 81 . W innym badaniu 1,8-cyneol hamował 16 z 18 testowanych szczepów bakteryjnych, w tym: Staphylococcus aureus, Bacillus sp., Citrobacter sp., Escherichia coli, Klebsiella sp., Salmonella sp., oraz szczepy Vibrio cholerae. Minimalne stężenie hamujące 1,8-cyneolu przeciwko większości patogenów, mierzone testem lekowrażliwości – metodą dyfuzyjno-krążkową, wyniosło 6,7 μl/ml. Tylko przeciwko P. aeruginosa związek działał słabo, a wartość MIC wynosiła >13,3 μl/ml 82 .
Podjęto próby ustalenia docelowego miejsca działania 1,8-cyneolu i sposobu uszkadzania komórek bakteryjnych. Li i wsp. udowodnili, że 1,8-cyneol może uszkadzać na różne sposoby komórki bakterii zarówno Gram(–), jak i Gram(+) 83 . Poddane działaniu tego związku komórki S. aureus i E. coli wykazują wyraźny rozpad błony zewnętrznej i redukcję nagromadzonej nukleoplazmy oraz chromatyny jądrowej. 1,8-cyneol charakteryzował się większą skutecznością przeciwko bakteriom E. coli, ponieważ w przeciwieństwie do S. aureus dochodziło w nich do kompletnego rozerwania warstwowych polisacharydów i fosfolipidów ściany oraz błony komórkowej. Skutkuje to utratą np. jonów potasu w komórkach Escherichia coli 84 i S. aureus 85 , zmniejszeniem potencjału błonowego i załamaniem się pompy protonowej, prowadząc do wyczerpania puli adenozynotrifosforanu (ATP) w komórce i w konsekwencji do śmierci. Badania wskazują również na kolejny, potencjalny cel działania 1,8-cyneolu, jakim jest L-asparaginaza produkowana przez takie patogeny, jak: Salmonella typhimurium, Shigella flexneri, Yersinia spp. i Helicobacter pylori, które wykorzystują ten enzym do pokonywania układu odpornościowego gospodarza, ostatecznie doprowadzając do poważnych infekcji 86 . Enzym ten uczestniczy w hamowaniu procesów komórkowych, szlaków regulujących syntezę białek i metabolizm, a ponadto ogranicza odpowiedź immunologiczną gospodarza (np. hamuje odpowiedź limfocytów T i nasila wirulencję bakterii).
1,8-cyneol może wzmacniać działanie przeciwdrobnoustrojowe środków antyseptycznych, np. chlorheksydyny, w stosunku do wybranych szczepów bakteryjnych, m.in. S. aureus ATCC 25923, S. aureus opornego na metycylinę, P. aeruginosa ATCC 27853, E. coli ATCC 25922, E. faecalis ATCC 51299 i K. pneumoniae ATCC 700603 83, 87 . 1,8-cyneol może również wzmacniać działanie atybiotykoterapii. W badaniu in vitro testowano 1,8-cyneol pojedynczo lub w połączeniu z amoksycyliną/kwasem klawulanowym (AMC) i gentamycyną na trzech szczepach S. aureus, które wyizolowano od pacjentów ze stanem zapalnym kości i szpiku. 1,8-cyneol dołączony do AMC działał synergistycznie wobec wszystkich trzech szczepów, podczas gdy przy połączeniu AMC z gentamycyną nie odnotowano takiego efektu. Skuteczność przeciwbakteryjna tych trzech związków była ponadto testowana in vivo w eksperymentalnym modelu zapalenia kości i szpiku u królików, indukowanym metycylinoopornym S. aureus. Po czterech dniach stosowania AMC z 1,8-cyneolem zaobserwowano znaczną redukcję liczby bakterii w szpiku kostnym zwierząt. 1,8-cyneol wykazał synergistyczne działanie w połączeniu zarówno z AMC, jak i gentamycyną 88 .
Działanie przeciwwirusowe
Infekcje wirusowe to najczęstsza przyczyna chorób zapalnych górnych i dolnych dróg oddechowych, takich jak przeziębienie, ostre i przewlekłe zapalenie zatok przynosowych, zapalenie oskrzeli. Powodują one ponadto częste zaostrzenia w przebiegu POChP i astmy. 1,8-cyneol aktywuje antywirusowy, interferonowy, regulatorowy czynnik 3 (IRF3) 56 . Oznacza to, że oprócz działania hamującego prozapalną sygnalizację NF-κB potęguje aktywność przeciwwirusową IRF3, co może poszerzyć obszar jego zastosowań 56 . Wykazano, że może on hamować wirusa zakaźnego zapalenia oskrzeli (IBV – infectious bronchitis virus) ze stężeniem hamującym leku IC50 (inhibitory concentration; jest to takie stężenie, które hamuje replikację wirusa o 50% w stosunku do kontroli) wynoszącym 0,61 mM 89 . Na podstawie testu MTT (testu redukcji soli tetrazolowej określającego aktywność metaboliczną komórek) stwierdzono, że hamowanie IBV przez 1,8-cyneol wydaje się dużo silniejsze po wniknięciu wirusa do komórki. W symulacjach in silico udokumentowano, że 1,8-cyneol wiąże się z N-terminalną domeną nukleokapsydowego białka (N) wirusa. Miejsce wiązania dobrze scharakteryzowano, istotną rolę odgrywają w nim reszty TyrA92, ProA134, PheA137, AspA138 i TyrA140, konserwowane ewolucyjnie w różnych szczepach IBV, co dowodzi, że 1,8-cyneol może hamować nie tylko białko N szczepu IBV Gray, lecz także inne znane szczepy tego wirusa. W badaniach przedklinicznych na myszach potwierdzono, że 1,8-cyneol hamując NF-κB i redukując cytokiny prozapalne, łagodzi zmiany patologiczne wirusowego zapalenia płuc w modelu zakażenia wirusem grypy A(H3N2) 90 . Wyniki badań przedklinicznych wskazują, że połączenie 1,8-cyneolu i oseltamiwiru daje efekt synergistyczny przeciwko zakażeniu wirusem grypy A. Leczenie skojarzone wiązało się z dłuższym średnim przeżyciem oraz istotnym zmniejszeniem ekspresji cytokin (IL10, TNFα, IL1β i IFNγ) w płucach, niż obserwowano dla samego oseltamiwiru 91 .
Li i wsp. opracowali donosową szczepionkę przeciw grypie w postaci inaktywowanego wirusa, którą przetestowali w modelu przedklinicznym grypy, podając razem z adiuwantem (1,8-cyneolem) 92 . Po podaniu zwierzętom 1,8-cyneolu w dawce 12,5 mg/kg zaobserwowano dłuższy czas przeżycia, łagodniejszy stan zapalny, mniejszą utratę masy ciała, zmniejszoną śmiertelność oraz mniejsze miano wirusa w płucach w porównaniu z grupą immunizowaną szczepionką bez 1,8-cyneolu. Szczepionka z adiuwantem wzmacniała zarówno ogólnoustrojową, jak i śluzówkową odpowiedź przeciwciał IgA i IgG2a, dając silniejszą ochronę krzyżową przeciw wirusowi grypy. Opracowanie nowej terapii adiuwantowej może pomóc utrzymać skuteczność szczepionek, które tracą swoją aktywność w wyniku dryftu antygenowego i rekombinacji samego wirusa grypy 90 .
Najnowsze badania wskazują również na potencjał 1,8-cyneolu do działania przeciwwirusowego wobec koronawirusów. Udowodniono działanie przeciwwirusowe wobec wirusa SARS-CoV-2 w zainfekowanej kulturze komórek Vero 78. Aktywność przeciwwirusowa tego związku została uznana jako umiarkowana z wartością IC50s >100 µM (128,93 µM) 93 .
Działanie przeciwgrzybicze
Badano również wpływ 1,8-cyneolu na wzrost grzyba z gatunku Aspergillus flavus ATCC 22546 oraz wytwarzanych przez niego mykotoksyn, tzw. aflatoksyn. Jest to o tyle ważne badanie, że zakażenie grzybicze Aspergillus flavus prowadzi do podrażnienia dróg oddechowych, reakcji alergicznych, aż do poważniejszych schorzeń, takich jak zapalenie płuc czy ciężka astma. Częstymi objawami tej infekcji są: gorączka, kaszel, świszczący oddech i zmęczenie. 1,8-cyneol w stężeniu 250 ppm ograniczał wzrost grzyba o ok. 50%, a w stężeniu 100 ppm hamował produkcję aflatoksyny B1 i B2. Efekty działania 1,8-cyneolu były związane z drastycznym zmniejszeniem ekspresji genów aflE i aflL dla reduktazy kwasu norsolorynowego (NOR – norsolorinic acid) – enzymu biorącego udział we wczesnym etapie biosyntezy aflatoksyn 94 .
Skuteczność 1,8-cyneolu w badaniach klinicznych
1,8-cyneol w nieżycie nosa i ostrym, nieropnym zapaleniu zatok
Do podwójnie zaślepionego badania klinicznego z randomizacją, kontrolowanego placebo zakwalifikowano 150 osób w średnim wieku 30 ± 9 lat (zakres 18-57 lat); 56% stanowili mężczyźni 95 . Około 43% osób zgłosiło współistniejące alergie, a 44% paliło tytoń na początku badania. Średni czas trwania objawów zapalenia zatok przynosowych wynosił ok. 3,5 dnia przed rozpoczęciem leczenia. Znaczące różnice w punktacji objawów były widoczne już 4 dnia terapii; 1,8-cyneol istotnie poprawiał stan zdrowia osób z nieżytem nosa oraz zapaleniem zatok i pozwalał uniknąć antybiotykoterapii 95 . Po 7 dniach leczenia w grupie stosującej 1,8-cyneol zaledwie u 6 osób (8%) nie wykazano 50% poprawy. Dla porównania: w grupie placebo poprawy nie stwierdzono u 55 osób (73%). 1,8-cyneol, działając mukolitycznie i przeciwzapalnie, zmniejszał nasilenie objawów ostrego zapalenia zatok, tj. ból głowy, wrażliwość nerwu trójdzielnego na ucisk, uczucie blokady nosa i nadprodukcję wydzieliny. Dodatkowo badacze stwierdzili, że stężenie białka C-reaktywnego zostało zredukowane w większym stopniu u uczestników otrzymujących 1,8-cyneol w porównaniu z grupą placebo, chociaż nie zaobserwowano różnic w liczbie leukocytów ani szybkości sedymentacji erytrocytów 95 .
Skuteczność i bezpieczeństwo 1,8-cyneolu (200 mg 3 ×/24 h) porównywano do obecnego na rynku preparatu ziołowego (160 mg 3 ×/24 h), który zawiera: korzeń goryczki (Gentiana lutea L., radix), kwiat pierwiosnka (Primula veris L., flos), ziele szczawiu (Rumex crispus L., herba), kwiat bzu czarnego (Sambucus nigra L., flos) oraz ziele werbeny (Verbena officinalis L., herba) 96 . Oceny dokonywano w badaniu klinicznym z randomizacją, z podwójnie ślepą próbą, kontrolowanym placebo, do którego włączono 150 pacjentów z zapaleniem zatok przynosowych. Do każdej z grup przydzielono po 75 osób 96 . Porównanie skuteczności działania po 4 i 7 dniach terapii wypadło na korzyść 1,8-cyneolu. Wyraźnie lepiej ograniczał on objawy zapalenia: ból głowy w okolicach czołowych, zaczerwienienie i obrzęk błony śluzowej nosa, nadprodukcję lepkiej wydzieliny, co przełożyło się na ogólnie większą poprawę samopoczucia pacjentów. Średnia redukcja sumy objawów po 4 dniach wyniosła 6,7 (± 3,4), a po 7 dniach 11,0 (± 3,3) w grupie leczonej 1,8-cyneolem oraz 3,6 (± 2,8) po 4 dniach i 8,0 (± 3,0) po 7 dniach w grupie kontrolnej 96 . W zakresie bezpieczeństwa preparaty mają porównywalny profil. Tygodniową terapię uznano za bezpieczną. Działania niepożądane wystąpiły u niewielkiej liczby pacjentów zarówno w grupie leczonej 1,8-cyneolem (n = 2), jak i preparatem ziołowym (n = 3); były to wyłącznie łagodne objawy, głównie ze strony przewodu pokarmowego: skurcze żołądka i nudności. W grupie przyjmującej preparat ziołowy dodatkowo odnotowano ból głowy niezwiązany z samym stanem zapalnym zatok 96 .
1,8-cyneol w przeziębieniu
W najnowszym otwartym, wieloośrodkowym badaniu klinicznym IV fazy grupę uczestników (n = 522) w wieku od 18 do 70 lat leczono 1,8-cyneolem (200 mg 3 ×/24 h) przez 15 (± 2) dni od wystąpienia objawów przeziębienia. Odnotowano, że wczesne – już w pierwszym dniu przeziębienia (≤12 h) – podanie 1,8-cyneolu zmniejsza o 38% nasilenie objawów i skraca czas trwania infekcji o 2 dni w porównaniu z jego opóźnionym włączeniem, np. w 3, 4 dobie 41, 97 . Potwierdzono ponadto dobry profil bezpieczeństwa 1,8-cyneolu. Odnotowano 25 (głównie łagodnych) działań niepożądanych, w tym w przypadku 17 potwierdzono związek przyczynowo-skutkowy z 1,8-cyneolem. Tolerancja 1,8-cyneolu została oceniona jako „bardzo dobra” lub „dobra” przez 95,5% pacjentów biorących udział w badaniu 41 .
1,8-cyneol w wirusowym zapaleniu oskrzeli
W wieloośrodkowym badaniu klinicznym z podwójnie ślepą próbą, kontrolowanym placebo, przeprowadzonym wśród pacjentów (n = 242) w wieku 18-70 lat z ostrym zapaleniem oskrzeli po 4 dniach stosowania 1,8-cyneolu (200 mg/24 h) zauważono znaczną poprawę wyniku sumarycznego wskaźnika zapalenia oskrzeli w odniesieniu do grupy placebo (p = 0,0383). 1,8-cyneol istotnie ograniczył częstotliwość napadów kaszlu produktywnego (p = 0,0001). Pacjent szybciej odczuwał ulgę niż w przypadku stosowania placebo 98 . Warto dodać, że uporczywy kaszel jest głównym kryterium diagnostycznym ostrego zapalenia oskrzeli, a zatem redukcja jego napadów jest dobrym wskaźnikiem skuteczności terapii. Zmniejszenie napadów kaszlu pod wpływem stosowania 1,8-cyneolu było możliwe dzięki ograniczeniu stanu zapalnego oraz stymulacji klirensu śluzówkowo-rzęskowego 98 .
1,8-cyneol w astmie i POChP
Przewlekłe choroby dróg oddechowych związane z procesem zapalnym tylko częściowo bywają opanowywane za pomocą standardowych leków wziewnych. Znane są wyniki randomizowanych, kontrolowanych badań klinicznych, które sugerują, że systematyczne stosowanie 1,8-cyneolu może być przydatne w kontroli procesów zapalnych leżących u podstaw zaostrzeń astmy i POChP.
W randomizowanym, kontrolowanym placebo badaniu z podwójnie ślepą próbą dotyczącym ciężkiej steroidoopornej astmy uczestnicy w średnim wieku ok. 57 lat otrzymywali średnią dzienną dawkę prednizolonu ok. 11 mg (zakres 5-24 mg) oraz 1,8-cyneol (3 × 200 mg/24 h) 38 . Dodatkowo przez cały czas trwania badania przyjmowali ustalone dawki wziewnych GKS, wziewnych β2-mimetyków o długim działaniu (LABA – long-acting β2-agonists), wziewnych leków antycholinergicznych i teofilinę. Ponadto doraźnie, w celu opanowania napadu duszności, mogli stosować wziewne krótko działające β-mimetyki (SABA – short-acting β-agonists). Badanie prowadzono przez 12 tygodni, wizyty kontrolne odbywały się co 3 tygodnie. O ile objawy astmy utrzymywały się na stabilnym poziomie, dawkę prednizolonu p.o. redukowano o 2,5 mg, jeśli dawka początkowa wynosiła <20 mg, i o 5 mg, jeśli przyjmowano ≥20 mg. Leczenie 1,8-cyneolem pozwoliło na zmniejszenie średnio o 3,75 mg (36%) dziennej dawki prednizolonu w porównaniu z placebo średnio o 0,91 mg (7%) – udokumentowano istotne statystycznie (p = 0,006) działanie ograniczające stosowanie GKS. Warto podkreślić, że 1,8-cyneol wykazywał lepszą skuteczność niż budezonid – silny GKS o działaniu przeciwalergicznym i przeciwzapalnym. Co więcej, redukcja doustnych GKS nie spowodowała znacznego wzrostu użycia inhalatora z β2-mimetykiem. Badanie potwierdziło sugerowany wcześniej synergizm działania GKS z 1,8-cyneolem. Długotrwała terapia ogólnoustrojowa 1,8-cyneolem ma znaczący wpływ na oszczędzanie steroidów w astmie steroidozależnej. Był to pierwszy dowód sugerujący działanie przeciwzapalne monoterpenu 1,8-cyneolu w astmie i powód jego stosowania jako środka mukoaktywnego w chorobach górnych i dolnych dróg oddechowych 38 .
W badaniu z randomizacją, z podwójnie ślepą próbą, kontrolowanym placebo pacjenci z astmą byli obserwowani przez 6 miesięcy 40 . 1,8-cyneol był stosowany oprócz standardowej terapii. Przyjmowanie go spowodowało statystycznie znaczącą poprawę w zakresie nasilonej pierwszosekundowej objętości wydechowej (FEV1 – forced expiratory volume in one second) (p = 0,0398); średni wzrost FEV1 wyniósł 0,31 l w grupie przyjmującej 1,8-cyneol i 0,20 l w grupie placebo. Odnotowano ponadto znaczne ograniczenie nocnych objawów astmy w grupie leczonej 1,8-cyneolem w porównaniu z placebo (3,1 vs 5,2) (p = 0,0325). Ogólne samopoczucie pacjentów leczonych 1,8-cyneolem było znacznie lepsze niż otrzymujących placebo, co potwierdza punktacja uzyskana na podstawie kwestionariusza jakości życia w astmie (AQLQ – Asthma Quality of Life Questionnaire) (odpowiednio 5,2 vs 2,6) (p = 0,0475). Po 6 miesiącach leczenia 1,8-cyneolem pacjenci mieli znacznie zwiększoną (p = 0,0226) natężoną pojemność życiową (FVC – forced vital capacity) o 0,29 l; dla porównania: w grupie placebo zmiana wynosiła 0,16 l. W porównaniu z grupą placebo odnotowano także zmniejszoną intensywność kaszlu i liczbę napadów duszności zarówno w spoczynku, jak i podczas ćwiczeń. Uważa się, że było to spowodowane przeciwzapalnym i rozszerzającym oskrzela działaniem 1,8-cyneolu, które pozwala uzyskać redukcję liczby zaostrzeń i poprawia kontrolę astmy 40 .
W wieloośrodkowym badaniu klinicznym z podwójnie ślepą próbą, kontrolowanym placebo 242 pacjentów ze stabilną postacią POChP losowo przydzielano do grupy leczonej 1,8-cyneolem (200 mg) lub placebo, podawanymi 3 razy dziennie jako terapia skojarzona przez 6 miesięcy w okresie zimowym 39 . Co miesiąc badani przychodzili na wizyty kontrolne, prowadzili dziennik pacjenta oraz wykonywano u nich testy spirometryczne na początku oraz po 3 i 6 miesiącach leczenia. Wyniki tego badania dowiodły, że 1,8-cyneol stosowany jednocześnie ze standardową terapią POChP spowodował istotny spadek częstotliwości, czasu trwania oraz nasilenia zaostrzeń. Liczba pacjentów z zaostrzeniami w okresie leczenia w grupie stosującej 1,8-cyneol wynosiła 31 (28,2%), natomiast w grupie placebo 50 (45,5%). Znacznemu ograniczeniu uległy napady zaostrzeń w spoczynku, ale nie odnotowano redukcji zaostrzeń powysiłkowych. Jakość życia pacjentów z POChP poprawiła się (całkowity wynik St. George’s Respiratory Questionnaire [SGRQ] wyniósł –9,1 po leczeniu 1,8-cyneolem oraz –4,1 po leczeniu placebo), ale nie osiągnięto istotności statystycznej (p = 0,063). Profil działań niepożądanych w obydwu grupach był porównywalny, co wskazuje na dobrą tolerancję 1,8-cyneolu. Badanie dowodzi, że 1,8-cyneol poprzez ingerencję w patofizjologię zapalenia błony śluzowej dróg oddechowych jest aktywnym regulatorem zapalenia w przewlekłej obturacyjnej chorobie płuc, a dodanie go do standardowej terapii w celu kontroli zaostrzeń POChP może być skuteczną strategią terapeutyczną 39 .
Podsumowanie
Dotychczasowy stan wiedzy oraz wyniki badań klinicznych wyraźnie wskazują, że czysty 1,8-cyneol, choć został sklasyfikowany jako lek wykrztuśny, wykazuje dużo szerszy zakres oddziaływań, a jego podstawowy mechanizm działania jest odmienny od pozostałych leków zarejestrowanych w tej grupie. Jego główne zalety to: kompleksowe działanie przeciwzapalne, sekretolityczne, mukoaktywne, antyseptyczne, przeciwdrobnoustrojowe (przenika biofilm bakterii) oraz stosunkowo niewielka liczba działań niepożądanych, jak również brak istotnych klinicznie interakcji. 1,8-cyneol może być stosowany jako element tzw. strategii czujnego wyczekiwania we wczesnym, objawowym leczeniu stanów zapalnych górnych i dolnych dróg oddechowych (w przeziębieniu, zapaleniu oskrzeli, zapaleniu zatok). Ponadto może być przydatny w leczeniu objawowym chorób przewlekłych (astma, POChP) oraz w zapobieganiu ich progresji do cięższych postaci. Odkryty w ostatnich latach potencjał 1,8-cyneolu do zwiększania skuteczności wziewnie podawanych steroidów w POChP czy astmie niewątpliwie wymaga dalszych badań molekularnych i klinicznych w celu wyjaśnienia istoty tych ważnych wzajemnych oddziaływań pomiędzy molekułami.
Artykuł z grantu edukacyjnego firmy Klosterfrau

Abstract
New insights into the mode of action, efficacy and safety profile of 1,8-cineole
To date, eucalyptol (1,8-cineole) was thought to act primarily as a symptomatic expectorant. Over the last 15 years, there has been growing scientific evidence pointing to a much broader profile of activity of this compound. It has been demonstrated that pure 1,8-cineole can also control the cause of the excessive release of inflammatory mediators, has antioxidant properties, reduces the duration of common cold and helps to control chronic inflammatory processes in asthma and chronic obstructive pulmonary disease (COPD), thus preventing exacerbations. It is classified as a biofilm-penetrating molecule with known antimicrobial potential. This review aims to summarize the current state of knowledge on the mode of action and safety profile of 1,8-cineole and to present clinical studies that evaluated pure monoterpene.
- 1. Cloez MS. Étude chimique de l’eucalyptol. Comptes Rendus 1870;70:687-90
- 2. Dhakad AK, Pandey VV, Beg S, et al. Biological, medicinal and toxicological significance of Eucalyptus leaf essential oil: A review. J Sci Food Agric 2018;98:833-48
- 3. Góra J, Lis A. Najcenniejsze olejki eteryczne. Część I i II. Łódź: Wydawnictwo Politechniki Łódzkiej, 2012
- 4. Wińska K, Mączka W. Farmakologiczne właściwości 1,8-cyneolu (eukaliptolu) w chorobach układu oddechowego. Część 1. Med Trib 2020;07-08:1-4
- 5. Wińska K, Mączka W. Farmakologiczne właściwości 1,8-cyneolu (eukaliptolu) w chorobach układu oddechowego. Część 2. Med Trib 2020;09-10:47-49
- 6. ChPL. Charakterystyka Produktu Leczniczego – Soledum forte, 200 mg, kapsułki dojelitowe, miękkie. https://rejestrymedyczne.ezdrowie.gov.pl/api/rpl/medicinal-products/41288/characteristic
- 7. WHO. https://www.whocc.no/atc_ddd_index/?code=R05CA&showdescription=no
- 8. Cai ZM, Pen JQ, Chen Y, et al. 1,8-Cineole: a review of source, biological activities, and application. Journal of Asian Natural Products Research 2021; 23(10). https://doi-1org-100001acp0001.han3.wum.edu.pl/10.1080/10286020.2020.1839432
- 9. Fal AM, Babicki M, Brożek-Mądry E i wsp. Diagnostyka i leczenie wybranych infekcji oraz stanów zapalnych dróg oddechowych. Wytyczne dla lekarzy POZ. Lekarz POZ 2021;7(5):325-53
- 10. Fal AM, Kuchar E, Zaremba M i wsp. Zasady racjonalizacji terapii antybiotykowych w schorzeniach układu oddechowego i moczowego. Medical Tribune 2022;5:3-18
- 11. Vogelmeier C, Buhl R, Burghuber O, et al. Guideline for the diagnosis and treatment of COPD patients – issued by the German Respiratory Society and the German Atemwegsliga in Cooperation with the Austrian Society of Pneumology. Pneumologie 2018;72(4):253-308
- 12. Duisken M, Sandner F, Blfmeke B, et al. Metabolism of 1,8-cyneole by human cytochrome P450 enzymes: Identification of a new hydroxylated metabolite. Biochim Biophys Acta 2005;1722:304-11
- 13. Azerad R. 1,8-Cineole: Chemical and biological oxidation reactions and products. ChemPlusChem 2014;79:634
- 14. Horst K, Rychlik M. Quantification of 1,8-cyneole and of its metabolites in humans using stable isotope dilution assays. Mol Nutr Food Res 2010;54:1515-29
- 15. Miyazawa M, Shindo M, Shimada T. Oxidation of 1,8-cineole, the monoterpene cyclic ether originated from Eucalyptus polybractea, by cytochrome P450 3A enzymes in rat and human liver microsomes. Drug Metab Disp 2001;29:200-5
- 16. Juergens LJ, Rackéb K, Tuleta I, et al. Anti-inflammatory effects of 1,8-cineole (eucalyptol) improve glucocorticoid effects in vitro: A novel approach of steroid-sparing add-on therapy for COPD and asthma? Synergy 2017;5:1-8
- 17. Beauchamp J, Kirsch F, Buettner A. Real-time breath gas analysis for pharmacokinetics: monitoring exhaled breath by on-line protontransfer-reaction mass spectrometry after ingestion of eucalyptol containing capsules. J Breath Res 2010;4:026006
- 18. Galan DM, Ezeudu NE, Garcia J, et al. Eucalyptol (1,8-cineole): An underutilized ally in respiratory disorders? J Essent Oil Res 2020;32:103-10
- 19. Kirsch F, Buettner A. Characterisation of the metabolites of 1,8-cineole transferred into human milk: Concentrations and ratio of enantiomers. Metabolites 2013;3:47-71
- 20. Kirsch F, Horst K, Röhrig W, et al. Tracing metabolite profiles in human milk: Studies on the odorant 1,8-cineole transferred into breast milk after oral intake. Metabolomics 2013;9:483-96
- 21. Unger M, Frank A. Simultaneous determination of the inhibitory potency of herbal extracts on the activity of six major cytochrome P450 enzymes using liquid chromatography/mass spectrometry and automated online extraction. Rapid Commun Mass Spectrom 2004;18:2273-81
- 22. Zhang W, Lim LY. Effects of spice constituents on P-gp-mediated transport and CYP3A4-mediated metabolism in vitro. Drug Metab Dispos 2008;36(7):1283-90
- 23. De-Oliveira ACAX, Fidalgo-Neto AA, Paumgartten FJR. In vitro inhibition of liver monooxygenases by β-ionone, 1,8-cineole, (−)-menthol and terpineol. Toxicology 1999;135:33-41
- 24. Hedlund E, Gustafsson JA, Warner M. Cytochrome P450 in the brain; a review. Curr Drug Metab 2001;2:245-63
- 25. Wang H, Tompkins LM. CYP2B6: New insights into a historically overlooked cytochrome P450 isozyme. Curr Drug Metab 2008;9:598-610
- 26. Santos FA, Silva RM, Campos AR, et al. 1,8-cineole (eucalyptol), a monoterpene oxide attenuates the colonic damage in rats on acute TNBS-colitis. Food Chem Toxicol 2004;42(4):579-84
- 27. Santos FA, Silva RM, Tome AR, et al. 1,8-Cineole protects against liver failure in an in-vivo murine model of endotoxemic shock. Pharm Pharmacol 2001;53:505
- 28. Santos FA, Rao VS. 1,8-cineol, a food flavoring agent, prevents ethanol-induced gastric injury in rats. Dig Dis Sci 2001;46(2):331-7
- 29. Lima PR, de Melo TS, Carvalho KM, et al. 1,8-cineole (eucalyptol) ameliorates cerulein-induced acute pancreatitis via modulation of cytokines, oxidative stress and NF-κB activity in mice. Life Sci 2013;92(24-26):1195-201
- 30. Murata S, Ogawa K, Matsuzaka T, et al. 1,8-Cineole Ameliorates Steatosis of Pten Liver Specific KO Mice via Akt Inactivation. Int J Mol Sci 2015;16:12051-63
- 31. Woroń J. Stosowanie niesteroidowych leków przeciwzapalnych u pacjentów z chorobą zwyrodnieniową stawów a ryzyko działań niepożądanych ze strony przewodu pokarmowego. Lekarz POZ 2019;5:395-401
- 32. Caldas RGF, da Silva Oliveira AR, Araújo AV, et al. Gastroprotective Mechanisms of the Monoterpene 1,9-Cineole (Eucalyptol). PLoS One 2015;10:e0134558
- 33. Zhihui J, Xiao G, Kunpeng Z, et al. The Essential Oils and Eucalyptol from Artemisia vulgaris L. Prevent Acetaminophen-Induced Liver Injury by Activating Nrf2-Keap1 and Enhancing APAP Clearance Through Non-Toxic Metabolic Pathway. Frontiers in Pharmacology 2019;10. https://doi.org/10.3389/fphar.2019.00782
- 34. Nascimento NR, Refosco RM, Vasconcelos EC, et al. 1,8-Cineole induces relaxation in rat and guinea-pig airway smooth muscle. J Pharm Pharmacol 2009;61:361-6
- 35. Steinegger E, Hänsel R. Textbook of Pharmacognosy and Phytopharmacy. Berlin, Heidelberg, New York: Springer-Verlag 1988:329-331
- 36. Gessner O, Orzechowski G. Toxic- and medicinal plants in middle Europe. Heidelberg: Carl Winter Universitätsverlag 1974:231-330
- 37. Barnes PJ, Ito K, Adcock IM. Corticosteroid resistance in chronic obstructive disease: inactivation of histone deacetylase. Lancet 2004;363:731-3
- 38. Juergens UR, Dethlefsen U, Steinkamp G, et al. Anti-inflammatory activity of 1.8-cineol (eucalyptol) in bronchial asthma: a double-blind placebo-controlled trial. Respir Med 2003;97(3):250-6
- 39. Worth H, Schacher C, Dethlefsen U. Concomitant therapy with Cineole (Eucalyptole) reduces exacerbations in COPD: a placebo-controlled double-blind trial. Respir Res 2009;10(1):69-76
- 40. Worth H, Dethlefsen U. Patients with Asthma Benefit from Concomitant Therapy with Cineole: A Placebo-Controlled, Double-Blind Trial. Journal of Asthma 2012;49(8):849-53
- 41. Kardos P, Goldenstein K, Klimek L, et al. Early cineole administration during common cold reduces severity and promotes faster symptom decline compared to delayed treatment. Poster presented at: European Respiratory Society (ERS) International Congress, 4-6/09/2022, Barcelona, Spain 2022
- 42. Bastos VP, Gomes AS, Lima FJ, et al. Inhaled 1,8-cineole reduces inflammatory parameters in airways of ovalbumin-challenged Guinea pigs. Basic Clin Pharmacol Toxicol 2011;108:34-9
- 43. Ciftci O, Ozdemir I, Tanyildizi S, et al. Antioxidative effects of curcumin, beta-myrcene and 1,8-cineole against 2,3,7,8-tetrachlorodibenzo-p-dioxin-induced oxidative stress in rats’ liver. Toxicol Ind Health 2011;27:447-53
- 44. Juergens UR, Stöber M, Vetter H. Inhibition of cytokine production and arachidonic acid metabolism by eucalyptol (1.8-cineole) in human blood monocytes in vitro. Eur J Med Res 1998;3:508-10
- 45. Juergens UR, Stober M, Schmidt-Schilling L, et al. Anti-inflammatory effects of eucalyptol (1,8-cineole) in bronchial asthma: Inhibition of arachidonic acid metabolism in human blood monocytes ex vivo. Eur J Med Res 1998;3:407-12
- 46. Juergens UR. Anti-inflammatory properties of the monoterpene 1.8-cineole: current evidence for co-medication in inflammatory airway diseases. Drug Res (Stuttg) 2014;64(12):638-46
- 47. Suissa S, Dell’Aniello S, Ernst P. Long-term natural history of chronic obstructive pulmonary disease: severe exacerbations and mortality. Thorax 2012;67:957-63
- 48. Kaspar P, Repges R, Dethlefsen U, et al. Secretolytics in comparison. Change of muco-ciliar frequency and lung-function following therapy with cineole and ambroxol. Atemw-Lungenkrkh 1994;20:605-14
- 49. Habich G, Repges R. Chronic obstructive airway diseases. Cineole as medication useful and approved. Therapiewoche 1994;44:356-65
- 50. Wittmann M, Petro W, Kasper P, et al. Therapy of chronic obstructive airway diseases with secretolytics. Atemw-Lungenkrkh 1998;24:67-74
- 51. Sudhoff H, Klenke C, Greiner JFW, et al. 1,8-Cineol Reduces Mucus-Production in a Novel Human Ex Vivo Model of Late Rhinosinusitis. PLoS ONE 2015;10(7):e0133040. doi: 10.1371/journal.pone.0133040
- 52. Sagortchev P, Lukanov J, Beer AM. Assessments of 1.8-cineole effects on histamine receptor activity. Z Phytother 2012;33(1):12-13
- 53. Coelho-de-Souza LN, Leal-Cardoso JH, de Abreu Matos FJ, et al. Relaxant effects of the essential oil of Eucalyptus tereticornis and its main constituent 1,8-cineole on guinea-pig tracheal smooth muscle. Planta Med 2005;71:1173-5
- 54. Pereira-Gonçalves Á, Ferreira-da-Silva FW, de Holanda-Angelin-Alves CM, et al. 1,8-Cineole blocks voltage-gated L-type calcium channels in tracheal smooth muscle. Pflugers Arch 2018;470:1803-13
- 55. Juergens LJ, Worth H, Juergens UR. New perspectives for mucolytic, anti-inflammatory and adjunctive therapy with 1,8-cineole in COPD and asthma: Review on the new therapeutic approach. Adv Ther 2020. doi: 10.1007/s12325-020-01279-0
- 56. Müller J, Greiner JF, Zeuner M, et al. 1,8-Cineole potentiates IRF3-mediated antiviral response in human stem cells and in an ex vivo model of rhinosinusitis. Clin Sci (Lond) 2016;130(15):1339-52
- 57. Nedeva C, Menassa J, Puthalakath H. Sepsis: Inflammation is a necessary evil. Front Cell Dev Biol 2019;7:108
- 58. Juergens UR, Gillissen A, Stöber M, et al. Antioxidative activity of 1.8-cineol by suppression of 8-isoprostane (8-lsoP) in human monocytes involves inhibition of superoxide anions (0 2 – ) and superoxide dismutases (SODs). Poster presented at: ATS Int Conference, 20–25/5/2005, San Diego, California, USA 2005
- 59. Juergens UR, Racke K, Tuleta I, et al. Antioxidative effects of monoterpene (1.8-cineol) compared with budesonide (bud) on superoxide (0 2 − ) production in human monocytes: new evidence for co-medication in COPD and sinusitis. Poster presented at: ATS lnt Conference, May 16–20th, 2009, San Diego, CA, USA 2009
- 60. Juergens UR, Engelen T, Racke K, et al. Inhibitory activity of 1,8-cineol (eucalyptol) on cytokine production in cultured human lymphocytes and monocytes. Pulm Pharmacol Ther 2004;17:281-7
- 61. Juergens UR, Engelen T, Stöber M, et al. Inhibition of cytokine production by 1,8-cineol (eucalyptol) in stimulated human Lymphocytes and monocytes in vitro. Poster presented at: ALA/ATS Int Conference, 16–21/5/2003, Seattle, Washington, USA 2003
- 62. Hansbro PM, Kaiko GE, Foster PS. Cytokine/anti-cytokine therapy – novel treatments for asthma? Br J Pharmacol 2011;163:81-95
- 63. Barnes PJ, Chung KF, Page CP. Inflammatory mediators of asthma: an update. Pharmacol Rev 1998;50:515-96
- 64. Ogawa Y, Calhoun WJ. The role of leukotrienes in airway inflammation. J Allergy Clin Immunol 2006;118:789-98; quiz 799-800
- 65. Baslas RK, Saxena S. Chemical Examination of Essential Oil from the Fruits of Eucalyptus globulus Labill. Herba Hung 1984;23:21-3
- 66. Brusselle G, Bracke K. Targeting immune pathways for therapy in asthma and chronic obstructive pulmonary disease. Ann Am Thorac Soc 2014;11:322-8
- 67. Greiner JFW, Müller J, Zeuner MT, et al. 1,8-Cineol inhibits nuclear translocation of NF-κB p65 and NF-κB-dependent transcriptional activity. Biochimica et Biophysica Acta (BBA) – Molecular Cell Research 2013;1833(12):2866-78
- 68. Zhou JY, Wang XF, Tang FD, et al. Inhibitory effect of 1,8-cineol (eucalyptol) on Egr-1 expression in lipopolysaccharide-stimulated THP-1 cells. Acta Pharmacol Sin 2007;28:908-12
- 69. Pawlinski R, Pedersen B, Kehrle B, et al. Regulation of tissue factor and inflammatory mediators by Egr-1 in a mouse endotoxemia model. Blood 2003;101:3940-7
- 70. Birben E, Sahiner UM, Sackesen C, et al. Oxidative stress and antioxidant defense. World Allergy Organ J 2012;5:9-19
- 71. Rosanna DP, Salvatore C. Reactive oxygen species, inflammation, and lung diseases. Curr Pharm Des 2012;18:3889-90
- 72. Packiavathy IASV, Agilandeswari P, Mustafa KS, et al. Antibiofilm and quorum sensing inhibitory potential of Cuminum cyminum and its secondary metabolite methyl eugenol against gram negative bacterial pathogens. Food Res Int 2012;45:85-92
- 73. Soković M, Glamočlija J, Marin PD, et al. Antibacterial effects of the essential oils of commonly consumed medicinal herbs using an in vitro model. Molecules 2010;15:7532-46
- 74. Schürmann M, Oppel F, Gottschalk M, et al. The Therapeutic Effect of 1,8-Cineol on Pathogenic Bacteria Species Present in Chronic Rhinosinusitis. Front Microbiol 2019;10:2325
- 75. Niederfuhr A, Kirsche H, Deutschle T, et al. Staphylococcus aureus in nasal lavage and biopsy of patients with chronic rhinosinusitis. Allergy 2008;63:1359-67
- 76. Feazel LM, Robertson CE, Ramakrishnan VR, et al. Microbiome complexity and Staphylococcus aureus in chronic rhinosinusitis. Laryngoscope 2012;122:467-72
- 77. Nazzaro F, Fratianni F, De Martino L, et al. Effect of essential oils on pathogenic bacteria. Pharmaceuticals 2013;6:1451-74
- 78. Plesiat P, Nikaido H. Outer membranes of Gram-negative bacteria are permeable to steroid probes. Mol Microbiol 1992;6:1323-33
- 79. Kavanaugh NL, Ribbeck K. Selected antimicrobial essential oils eradicate Pseudomonas spp. and Staphylococcus aureus biofilms. Appl Environ Microbiol 2012;78:4057-61
- 80. Merghni A, Noumi E, Hadded O, et al. Assessment of the antibiofilm and antiquorum sensing activities of Eucalyptus globulus essential oil and its main component 1,8-cineole against methicillin-resistant Staphylococcus aureus strains. Microb Pathogen 2018;118:74-80
- 81. Elaissi A, Abid NBS, Rouis Z, et al. Chemical composition of 8 eucalyptus species’ essential oils and the evaluation of their antibacterial, antifungal and antiviral activities. BMC Complement Altern Med 2012;12:81
- 82. Pattnaik S, Subramanyam VR, Bapaji M, et al. Antibacterial and antifungal activity of aromatic constituents of essential oils. Microbios 1997;89:39-46
- 83. Li ZW, Yin ZQ, Wei Q, et al. Antibacterial activity of leaf essential oils and its constituents from Cinnamomum longepaniculatum. Int J Clin Exp Med 2014;7:1721-7
- 84. Cox SD, Gustafson JE, Mann CM, et al. Tea tree oil causes K+ leakage and inhibits respiration in Escherichia coli. Lett Appl Microbiol 1998;26:355-8
- 85. Cox SD, Mann CM, Markham JL, et al. The mode of antimicrobial action of the essential oil of Melaleuca alternifolia (tea tree oil). J Appl Microbiol 2000;88:170-5
- 86. Kullas AL, Mcclelland M, Yang H, et al. L-Asparaginase II produced by salmonella typhimurium inhibits T cell responses and mediates virulence. Cell Host Microbe 2012;12:791-8
- 87. Simsek M, Duman R. Investigation of effect of 1,8-cineole on antimicrobial activity of chlorhexidine gluconate. Pharmacogn Res 2017;9:234-7
- 88. Hriouech S, Akhmouch AA, Mzabi A, et al. The antistaphylococcal activity of amoxicillin/clavulanic acid, gentamicin, and 1,8-cineole alone or in combination and their efficacy through a rabbit model of methicillin-resistant Staphylococcus aureus osteomyelitis. Evid Based Complement Altern Med 2020;4271017. doi: 10.1155/2020/4271017
- 89. Yang Z, Wu N, Fu Y, et al. Anti-infectious bronchitis virus (IBV) activity of 1,8-cineole: effect on nucleocapsid (N) protein. J Biomol Struc Dyn 2010;28:323-30
- 90. Li Y, Lai Y, Wang Y, et al. 1, 8-Cineol Protect Against Influenza-Virus-Induced Pneumonia in Mice. Inflammation 2016;39(4):1582-93
- 91. Lai YN, Li Y, Fu LC, et al. Combinations of 1,8-cineol and oseltamivir for the treatment of influenza virus A (H3N2) infection in mice. J Med Virol 2017;89(7):1158-67
- 92. Li Y, Xu YN, Lai Y, et al. Intranasal co-administration of 1,8-cineole with influenza vaccine provide cross-protection against influenza virus infection. Phytomedicine 2017;34:127-35
- 94. Kim H-M, Kwon H, Kim K, et al. Antifungal and Antiaflatoxigenic Activities of 1,8-Cineole and t-Cinnamaldehyde on Aspergillus flavus. Appl Sci 2018;8:1655
- 95. Kehrl W, Sonnemann U, Dethlefsen U. Therapy for Acute Nonpurulent Rhinosinusitis with Cineole: Results of a Double-Blind, Randomized, Placebo-Controlled Trial. Laryngoscope 2004;114:738-42
- 96. Tesche S, Metternich F, Sonnemann U, et al. The value of herbal medicines in the treatment of acute non-purulent rhinosinusitis. Results of a double-blind, randomised, controlled trial. Eur Arch Otorhinolaryngol 2008;265(11):1355-9
- 97. Kardos P, Klimek L, Palm J, et al. Benefits of early cineole administration during common cold: an exploratory clinical trial. Poster presented at: 56 DEGAM-Jahreskongress, 09/2022b, Greifswald, Germany
- 98. Fischer J, Dethlefsen U. Efficacy of cyneole in patients suffering from acute bronchitis: a placebo-controlled double-blind trial. Cough 2013;9(1):25
