Neuroinfekcje
Hiponatremia w przebiegu neuroinfekcji – zespół nieadekwatnej syntezy wazopresyny i mózgowy zespół utraty soli
lek. Adam Garkowski
prof. hab. n. med. Joanna Zajkowska
dr n. med. Piotr Czupryna
Wprowadzenie
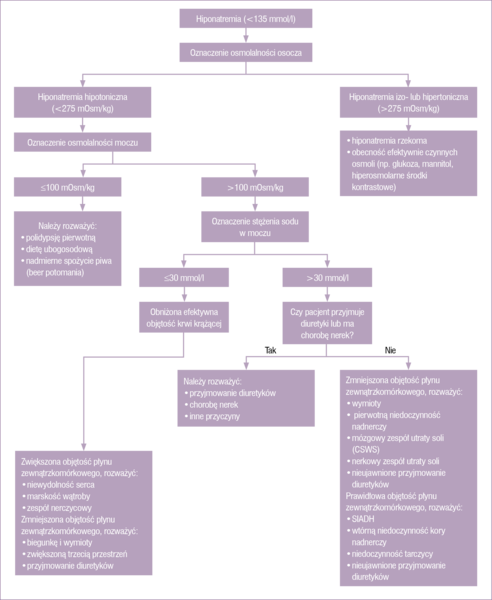
Zaburzenia elektrolitowe, zwłaszcza przebiegające z hiponatremią, są częstym powikłaniem neuroinfekcji i innych chorób ośrodkowego układu nerwowego (OUN). Hiponatremia jest skutkiem względnego nadmiaru wody w stosunku do zawartości sodu w organizmie i jest definiowana jako zmniejszenie stężenia sodu w osoczu <135 mmol/l.1 Określa się ją jako ostrą, jeśli czas jej trwania wynosi <48 godzin i jako przewlekłą, gdy utrzymuje się >48 godzin. Jeśli nie można określić czasu trwania hiponatremii, to stan ten definiuje się jako przewlekły.2 Hiponatremia jest najczęstszym zaburzeniem elektrolitowym u hospitalizowanych pacjentów (występuje u około 30-40% chorych).3 Obniżenie stężenia sodu w surowicy może doprowadzić m.in. do zagrażającego życiu obrzęku mózgu, który z kolei prowadzi do wzrostu ciśnienia śródczaszkowego i ryzyka wgłobienia mózgu. W większości przypadków hiponatremia przebiega z niską osmolalnością osocza. Hiponatremia przebiegająca z prawidłową lub zwiększoną osmolalnością osocza (hiponatremia niehipotoniczna) obejmuje hiponatremię rzekomą (pseudohiponatremię, m.in. w przebiegu hiperlipidemii lub paraproteinemii) oraz hiponatremię w przebiegu stanów przebiegających z obecnością tzw. efektywnych osmoli (np. glukozy, mannitolu, hiperosmolarnych środków kontrastowych) oraz tzw. nieefektywnych osmoli (np. mocznika lub alkoholi) zwiększających osmolalność osocza.2 W przebiegu chorób zakaźnych OUN hiponatremia jest zjawiskiem częstym i w większości przypadków spowodowana jest gorączką i odwodnieniem, a dość często również leczeniem wzmożonego ciśnienia śródczaszkowego diuretykami osmotycznymi, takimi jak mannitol, zwłaszcza przy współistniejącej niewydolności nerek. Stosowanie mannitolu w większych dawkach może również powodować hipernatremię i hiperkaliemię.4 Hiponatremia występuje w ponad 40% przypadków kleszczowego zapalenia mózgu, a jej częstość wzrasta wraz z wiekiem chorych. W jednym z badań z udziałem pacjentów z kleszczowym zapaleniem mózgu zespół nieadekwatnej syntezy wazopresyny (syndrome of inappropriate antidiuretic hormone secretion, zespół Schwartza-Barttera, SIADH) stanowił przyczynę hiponatremii w 12% przypadków.5 W innym badaniu z udziałem prawie 700 pacjentów z bakteryjnym zapaleniem opon mózgowo-rdzeniowych hiponatremię obserwowano u 30% wszystkich chorych, w tym u ponad 70% chorych z zapaleniem opon spowodowanym zakażeniem bakterią Listeria monocytogenes.6 W innych obserwacjach podobnie wysokie odsetki hiponatremii obserwowano również w zapaleniach opon o etiologii Mycobacterium tuberculosis oraz Streptococcus pyogenes (odpowiednio 79 i 58%).7,8 Wśród przyczyn hiponatremii należy wyróżnić dwa zespoły przebiegające z hiponatremią hipotoniczną (z oznaczoną osmolalnością osocza <275 mOsm/kg H2O) mogące występować w przebiegu neuroinfekcji – SIADH oraz mózgowy zespół utraty soli (cerebral salt-wasting syndrome, CSWS). Szybka diagnostyka i odpowiednie leczenie powyższych zespołów zmniejszają ryzyko wystąpienia groźnych dla życia powikłań.9 Opisano pojedyncze przypadki SIADH w przebiegu neuroboreliozy.10,11 Obniżenie stężenia sodu w surowicy, przebiegające bez zmian w objętości płynu zewnątrzkomórkowego, jest zazwyczaj skutkiem zwiększonego wydzielania wazopresyny (antidiuretic hormone, ADH), nadmiernego w stosunku do efektywnej osmolalności osocza i objętości płynu pozakomórkowego. CSWS najczęściej jest obserwowany u krytycznie chorych osób, często w przebiegu uszkodzenia OUN w wyniku krwotoku podpajęczynówkowego lub urazu głowy. Mimo pozornego podobieństwa patofizjologiczne mechanizmy rozwoju i leczenie SIADH i CSWS są odmienne. Algorytm diagnostyczny w hiponatremii przedstawia rycina 1.
Zespół nieadekwatnej syntezy wazopresyny
Zespół nieadekwatnej syntezy wazopresyny jest najczęstszą przyczyną hiponatremii przebiegającej z normowolemią. W zespole tym pierwotnym zaburzeniem jest nadmierne uwalnianie ADH, które prowadzi do zagęszczenia moczu, retencji wody w organizmie i wtórnej hiponatremii z rozcieńczenia. Każde zaburzenie w obrębie OUN może stymulować nadmierne wydzielanie ADH, w tym udar niedokrwienny lub krwotoczny mózgu, infekcje, zabiegi neurochirurgiczne czy zaburzenia psychiczne. Poza tym możliwa jest ektopowa synteza ADH, najczęściej opisywana w przebiegu raka drobnokomórkowego płuc. Do rozwoju SIADH może dojść również w wyniku stosowania różnych leków, np. karbamazepiny, cyklofosfamidu, cyprofloksacyny, haloperydolu, fluoksetyny i wielu innych. Spośród chorób zakaźnych nieobejmujących OUN SIADH najczęściej obserwuje się w przebiegu zapaleń płuc o różnej etiologii. Częstym czynnikiem wywołującym jest zakażenie prątkiem gruźlicy.12 Wtórnie do nadmiernej retencji wody w organizmie dochodzi do zwiększenia wydzielania peptydów natriuretycznych (ANP i BNP) i zwiększonej natriurezy, co przeciwdziała hiperwolemii, ale dodatkowo nasila hiponatremię. Mimo zwiększonej objętości płynu zewnątrz- i wewnątrzkomórkowego u chorych nie stwierdza się obrzęków. Objętość krwi krążącej jest prawidłowa. Stężenie ADH w surowicy również jest prawidłowe (lub zwiększone), mimo hipoosmolalności osocza, jednak jego pomiar nie ma większego znaczenia diagnostycznego dla rozpoznania, ponieważ wzrost stężenia ADH obserwuje się w wielu innych zaburzeniach. Jeśli hiponatremia rozwija się stopniowo, początkowo może nie dawać objawów klinicznych, ponieważ obraz kliniczny zależy od szybkości obniżania się stężenia sodu w surowicy. Jednak jeśli rozwija się w sposób ostry, to objawy kliniczne zwykle są obecne i obejmują m.in. bóle głowy, nudności, wymioty, zaburzenia świadomości i napady drgawkowe. Podstawą rozpoznania SIADH jest stwierdzenie hiponatremii ze współistniejącą niską efektywną osmolalnością osocza, zwiększoną osmolalnością moczu i zwiększonym wydalaniem sodu z moczem, przy wykluczeniu innych przyczyn hiponatremii (tab. 1). Stwierdzenie hipo- lub hiperwolemii uniemożliwia rozpoznanie. Przed postawieniem rozpoznania SIADH należy wykluczyć inne przyczyny hiponatremii, m.in. niewydolność serca, marskość wątroby, niedoczynność kory nadnerczy i tarczycy.13
Mózgowy zespół utraty soli
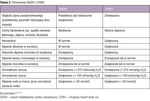
Mózgowy zespół utraty soli został po raz pierwszy opisany przez Petersa i wsp. w 1950 r.14 CSWS jest dość rzadko wymieniany w piśmiennictwie jako przyczyna hiponatremii. Dokładny patomechanizm zespołu jest nieznany, ale prawdopodobnie rozwija się wskutek zwiększonego uwalniania peptydów natriuretycznych (ANP i BNP) w przebiegu stanów powodujących zaburzenie funkcji OUN, co prowadzi do nadmiernej natriurezy i hiponatremii z hipowolemią. Wtórnie, w wyniku odwodnienia, dochodzi do zwiększenia wydzielania ADH. Uważa się, że CSWS występuje rzadko w przebiegu chorób OUN, jednak należy o nim pamiętać ze względu na odmienny od SIADH sposób leczenia. Poza tym częstość występowania CSWS może być niedoszacowana ze względu na rozpoznawanie części przypadków mylnie jako SIADH.13,15 Opisano przypadki CSWS m.in. w przebiegu krwotoku podpajęczynówkowego, zapalenia opon mózgowo-rdzeniowych, zapalenia mózgu, nowotworów OUN oraz jako skutek operacji neurochirurgicznych.16-20 W jednym z badań opisujących przyczyny hiponatremii około 6,5% przypadków było spowodowanych CSWS, a ponad 69% było wynikiem SIADH.16 Najczęstszą przyczyną zapalenia opon mózgowo-rdzeniowych, w przebiegu którego opisywano CSWS, było zakażenie prątkiem gruźlicy.21 Jak wspomniano, w przebiegu zespołu dochodzi do hiponatremii i zmniejszenia objętości płynu pozakomórkowego w wyniku utraty sodu z moczem, na skutek czego klinicznie obserwuje się cechy hipowolemii: m.in. obniżenie ciśnienia tętniczego (w tym ortostatyczne), tachykardię, obniżenie napięcia skóry i suchość śluzówek, zapadnięcie żył szyjnych, podwyższenie wartości hematokrytu. Hiponatremia stwierdzana w tym zespole jest zazwyczaj ciężka lub umiarkowana i zwykle pojawia się w ciągu 10 dni od zadziałania czynnika inicjującego (np. wystąpienia krwotoku podpajęczynówkowego lub zapalenia opon mózgowo-rdzeniowych), czasem później. Głównym zaburzeniem, z którym należy różnicować CSWS jest SIADH. W przebiegu CSWS objawy kliniczne spadku objętości płynu pozakomórkowego nie zawsze są widoczne i niestety nie istnieje żadne badanie biochemiczne, które pomogłoby jednoznacznie odróżnić CSWS od SIADH. W diagnostyce różnicowej obu zespołów można również wziąć pod uwagę odpowiedź na wlew izotonicznego roztworu NaCl. W przypadku CSWS, po podaniu izotonicznego roztworu NaCl następuje przywrócenie normowolemii, rozcieńczenie moczu (hamowanie stymulowanego hipowolemią uwalniania ADH) i korekta hiponatremii. Z kolei w przypadku SIADH wlew izotonicznego roztworu NaCl zwykle nasila hiponatremię.9,13,15 Porównanie zespołów SIADH i CSWS przedstawiono w tabeli 2.
Leczenie
Jednym z podstawowych elementów leczenia hiponatremii jest rozpoznanie czynnika przyczynowego, ponieważ leczenie zależy od mechanizmu patofizjologicznego, który wywołuje hiponatremię. Ogólnie mówiąc, w SIADH zasadnicze znaczenie ma rygorystyczne ograniczenie przyjmowanych płynów oraz uzupełnianie niedoborów sodu, natomiast w CSWS zaleca się odpowiednie nawodnianie.
Postępowanie w SIADH
Postępowanie lecznicze w SIADH zależy od ciężkości hiponatremii oraz obecności objawów klinicznych. Podstawowe elementy leczenia SIADH to leczenie przyczynowe choroby wywołującej oraz zwiększenie i utrzymanie prawidłowego stężenia sodu w surowicy. Podstawą leczenia jest ograniczenie spożycia płynów do <1000 ml na dobę.
U pacjentów z hiponatremią klasyfikowaną jako ciężka (<125 mmol/l) wraz ze współistniejącymi ciężkimi objawami neurologicznymi (np. drgawkami, sennością lub śpiączką) lub u pacjentów z objawową hiponatremią w przebiegu chorób OUN zaleca się niezwłoczne podanie hipertonicznego 3% roztworu chlorku sodu w ilości 100 ml w dożylnym bolusie trwającym 15-20 minut. Powinno to skutkować wzrostem stężenia sodu w surowicy o 1,5-2 mmol/l i zmniejszeniem nasilenia objawów neurologicznych. Jeśli nie uzyskano odpowiedzi na tę dawkę, można ją powtórzyć 2-3-krotnie w odstępach 10-minutowych.22 Natychmiastowy wlew hipertonicznego roztworu NaCl może uratować życie. W przypadku braku 3% roztworu NaCl można zastosować roztwór 10%, rozcieńczając go 5% roztworem glukozy w stosunku objętościowym 1:2. Dzięki temu otrzyma się roztwór 3,3%. Roztwór 3% można otrzymać, mieszając 30 ml 10% roztworu NaCl z 100 ml 0,9% roztworu NaCl.23 Korekta hiponatremii nie powinna przekraczać 10 mmol/l w ciągu pierwszych 24 godzin oraz 18 mmol/l w ciągu 48 godzin. Zbyt szybkie zwiększanie stężenia sodu może doprowadzić do demielinizacji osmotycznej (zwłaszcza gdy stężenie sodu wynosi ≤120 mmol/l). Stężenie sodu w surowicy należy kontrolować co 2-3 godziny do czasu uzyskania stabilizacji stanu pacjenta. U pacjentów z osmolalnością moczu przekraczającą dwukrotnie wartość osmolalności osocza (zwykle gdy osmolalność moczu przekracza 500 mOsm/kg) dodatkowo zaleca się włączenie diuretyku pętlowego (np. furosemidu) w celu zwiększenia rozcieńczenia moczu.2,22
Pacjenci z przewlekłą i łagodną hiponatremią bez objawów klinicznych zwykle nie wymagają intensywnego leczenia. Wystarczające jest ograniczenie ilości przyjmowanych płynów. Ponadto w piśmiennictwie wspomina się o terapii przy użyciu antagonistów receptora wazopresyny (V2) – tzw. waptanów (liksywaptan, tolwaptan), które w dotychczas opublikowanych badaniach okazywały się bezpieczne i skuteczne w leczeniu hiponatremii przebiegającej z normowolemią.24 Waptany nasilają wydalanie wolnej wody, bez wpływu na wydalanie elektrolitów, co prowadzi do wzrostu stężenia sodu w surowicy. Tolwaptan ze względu na potencjalne działania hepatotoksyczne nie powinien być stosowany dłużej niż 30 dni oraz u pacjentów z chorobami wątroby. Leki te nie mogą być stosowane w CSWS.22