Zaburzenia rytmu i przewodzenia
Kamizelka ICD – wskazania, dotychczasowe doświadczenia, perspektywy i ograniczenia
dr hab. n. med. Jerzy Krzysztof Wranicz, prof. nadzw. UM
mgr Anna Nowek
Wprowadzenie
Implantowane kardiowertery-defibrylatory (implantable cardioverter-defibrillator, ICD) są powszechnie stosowanymi urządzeniami ratującymi życie pacjentów zagrożonych nagłym zgonem sercowym, chociaż wykazano, że nie są one użyteczne u pacjentów w początkowym okresie po zawale serca. Ponadto nie zaleca się ich stosowania w przypadku nowo zdiagnozowanej kardiomiopatii, bezpośrednio po zabiegach rewaskularyzacyjnych mięśnia sercowego oraz bezpośrednio po usunięciu układu ICD w przebiegu odelektrodowego zapalenia wsierdzia (cardiac device infective endocarditis, CDIE). Sytuacje, gdy zabezpieczenie chorego ma charakter czasowy, a implantacja elektrod endokawitarnych jest niemożliwa, uzasadniają potrzebę stosowania nieinwazyjnych urządzeń ratujących życie, jakimi są kamizelki ICD.
Nagła śmierć sercowa – stratyfikacja ryzyka
Nagła śmierć sercowa (sudden cardiac death, SCD) to poważny problem zdrowia publicznego dotykający znacznej liczby chorych często jeszcze w sile wieku, który wywiera niekorzystny wpływ psychospołeczny na społeczeństwo. Ocena ryzyka SCD oraz jej profilaktyka stanowią wyzwanie dla medycyny, a zwłaszcza dla współczesnej kardiologii. Mimo że w ciągu ostatnich dwudziestu lat śmiertelność z powodu przyczyn sercowych w krajach uprzemysłowionych zmniejszyła się, nadal ok. 20% wszystkich zgonów stanowią zgony nagłe – najczęściej z powodu migotania komór lub asystolii.1-4 Szacuje się, że w Unii Europejskiej i Stanach Zjednoczonych w wyniku SCD umiera 10 razy więcej osób niż w wypadkach komunikacyjnych, co pokazuje ogrom problemu. Do SCD dochodzi w różnych grupach populacyjnych – głównie u osób bez wywiadu w kierunku choroby serca (mała przewidywalność) lub z łagodną dysfunkcją serca (ograniczona przewidywalność) oraz rzadziej u chorych z ciężką niewydolnością serca (możliwa przewidywalność) lub genetycznie obciążonych arytmogennie (ryc. 1).
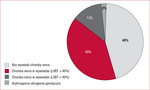
Rycina 1. Odsetek występowania nagłej śmierci sercowej w zależności od wywiadu choroby serca.5 LVEF – frakcja wyrzutowa lewej komory
Identyfikację i ocenę czynników ryzyka SCD znacznie utrudnia fakt, że w blisko 50% SCD jest pierwszym zdarzeniem klinicznym wśród osób bez wywiadu choroby serca.6 Wystąpienie istotnych zdarzeń sercowo-naczyniowych (m.in. nagłe zatrzymanie krążenia, rozpoznanie niewydolności serca, niestabilna choroba wieńcowa) nie zwiększa liniowo ryzyka SCD – jest ono największe w ciągu pierwszych 6-18 miesięcy od zdarzenia.7 Najwyższą śmiertelność obserwuje się u pacjentów w pierwszym miesiącu po zawale serca z frakcją wyrzutową poniżej 30%.8 Ryzyko wystąpienia SCD zwiększa się również z wiekiem – jest ono 100 razy niższe w grupie do 30 roku życia niż wśród osób po 35 roku życia.9,10 Dodatkowo zaobserwowano dużą dysproporcję między częstością występowania nagłej śmierci sercowej – w grupie osób młodych i w średnim wieku częstość SCD jest wyższa u mężczyzn niż u kobiet, między innymi ze względu na występujące przed menopauzą hormonalne czynniki chroniące przed miażdżycą tętnic.11 Niektóre badania wykazały również różnice wynikające z rasy: wyższym ryzykiem SCD są obciążone osoby rasy czarnej w porównaniu z osobami rasy białej.12 Ważnymi czynnikami ryzyka są m.in. nadciśnienie tętnicze, przerost lewej komory widoczny w zapisie elektrokardiograficznym i badaniu echokardiograficznym, zaburzenia przewodzenia międzykomorowego, takie jak blok lewej odnogi.13 Nie bez znaczenia jest również styl życia. Nagła śmierć sercowa występuje częściej u osób otyłych i palących tytoń (2-3 razy częściej niż u osób, które nie palą).14 Warto dodać, że wykazano zależność między występowaniem czynników stresogennych i istotnych zmian w życiu (osobistym i społecznym) a wystąpieniem zawału mięśnia sercowego i SCD – najczęściej do zmian tych dochodziło w ciągu 6 miesięcy przed zdarzeniem klinicznym.15,16
Złożoność problemu nagłej śmierci sercowej i różnorodność czynników ryzyka jej wystąpienia pokazuje jak istotne jest zgłębianie tego tematu i podejmowanie działań profilaktycznych.
Profilaktyka bezpośrednia SCD to implantacja ICD, która najlepiej ze wszystkich metod chroni chorych przed zgonem w wyniku groźnych dla życia arytmii, zwłaszcza u chorych, którzy przebyli incydent nagłego zatrzymania krążenia oraz tych, u których nie doszło jeszcze do tego zdarzenia, ale istnieje u nich wysokie prawdopodobieństwo wystąpienia SCD.
Grupa pierwsza to chorzy, u których implantacja ICD, poza nielicznymi wyjątkami, nie podlega dyskusji. Grupa druga to chorzy, u których na podstawie czynników ryzyka ustalamy wskazania do implantacji ICD w tzw. profilaktyce pierwotnej, a więc staramy się zapobiec SCD.
Najważniejsze zagadnienia to skuteczna identyfikacja potencjalnych ofiar zatrzymania krążenia przed wystąpieniem zdarzenia. Oczywiście nie zawsze jesteśmy w stanie zidentyfikować właściwie grupę zagrożoną SCD, dlatego ważna jest edukacja społeczeństwa w zakresie podstaw reanimacji oraz możliwych modyfikowalnych czynników ryzyka. Mimo licznych badań dotyczących stratyfikacji ryzyka SCD, nadal brakuje prostych i wiarygodnych wskaźników pomocnych w identyfikacji osób zagrożonych SCD oraz kwalifikacji do implantacji ICD w ramach profilaktyki pierwotnej, poza oceną frakcji wyrzutowej lewej komory (LVEF), zaawansowania niewydolności serca ocenianego za pomocą klasyfikacji NYHA oraz pojedynczych wskaźników elektrokardiograficznych.
Historia kamizelki ICD
Pierwszej implantacji kardiowertera dokonał w 1980 r. dr Michel Mirowski – wówczas jeszcze drogą torakotomii. Przez lata ICD ulegało ewolucji, aby obecnie można go było implantować podskórnie, a elektrody drogą przezżylną – jak przy implantacji układów stymulujących serce.
Paradoksalnie rozwój elektroterapii przez wprowadzenie dwóch i trzech elektrod do jam serca oraz konieczność licznych reimplantacji u chorych żyjących coraz dłużej prowadzi do powikłań infekcyjnych, których skutkiem jest wzrost liczby usuwanych układów. Rosnąca wiedza na temat powikłań infekcyjnych u chorych z wszczepionymi ICD ukazała potrzebę opracowania systemu pozwalającego na czasowe zabezpieczenie chorego przed SCD, podobnie jak ma to miejsce w przypadku stymulatorów do czasowej stymulacji serca chroniących przed zbyt głęboką bradykardią. Również inne odwracalne przyczyny spadku frakcji wyrzutowej u chorych rokujących na jej normalizację po wdrożeniu właściwego leczenia to grupa, która może wymagać czasowego zabezpieczenia przed incydentami arytmicznymi prowadzącymi do SCD.
Dopiero w 1998 roku Angelo Auricchio opublikował wstępne wyniki badania dotyczące zewnętrznego, noszonego przez chorego urządzenia – tzw. kamizelki ICD (wearable cardioverter-defibrillator, WCD). Badana grupa złożona była z 15 osób, które przeżyły nagłe zatrzymanie krążenia w wyniku częstoskurczu komorowego i/lub migotania komór.17 Wykorzystane urządzenie było wyposażone w cztery elektrody odczytujące sygnał EKG oraz 3 elektrody defibrylujące umieszczone w kamizelce założonej przez pacjenta. Badanie przeprowadzono w laboratorium elektrofizjologicznym w warunkach tzw. płytkiej sedacji. Maksymalna energia wyładowania możliwego do dostarczenia przez defibrylator wynosiła 285 J. W celu przerwania wyindukowanej arytmii komorowej zastosowano u pacjentów wyładowanie o energii 230 J. Pojedyncze wyładowanie o tej mocy skutecznie przerwało arytmię w 10 przypadkach – w 9 na 10 urządzenie prawidłowo rozpoznało arytmię, a w jednym przypadku nie została ona wykryta ze względu na rozłączenie się elektrod odczytujących EKG w trakcie indukcji arytmii.
Kolejnym krokiem było sprawdzenie zastosowania urządzenia poza pracownią elektrofizjologiczną.18 Zostało ono umieszczone w kamizelce z elektrodami do monitorowania zapisu EKG oraz elektrodami defibrylującymi połączonymi z monitorem i systemem alarmującym. Dane były przesyłane z domu pacjenta przez transmiter i modem do szpitala. Urządzenie ważyło ok. 1500 g i mogło dostarczyć maksymalne wyładowanie o energii 285 J. W badaniu wzięło udział 39 pacjentów. U 17 osób frakcja wyrzutowa lewej komory wynosiła poniżej 30%, u 16 zarejestrowano nieutrwalone częstoskurcze komorowe (non-sustained ventricular tachycardia, nsVT), a 6 przebyło migotanie komór w związku ze świeżym zawałem serca. Wszystkie epizody nsVT zostały prawidłowo rozpoznane przez urządzenie, a mimo alarmów na poziomie 15%, wynikających z artefaktów, żaden z pacjentów nie doświadczył nieadekwatnej interwencji. Trzy z 4 epizodów arytmii komorowej zostały prawidłowo rozpoznane i zakończone dzięki wyładowaniu dostarczonemu przez defibrylator – u 2 z tych pacjentów w rezultacie wszczepiono ICD.
Amerykańska FDA po raz pierwszy dopuściła kamizelkę ICD do stosowania w 2002 roku. Urządzenie miało być noszone przez całą dobę prócz czasu przeznaczonego na prysznic lub kąpiel. Użytkownik kamizelki musiał raz w tygodniu przesyłać dane zgromadzone przez urządzenie do szpitala za pomocą modemu.

