III Kongres Akademii po Dyplomie Okulistyka już w ten piątek! Kup bilet i dołącz do ekspertów podczas Siatkówka Meeting! Sprawdź >
Postępowaniem z wyboru u chorych z OZW i wysoką glikemią jest dożylne podanie insuliny, pozwalające na szybką normalizację stężenia glukozy i łatwe nim sterowanie. Dotychczas nie sprecyzowano ostatecznie i jednoznacznie docelowych stężeń glukozy w OZW. Skuteczność leczenia insuliną w OZW u chorych na cukrzycę oceniano w badaniach Diabetes and Insulin-Glucose Infusion in Acute Myocardial Infarction (DIGAMI 1 i 2) oraz badaniu Hyperglycaemia; Intensive Insulin Infusion in Infarction (HI-5). Badanie DIGAMI 1 przeprowadzono na grupie 620 pacjentów z cukrzycą i OZW. Wykazano w nim, że wlew insuliny i glukozy przez pierwsze 24 godz., a następnie intensywna insulinoterapia w modelu wielokrotnych wstrzyknięć przez minimum 3 miesiące w porównaniu z konwencjonalną terapią istotnie zmniejszają śmiertelność po roku i po 3 latach obserwacji.11
Wnioski te nie znalazły jednak potwierdzenia w podobnie zaprojektowanym badaniu DIGAMI 2, w którym nie udowodniono korzystnego wpływu intensywnej insulinoterapii na rokowanie w porównaniu z terapią standardową (18,4% vs 17,3%).12 Brak powtarzalności rezultatów tych badań może wynikać z niemożności osiągnięcia docelowego wyrównania metabolicznego w grupie leczonej intensywnie w badaniu DIGAMI 2 oraz z większej względnej redukcji stężenia hemoglobiny glikowanej (HbA1C) w badaniu DIGAMI 1. Podobnie autorzy badania HI-5 nie wykazali redukcji śmiertelności (4,8 vs 3,5%) u pacjentów leczonych wlewem insuliny i dekstrozy w porównaniu z klasyczną terapią.13
W aktualnych wytycznych (2017 r.) European Society of Cardiology (ESC) dotyczących postępowania w STEMI proponuje się w ostrej fazie OZW „ścisłą, ale niezbyt ścisłą” kontrolę glikemii z utrzymaniem stężenia glukozy <11 mmol/l lub 200 mg/dl.10 Mniej rygorystyczną kontrolę glikemii należy rozważyć u starszych chorych, z wieloletnią cukrzycą, zaawansowaną chorobą wieńcową i wieloma chorobami towarzyszącymi (klasa zaleceń IIa, poziom dowodu C). Tak sformułowane zalecenia wskazują na konieczność zbilansowania korzyści wynikających z redukcji stężenia glukozy z ryzykiem prowokowania hipoglikemii, która również pogarsza rokowanie w OZW.
Więcej praktycznych wskazówek znajduje się w corocznie publikowanych zaleceniach Polskiego Towarzystwa Diabetologicznego (PTD) dotyczących postępowania u chorych na cukrzycę.14 W dokumencie tym jednoznacznie określono wartości progowe glikemii, od których należy rozpoczynać insulinoterapię w ostrej fazie OZW. Są to stężenia glukozy >140 mg/dl u osób z wcześniej rozpoznaną cukrzycą lub >180 mg/dl u pozostałych chorych. Jeśli te progi są przekroczone, trzeba rozpocząć dożylny wlew insuliny z równoczesnym wlewem glukozy o odpowiedniej kaloryczności wg schematu podanego w tabeli 1. Jest to najszybszy i najbezpieczniejszy sposób uzyskania normoglikemii, ale warunkiem skuteczności i bezpieczeństwa tego schematu jest częste kontrolowanie glikemii (początkowo co godzinę, następnie co 2 godz., po stabilizacji glikemii) i stężenia potasu. Docelowe stężenia glukozy w trakcie wlewu insuliny to 100-180 mg/dl (5,6-10 mmol/l). Pacjentom spożywającym posiłek należy dodatkowo dostrzyknąć dożylnie insulinę krótko działającą. Jeśli glikemia wynosi >180 mg/dl (10 mmol/l), zaleca się czasowe przerwanie dożylnego wlewu glukozy i powrót do tej terapii po obniżeniu glikemii <180 mg/dl ze zwiększeniem wlewu insuliny.
Istnieje wiele doniesień wskazujących na niebezpieczeństwo związane z wywołaniem hipoglikemii u chorego z OZW. Jej powodem jest najczęściej zbyt intensywna terapia insuliną. W badaniu GRACE zauważono, że nie tylko epizody hiperglikemii, ale również hipoglikemia wiąże się z niepomyślnym rokowaniem.9 W dużym, wieloośrodkowym badaniu Normoglycemia in Intensive Care Evaluation-Survival Using Glucose Al-
gorithm Regulation (NICE-SUGAR) 6104 pacjentów leczonych na oddziałach intensywnej terapii przydzielono losowo do 2 grup. W pierwszej grupie stosowano ścisłą kontrolę glikemii, dążąc do wartości w zakresie 81-108 mg/dl (4,5-6,0 mmol/l), w 2 – konwencjonalną kontrolę glikemii do wartości 180 mg/dl lub niższej (≤10 mmol/l). W obu grupach stosowano dożylny wlew insuliny. W grupie leczonej konwencjonalnie insulinę podawano dopiero przy stężeniach glukozy >180 mg/dl i zatrzymywano wlew po jej obniżeniu do <144 mg/dl (8,0 mmol/l). Odnotowano istotnie wyższą 90-dniową śmiertelność w grupie, w której wdrożono intensywną terapię insuliną (27,5% vs 24,9%; p=0,02), a najczęstszą przyczyną zgonów były powikłania sercowo-naczyniowe. Epizody ciężkich hipoglikemii (glikemia ≤40 mg/dl; 2,2 mmol/l) występowały częściej u pacjentów, u których włączono intensywną terapię insuliną (6,8 vs 0,5%).15
W innym badaniu, przeprowadzonym na grupie 130 chorych z OZW i hiperglikemią (BIOMArCS-2 – BIOMarker study to identify the acute risk of a coronary syndrome-2), nie stwierdzono korzyści w zakresie zmniejszenia obszaru zawału u pacjentów poddanych intensywnej terapii insuliną. Złożony parametr oceny końcowej, tj. zgon lub ponowny zawał mięśnia sercowego, był nawet częstszy w tej grupie chorych.16
Niekorzystny wpływ hipoglikemii na układ krążenia w OZW wynika głównie ze wzmożonej aktywacji układu adrenergicznego, co przyczynia się do nasilenia niedokrwienia mięśnia sercowego. Ponadto hipoglikemia odpowiada za zjawisko proarytmii: odstęp QT się wydłuża, zmienia się morfologia załamka T, wskutek pobudzenia układu współczulnego kardiomiocyt jest przeładowany wapniem. Powstają idealne warunki do wyzwolenia ektopii komorowej, mogącej łatwo przekształcić się w groźne formy zaburzeń rytmu serca.17 Podsumowując, można przyjąć, że aby ograniczyć ryzyko hipoglikemii, w ostrej fazie OZW docelowe stężenia glukozy nie powinny być niższe niż 90 mg/dl.1
Od 2 doby OZW dożylny wlew insuliny należy zamienić na insulinoterapię w modelu wielokrotnych wstrzyknięć podskórnych. Można zastosować insulinę krótko działającą albo analog szybko działający przed posiłkami i insulinę izofanową o przedłużonym działaniu (NPH – neutral protamine Hagedorn; obojętna insulina protaminowa Hagedorna), albo analog długo działający przed snem i/lub w godzinach porannych. Duże zapotrzebowanie na insulinę (przekraczające 100 j./24 godz.) świadczy o insulinooporności. Aby przełamać to niekorzystne zjawisko, należy rozważyć przedłużenie dożylnego wlewu insuliny do 72-96 godz. Docelowe wartości glikemii wg zaleceń PTD to 100-180 mg/dl (5,6-10 mmol/l).14 Pacjenci, którzy przed wystąpieniem OZW byli skutecznie leczeni wyłącznie metforminą, lub chorzy, u których hiperglikemię rozpoznano po raz pierwszy w pierwszej dobie OZW, ale bez cech kwasicy, w pierwszych dobach mogą być leczeni wyłącznie dietą. W cukrzycy typu 2 metforminę można włączyć już w 3 dobie po interwencji wieńcowej w OZW, po uwzględnieniu ewentualnych przeciwwskazań.
Ocena parametrów wydolności nerek (stężenie kreatyniny/współczynnik przesączania kłębuszkowego [GFR – glomerular filtration rate]) jest integralnym elementem diagnostyki chorego z OZW. Wyniki tych badań są szczególnie istotne u pacjentów, którzy bezpośrednio przed koronarografią/przezskórną interwencją wieńcową byli leczeni metforminą i/lub inhibitorem kotransportera sodowo-glukozowego typu 2 (SGLT2 – sodium-glucose cotransporter 2). W tej grupie chorych ocena funkcji nerek powinna być powtarzana przez co najmniej 3 dni po zabiegach inwazyjnych (klasa zaleceń I/poziom dowodu C).9
Od 1960 r. popularne jest stosowanie mieszanki polaryzującej, tj. wlewu glukozy, insuliny, potasu (GIK). Pomysł ten opiera się na przekonaniu, że podaż egzogennej insuliny zmniejsza stężenie krążących FFA. Glukoza stanowi substrat energetyczny dla niedokrwionego miokardium, a suplementacja potasu stabilizuje błony komórkowe kardiomiocytów. Podawanie GIK w OZW niezależnie od stężenia glukozy było przedmiotem wielu badań. Teoretyczny korzystny wpływ GIK na niedokrwione komórki mięśnia sercowego nie został potwierdzony w wieloośrodkowym badaniu Clinical Trial of MEtabolic Modulation in Acute Myocardial Infarction Treatment Evaluation-Estudios Cardiologicos Latinoamerica (CREATE-ECLA), w którym wzięło udział ponad 20 000 pacjentów ze STEMI.18 Immediate Myocardial Metabolic Enhancement During Initial Assessment and Treatment in Emergency Care (IMMEDIATE) – kolejne badanie z wlewem GIK – zaprojektowano tak, by podaż GIK nastąpiła w momencie podejrzenia OZW, jeszcze na etapie przedszpitalnym. Wykazało ono korzystny wpływ GIK na częstość zaburzeń rytmu serca lub nagłego zatrzymania krążenia w trakcie hospitalizacji w porównaniu z placebo. Autorzy badania nie udowodnili jednak, aby wlew GIK ograniczał progresję do zawału mięśnia sercowego czy zmniejszał 30-dniową śmiertelność po OZW.19 W związku z tym rutynowy wlew GIK nie jest obecnie zalecany.
Leczenie hipoglikemizujące po zakończeniu hospitalizacji
Schemat dalszego leczenia hipoglikemizującego u pacjentów z OZW i cukrzycą typu 2 ustala się na podstawie dobowego zapotrzebowania na insulinę i stopnia wyrównania metabolicznego. Jeżeli u pacjenta z wcześniej rozpoznaną cukrzycą typu 2 udało się uzyskać docelowe stężenia glikemii przy zapotrzebowaniu na insulinę <30 j./24 h, można powrócić do leczenia hipoglikemizującego sprzed OZW. Chorym niespełniającym tych warunków (glikemia >180 mg/dl lub zapotrzebowanie na insulinę >30 j./24 h) należy zaproponować insulinoterapię również w warunkach domowych.
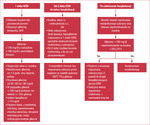
Algorytm postępowania terapeutycznego u pacjentów z OZW i hiperglikemią zaprezentowano na rycinie 1.
Jak wspomniano wyżej, OZW nierzadko bywa momentem, kiedy po raz pierwszy ustalane jest rozpoznanie cukrzycy, chociaż choroba mogła bezobjawowo przebiegać już od dłuższego czasu. Dlatego konieczna jest aktywna diagnostyka w kierunku wykrywania zaburzeń gospodarki węglowodanowej. U każdego pacjenta z OZW (poza chorymi z już rozpoznaną cukrzycą) przed wypisem ze szpitala powinno się wykonać doustny test obciążenia glukozą (OGTT – oral glucose tolerance test). Jeśli zostanie rozpoznana cukrzyca typu 2 skojarzona z nadwagą lub otyłością, ale z zapotrzebowaniem na insulinę <30 j./24 h i glikemiami <180 mg/dl, można rozpocząć leczenie od metforminy, ewentualnie w połączeniu z innym lekiem hipoglikemizującym. Ogólnym celem terapii hipoglikemizującej jest uzyskanie stężenia HbA1C ≤7%, co odpowiada stężeniom glukozy na czczo 80-130 mg/dl, a po posiłkach <180 mg/dl. U pacjentów w zaawansowanym wieku z powikłaniami o charakterze makroangiopatii i/lub z licznymi chorobami towarzyszącymi za zadowalające uważa się stężenia HbA1C ≤8%.14
Duże nadzieje w zakresie redukcji powikłań sercowo-naczyniowych pokładano w nowych lekach hipoglikemizujących, takich jak: analogi glukagonopodobnego peptydu typu 1 (GLP-1 – glucagon-like peptide 1), inhibitory peptydazy dipeptydylowej 4 (DPP-4 – dipeptidyl peptidase 4) czy inhibitory SGLT2. Większość badań nie potwierdziła jednak kardioprotekcyjnego działania tych leków.20 Analog GLP-1, eksenatyd, redukował wprawdzie aż o 30% obszar zawału mięśnia sercowego u pacjentów ze STEMI ale tylko wówczas, gdy był włączany w ciągu <132 min od wystąpienia objawów.21
Obecnie duże zainteresowanie budzi empagliflozyna. Ten inhibitor SGLT2 hamuje reabsorpcję glukozy w kanalikach nerkowych, powodując glukozurię. Ostatnio opublikowano wyniki badania BI 10773 (Empagliflozin) Cardiovascular Outcome Event Trial in Type 2 Diabetes Mellitus Patients (EMPA-REG OUTCOME), w którym oceniano skuteczność leczenia empagliflozyną dołączoną do standardowej terapii u pacjentów obciążonych wysokim ryzykiem sercowo-naczyniowym. W analizie tej wykazano 14% redukcję pierwotnego punktu końcowego (śmierć z przyczyn sercowo-naczyniowych, zawał mięśnia sercowego czy udar niezakończony zgonem) i 32% redukcję śmiertelności ogólnej. Autorzy badania postulują istnienie wielu mechanizmów działania leku korzystnych z punktu widzenia układu krążenia, takich jak: spadek aktywacji współczulnej, ograniczenie zapotrzebowania mięśnia sercowego na tlen, zmniejszenie sztywności ściany naczyniowej, albuminurii i stężenia kwasu moczowego oraz redukcja masy ciała.22