Zastosowano leczenie heparyną niefrakcjonowaną w stałym wlewie dożylnym z docelowym APTT 1,5-2,5 wartości prawidłowej, kontynuowano leczenie przeciwbakteryjne i tlenoterapię. W ciągu kilku dni stan chorego uległ znaczącej poprawie, krwioplucie ustąpiło całkowicie. Włączono doustny lek przeciwzakrzepowy. W kontrolnym RTG klatki piersiowej zaobserwowano ustąpienie płynu w jamach opłucnowych i zmniejszenie zmian miąższowych w prawym płucu. Przeprowadzono dalszą diagnostykę w kierunku choroby nowotworowej: PSA całkowite, kał na krew utajoną (trzykrotnie), USG jamy brzusznej. Wyniki badań były prawidłowe. Rozpoznano ostatecznie ostrą zatorowość płucną niewysokiego ryzyka zgonu w przebiegu zakrzepicy żył głębokich kończyny dolnej prawej, powikłaną zawałem płuca i prawostronnym zapaleniem płuc. Przy wypisie ze szpitala zalecono acenokumarol, z docelowym INR 2,5 (2,0-3,0), omeprazol 1 × 20 mg/24 h doustnie i pończochy o stopniowanym ucisku (stopień ucisku 2).
Dyskusja
Prezentowany przypadek kliniczny stanowił wyzwanie zarówno diagnostyczne, jak i terapeutyczne. Do rzadkich, ale poważnych przyczyn krwioplucia należy zatorowość płucna (ZP).1 Najczęstszą statystycznie przyczyną tego objawu u chorego zgłaszającego się do szpitala są jednak rozstrzenie oskrzeli, następnie nowotwory pierwotne lub przerzutowe płuc, co jest wynikiem nacieku przez nieprawidłowe komórki guza otaczających tkanek i nowotworzenia naczyń. W zapaleniu oskrzeli lub płuc krwioplucie wywołane jest tworzeniem się miejscowego stanu zapalnego i proliferacją łatwo krwawiących naczyń. Kolejną częstą przyczyną krwioplucia jest wzrost ciśnienia w lewym przedsionku serca oraz wtórnie w tętnicy płucnej i naczyniach oskrzelowych płuc odchodzących od aorty, co może powodować krwioplucie w stenozie mitralnej czy innych chorobach prowadzących do lewokomorowej niewydolności serca. Znacznie rzadszą przyczyną tego objawu w naszej szerokości geograficznej, ale częstą w krajach rozwijających się, jest gruźlica płuc.1 Możliwe przyczyny krwioplucia zebrano w tabeli 1.1
Tabela 1.
|
Przyczyny krwioplucia1 |
|
|
Rozstrzenie oskrzeli |
20% |
|
Rak płuca, pierwotny i przerzutowy* |
19% |
|
Zapalenie oskrzeli |
18% |
|
Zapalenie płuc |
16% |
|
Skaza krwotoczna** |
4% |
|
Niewydolność lewokomorowa serca |
4% |
|
Zatorowość płucna |
2% |
|
Stenoza mitralna |
1% |
|
Gruźlica |
1% |
|
Nadciśnienie tętnicze systemowe |
1% |
|
Nadciśnienie płucne |
1% |
|
Zapalenie naczyń |
1% |
|
Uraz |
1% |
|
Inne |
1% |
*Rak sutka, krtani, czerniak, chłoniak.
**Pierwotna i wtórna, np. przedawkowanie leków przeciwzakrzepowych.
Krwioplucie nie było jedynym objawem zgłaszanym przez pacjenta. Nagła duszność, ból w klatce piersiowej o charakterze opłucnowym powinny nakierować lekarza badającego na inne alternatywne rozpoznania. Kiedy pogłębiono wywiad, okazało się, że niewielki obrzęk kończyny dolnej prawej pacjent obserwował już od pierwszych dni choroby, ale nie zgłaszał tego objawu lekarzowi, gdyż myślał, że jest nieistotny, a nie został o to zapytany. Brak obfitego odkrztuszania przemawia raczej przeciwko rozstrzeniom oskrzeli, a brak produktywnego kaszlu z odkrztuszaniem ropnej plwociny jako objawu towarzyszącego krwiopluciu – przeciwko zapaleniu płuc czy oskrzeli. W lewokomorowej niewydolności serca spodziewalibyśmy się odkrztuszania pienistej różowej wydzieliny i innych objawów sugerujących niewydolność serca. Pacjent odkrztuszał niewielkie ilości świeżej krwi, co raczej obserwuje się w nowotworach, zatorowości płucnej, gruźlicy płuc, malformacjach tętniczo-żylnych lub skazach krwotocznych.2
Należy pamiętać, że krwioplucie może być jednym z pierwszych objawów zatorowości płucnej, choroby, której podejrzenie obliguje do innej strategii diagnostycznej i zupełnie innego sposobu leczenia niż w przypadku innych przyczyn krwioplucia. Krwioplucie występuje u około 11% pacjentów zgłaszających się do szpitala, u których następnie potwierdza się zatorowość płucną.3 Krwioplucie w ZP towarzyszy najczęściej tzw. „zespołowi objawów zawału płuca”, w którym dochodzi do zawału na skutek nagłego zamknięcia drobnych dystalnych tętnic płucnych przez materiał zatorowy i wtórnie do krwawienia śródpęcherzykowego w tej okolicy. Do typowych elementów tego zespołu należy: ból w klatce piersiowej o charakterze opłucnowym, wynikający z podrażnienia opłucnej i typowy obraz radiologiczny w RTG lub TK klatki piersiowej.3,4 Gdy dojdzie do nagłego pęknięcia drobnych naczyń okołooskrzelowych, może dodatkowo pojawić się krwioplucie. Nagła duszność nie jest dla tego zespołu typowa i świadczy o bardziej centralnej lokalizacji zmian zatorowych.4 Częstość występowania objawów klinicznych u chorych, u których potwierdzono ZP, przedstawiono w tabeli 2.
Tabela 2.
|
Częstość występowania poszczególnych objawów klinicznych u pacjentów zgłaszających się do szpitala, u których potwierdzono zatorowość płucną (n=219)3 |
|
|
Objawy podmiotowe |
|
|
Duszność |
80% |
|
Ból w klatce piersiowej opłucnowy |
52% |
|
Kaszel |
20% |
|
Omdlenie |
19% |
|
Ból w klatce piersiowej wieńcowy |
12% |
|
Krwioplucie |
11% |
|
Objawy przedmiotowe |
|
|
Tachypnoe ≥20/min |
70% |
|
Tachykardia >100/min |
26% |
|
Objawy zakrzepicy żył głębokich |
15% |
|
Sinica |
11% |
|
Gorączka >38,5°C |
7% |
Strata czasu związana z niewłaściwym rozpoznaniem wstępnym, a co za tym idzie opóźnionym włączeniem leczenia przeciwzakrzepowego, może skutkować nawrotem ZP, destabilizacją stanu klinicznego pacjenta i istotnym zwiększeniem ryzyka zgonu. Dlatego tak ważne jest, aby uwzględniać tę chorobę w diagnostyce różnicowej. Żylna choroba zakrzepowo-zatorowa sprawia trudności diagnostyczne z uwagi na nieswoistość objawów. Aktualnie obowiązujące strategie diagnostyczne, zawarte w wytycznych European Society of Cardiology, zaakceptowane przez Polskie Towarzystwo Kardiologiczne, opierają się na prostych schematach, pozwalających na szybkie podjęcie decyzji klinicznych. W diagnostyce ZP wykorzystuje się ocenę stanu klinicznego pacjenta, skalę klinicznego prawdopodobieństwa ZP (genewską, którą przedstawiono w tabeli 3, lub Wellsa) oraz odpowiednio dobrane badania dodatkowe: oznaczenie stężenia dimera D, spiralną tomografię komputerową klatki piersiowej uzupełnioną w szczególnych przypadkach o badanie ultrasonograficzne żył kończyn dolnych.
Tabela 3.
|
Zmodyfikowana skala genewska w ocenie prawdopodobieństwa klinicznego zatorowości płucnej4 |
|
|
Parametr |
Punkty |
|
Czynniki predysponujące |
|
|
Wiek >65 lat |
+1 |
|
Przebyta zakrzepica żył głębokich kończyn dolnych lub zatorowość płucna |
+3 |
|
Operacja chirurgiczna lub złamanie ≤1 mies. |
+2 |
|
Aktywny nowotwór złośliwy |
+2 |
|
Objawy podmiotowe |
|
|
Jednostronny ból kończyny dolnej |
+3 |
|
Krwioplucie |
+2 |
|
Objawy przedmiotowe |
|
|
Częstość rytmu serca ≥95/min |
+5 |
|
Częstość rytmu serca 75-94/min |
+3 |
|
Jednostronny obrzęk kończyny dolnej lub ból żył głębokich kończyny dolnej podczas palpacji |
+4 |
|
Prawdopodobieństwo kliniczne zatorowości płucnej (suma punktów) |
|
|
Niskie |
0-3 |
|
Pośrednie |
4-10 |
|
Wysokie |
≥11 |
Proces diagnostyczny powinno się rozpocząć od oceny stanu klinicznego pacjenta. Chory niestabilny, we wstrząsie lub z hipotonią (definiowaną jako ciśnienie skurczowe <90 mmHg lub spadek ciśnienia skurczowego ≥40 mmHg trwający dłużej niż 15 min i niespowodowany inną przyczyną) obarczony jest wysokim ryzykiem zgonu, wynoszącym >15% w ciągu 30 dni obserwacji. Taki chory powinien być natychmiast przetransportowany do szpitala karetką reanimacyjną i w zależności od jego stanu należy podjąć odpowiednie kroki diagnostyczne i terapeutyczne.4 U wszystkich chorych w stanie stabilnym, czyli obarczonych niewysokim (<15%) ryzykiem zgonu (wewnątrzszpitalnego i 30 dni po wypisie ze szpitala), należy oszacować kliniczne prawdopodobieństwo ZP na podstawie własnego doświadczenia klinicznego albo prostych skal (genewskiej lub Wellsa).5 Strategię diagnostyczną u chorych z niewysokim ryzykiem zgonu przedstawiono na rycinie 3.
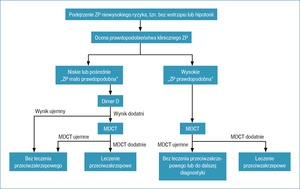
Rycina 3. Algorytm diagnostyczny rekomendowany przez wytyczne European Society of Cardiology i Polskiego Towarzystwa Kardiologicznego przy podejrzeniu ZP niewysokiego ryzyka7
Diagnostykę przy niskim bądź pośrednim klinicznym prawdopodobieństwie ZP rozpoczyna się od oznaczenia stężenia dimera D za pomocą testu o odpowiedniej czułości, najlepiej testu enzymatycznego ze znanym punktem odcięcia dla wyniku prawidłowego.
W ZP dochodzi do aktywacji układu krzepnięcia i jednocześnie układu fibrynolizy, czego wyznacznikiem jest podwyższone stężenie dimera D. Oznaczenie stężenia dimera D służy do wykluczenia, a nie do potwierdzenia ZP lub zakrzepicy żył głębokich kończyn dolnych, co związane jest z wysoką czułością, a niską swoistością testu. Zastosowanie tej prostej metody diagnostycznej pozwala na odstąpienie od leczenia przeciwzakrzepowego bez potrzeby wykonania badania obrazowego naczyń płucnych i narażenia pacjenta na promieniowanie jonizujące. U wszystkich chorych z pośrednim klinicznym prawdopodobieństwem ZP i podwyższonym stężeniem dimera D należy wykonać wielorzędową (czyli posiadającą co najmniej 4 rzędy detektorów) spiralną tomografię komputerową klatki piersiowej uwidaczniającą naczynia płucne lub jednorzędową spiralną tomografię komputerową uzupełnioną o kompresyjne badanie ultrasonograficzne proksymalnych żył głębokich kończyn dolnych.
Wynik prawidłowy pozwala odstąpić od leczenia przeciwzakrzepowego. U pacjentów z wysokim klinicznym prawdopodobieństwem ZP należy od razu wykonać tomografię komputerową klatki piersiowej z pominięciem oznaczenia dimera D, gdyż w tej grupie negatywna wartość predykcyjna tego markera jest niewystarczająca, aby wykluczyć ZP.4 Jeśli wielorzędowa spiralna tomografia komputerowa klatki piersiowej lub jednorzędowa spiralna tomografia komputerowa uzupełniona o kompresyjne badanie ultrasonograficzne proksymalnych żył głębokich kończyn dolnych nie potwierdzi rozpoznania ZP, należy rozważyć poszerzenie diagnostyki o dodatkowe badania (USG żył kończyn dolnych, scyntygrafię perfuzyjną płuc).4
Opisany przez nas chory był w stanie stabilnym, miał prawidłowe ciśnienie tętnicze i w związku z tym można było podejrzewać ZP niewysokiego ryzyka wczesnego zgonu. Kolejnym krokiem powinna być ocena klinicznego prawdopodobieństwa ZP. Nasz chory ma 67 lat, krwioplucie, tachykardię ≥95/min, co daje łącznie 6 punktów (nie doliczamy punktów na obrzęk kończyny dolnej i objawy zakrzepicy, gdyż nie zgłaszał ich na początku choroby), a więc korzystając ze skali genewskiej, można oszacować, że kliniczne prawdopodobieństwo ZP jest u niego pośrednie (6 punktów).5 Kolejnym krokiem diagnostycznym powinno w tej sytuacji być oznaczenie dimera D. W tym przypadku wynik był nieprawidłowy, co obliguje od razu do wykonania badania obrazowego naczyń płucnych. Wielorzędowa spiralna tomografia komputerowa klatki piersiowej pozwoliłaby na szybkie ustalenie właściwego rozpoznania, a wykonane dodatkowo obrazy o wysokiej rozdzielczości celowane na miąższ płucny (HRCT – high resolution computed tomography) pozwoliłyby zróżnicować zmiany w miąższu płuc i ostatecznie ustalić przyczynę krwioplucia. W przypadku naszego pacjenta opóźnienie w diagnostyce i właściwym leczeniu nie miało dramatycznych konsekwencji, ale wiadomo z badań obserwacyjnych, np. prospektywnego rejestru ZATPOL, oceniającego wiarygodność procesu diagnostycznego w zatorowości płucnej oraz konsekwencje nieprawidłowych strategii diagnostycznych przy podejrzeniu ZP w grupie chorych hospitalizowanych w ośrodkach kardiologicznych w Polsce, że nieprawidłowa strategia diagnostyczna zwiększa ryzyko zgonu wewnątrzszpitalnego i 90-dniowego nawet 2-krotnie.6 Biorąc pod uwagę powikłanie w postaci zapalenia płuc i zawał płuca, a także starszy wiek chorego, wieloletnie palenie tytoniu w wywiadzie (wysokie ryzyko przewlekłej obturacyjnej choroby płuc), ryzyko wewnątrzszpitalnego zgonu u tego chorego było znacznie większe niż ryzyko wynikające tylko z samej zatorowości płucnej obciążającej układ krążenia.