Sympozjum: choroby oskrzeli
Przewlekła obturacyjna choroba płuc: leczenie oparte na dowodach naukowych
Nicholas J. Gross, MD, PhD
W SKRÓCIE
Przewlekła obturacyjna choroba płuc (POChP) jest szeroko rozpowszechniona na świecie i wiąże się z wysokimi kosztami społecznymi. Mimo że w Stanach Zjednoczonych zmniejsza się częstość palenia tytoniu, przewiduje się, że wskaźniki chorobowości i umieralności z powodu POChP nadal będą rosły. Właściwe leczenie może istotnie wpływać na wiele aspektów tej choroby. Artykuł stanowi przegląd dowodów z publikacji wydanych między 1 stycznia 2004 r. a 31 grudnia 2007 r., które można znaleźć w bazie PubMed. Terminy, według których przeszukiwano bazę, to: chronic obstructive pulmonary disease, epidemiology, practice guidelines, clinical trial, meta-analysis (przewlekła obturacyjna choroba płuc, epidemiologia, praktyczne wytyczne, badanie kliniczne, metaanaliza). Wybór farmakoterapii zależy od stopnia ciężkości choroby i różnic w działaniu leków na różne parametry oceny końcowej, włączając w to standardowe kryterium, jakim jest pierwszosekundowa natężona objętość wydechowa. Inne ważne zmienne, które istotnie wpływają na percepcję przez chorych ich stanu ogólnego, to redukcja częstości nagłych zaostrzeń, polepszenie się jakości życia, poprawa wydolności wysiłkowej i zmniejszenie hiperinflacji. Jeśli są wskazania do przewlekłej terapii, dowody kliniczne przemawiają za rozpoczęciem jej od długodziałających leków – albo od stosowanych raz dziennie cholinolityków, albo dwa razy dziennie β2-mimetyków. W przypadku wskazań do terapii skojarzonej dane potwierdzają skuteczność długodziałających leków z różnych klas o uzupełniającym się mechanizmie działania (β2-mimetyków, leków cholinolitycznych, wziewnych glikokortykosteroidów). W tym postępowaniu wziewne glikokortykosteroidy mogą dalej zmniejszać częstość zaostrzeń zarówno w połączeniu z β2-mimetykami, jak i lekami cholinolitycznymi, a także w skojarzeniu z lekami z obu tych grup.
Przewlekła obturacyjna choroba płuc jest powszechnym i szeroko rozprzestrzenionym na świecie schorzeniem.1,2 Jego częstość stale wzrasta, szczególnie w Azji i wśród kobiet. W USA, mimo że w ciągu kilku ostatnich dekad stwierdzono redukcję częstości palenia papierosów, współczynniki chorobowości i umieralności związane z POChP nadal rosną i przewiduje się, że tendencja ta będzie się utrzymywać jeszcze przez kilka kolejnych lat. Co więcej, z powodu przewlekłej obturacyjnej choroby płuc ponoszone są wysokie koszty, a nagłe zaostrzenia, które u osób z umiarkowaną i cięższymi postaciami choroby zwykle pojawiają się raz w roku, wiążą się z największymi wydatkami. W 2002 r. bezpośrednie koszty leczenia przewlekłej obturacyjnej choroby płuc wyniosły 18 mld dol., a pośrednie obciążały budżet dodatkowo na kwotę 14 mld dol.3 Według prognoz liczby te wzrosną, ponieważ społeczeństwo się starzeje.
Aby sprostać wielu problemom związanym z tą chorobą, powstają wytyczne oparte na dowodach naukowych.4-6 Chociaż różnią się one nieco w podejściu do tematu, to dostarczają podstawowych, dostosowanych do natężenia objawów wariantowych schematów postępowania. Takie podejście uwzględnia istotną rolę lekarza w wyborze najodpowiedniejszego postępowania dla indywidualnego pacjenta.
Wybór optymalnej terapii może zależeć od stopnia ciężkości choroby, dlatego należy rozważać skuteczność różnych metod leczenia z uwzględnieniem stadium choroby. System stopni wypracowany przez Global Initiative for Chronic Obstructive Lung Disease (GOLD) jest powszechnie znany i zbliżony do klasyfikacji American Thoracic Society i European Respiratory Society.4,5 Wytyczne American College of Physicians odwołują się do obu systemów klasyfikacji.6 Wytyczne GOLD (w ostatniej dekadzie często uaktualniane przez National Heart, Lung and Blood Institute i World Health Organization) zostały niedawno zaktualizowane [w listopadzie 2008 r. – przyp. tłum.].7 W artykule podsumowano rekomendacje zawarte w wytycznych GOLD, podkreślając rolę leków rozkurczających oskrzela zgodnie z wynikami ostatnich badań i wnioskami artykułów publikowanych między 1 stycznia 2004 a 31 grudnia 2007 r., które znajdują się w bazie PubMed. Bazę przeszukiwano według kilku słów kluczy: chronic obstructive pulmonary disease, epidemiology, practice guidelines, clinical trial, meta-analysis. Po wyszukaniu w bazie PubMed badań sprawdzono również piśmiennictwo do tych artykułów pod kątem dodatkowych istotnych źródeł danych.

Tabela 1. Klasyfikacja przewlekłej obturacyjnej choroby płuc na podstawie FEV1 i FVCa mierzonych po podaniu leku rozkurczającego oskrzela
GOLD definiuje POChP jako „chorobę poddającą się prewencji i leczeniu z istotnymi pozapłucnymi objawami (…). Charakteryzuje się ona zwężeniem dróg oddechowych, które nie jest w pełni odwracalne (…), zwykle postępuje i wiąże się z nieprawidłową reakcją zapalną płuc na szkodliwe cząsteczki lub gazy”.7 Aktualna klasyfikacja wyróżnia 4 stopnie ciężkości choroby, od łagodnego do bardzo ciężkiego, które w głównej mierze opierają się na kryterium spirometrycznym – redukcji pierwszosekundowej natężonej objętości wydechowej (FEV1) i wskaźnikach FEV1/FVC (natężona wydechowa pojemność życiowa) (tab. 1).4 Badanie spirometryczne uważa się za podstawową metodę diagnostyczną umożliwiającą ocenę stopnia ciężkości choroby. Przewlekła obturacyjna choroba płuc może występować nawet u 24 mln Amerykanów, przy czym u połowy z nich nie ustalono właściwego rozpoznania.3 W USA najistotniejszym czynnikiem etiologicznym choroby pozostaje palenie papierosów, chociaż zanieczyszczenie środowiska, jak również niekorzystne czynniki środowiskowe występujące w domach też odgrywają pewną rolę. Określenie „choroba poddająca się prewencji” włączone do definicji POChP odnosi się do tych właśnie czynników. Genetyczne uwarunkowania również mają znaczenie, ale jedynym zaburzeniem, które udało się zidentyfikować, jest niedobór α1-antytrypsyny występujący stosunkowo rzadko. W diagnostyce stosuje się laboratoryjne testy przesiewowe swoiste dla tej jednostki chorobowej, które umożliwiają jej rozpoznanie. GOLD rekomenduje wykonywanie takich testów u wszystkich chorych na POChP rasy białej, u których choroba rozwinęła się przed 45. r.ż., lub z dodatnim wywiadem rodzinnym w jej kierunku.7
Kluczowe elementy opieki medycznej w stabilnej przewlekłej obturacyjnej chorobie płuc, których skuteczność została jednoznacznie udowodniona, zaadaptowano z wytycznych GOLD i przedstawiono w tabeli 2.7 Dodatkowo należy rozpoznać choroby, które mogą współistnieć z POChP (choroby sercowo-naczyniowe, depresja, rak płuc i infekcje dróg oddechowych), ponieważ mogą one niekorzystnie wpływać na stan zdrowia chorych i być przyczyną powikłań.
Łagodna do umiarkowanej postać POChP: leki rozkurczające oskrzela

Rycina 1. Wytyczne Global Initiative for Chronic Obstructive Lung Disease (GOLD) dotyczące leczenia przewlekłej obturacyjnej choroby płuc na różnych stopniach zaawansowania choroby – od postaci łagodnej (FEV1 ≥80% WN) do bardzo ciężkiej (FEV1 <30% WN lub FEV1 <50% WN i współistniejąca przewlekła niewydolność oddechowa)
Pacjentom z łagodną postacią choroby (stopień 1) należy zalecić stosowanie w razie potrzeby krótkodziałających leków rozkurczających oskrzela (ryc. 1).7 Mogą to być β2-mimetyki, np. salbutamol (w USA nazywany albuterolem), pirbuterol czy terbutalina [w Polsce dostępne są salbutamol i fenoterol – przyp. tłum.], bromek ipratropium [krótkodziałający lek cholinolityczny – przyp. tłum.] lub skojarzenia β2-mimetyków z bromkiem ipratropium. Zwykle leki te stosuje się, korzystając z inhalatorów ciśnieniowych (MDI – metered-dose inhalers), ale niektórzy pacjenci wolą je przyjmować za pomocą nebulizacji, ponieważ z powodu upośledzonej zręczności manualnej wynikającej ze zmian reumatycznych, chorób neurologicznych lub z powodu słabego wzroku nie są w stanie prawidłowo wykonać inhalacji aerozolu.
Przewlekła terapia z zastosowaniem wziewnych preparatów rozkurczających oskrzela o długim czasie działania powinna być zalecana pacjentom z umiarkowaną postacią choroby (stopień 2), u których objawy są źle kontrolowane lub zużycie leku ratunkowego przekracza 1 inhalator w miesiącu. W przypadku leków rozkurczających oskrzela o długim okresie działania można wybrać stosowany raz dziennie lek cholinolityczny – tiotropium – lub jeden z długodziałających β2-mimetyków (LABA – long-acting β2-agonist) – salmeterol albo formoterol, które zaleca się stosować dwa razy dziennie. Leki te są wygodne dla pacjenta ze względu na dawkowanie raz lub dwa razy dziennie oraz utrzymujące się długo działanie rozkurczające oskrzela, a ponadto – jak wykazano w badaniach – przynoszą inne istotne korzyści dla chorego. Wśród nich należy wymienić redukcję liczby (i prawdopodobnie ciężkości) nagłych zaostrzeń,8,9 poprawę stanu zdrowia (jakości życia),10,11 polepszenie wydolności wysiłkowej12,13 i większą skuteczność rehabilitacji pulmonologicznej (zgodnie z rekomendacjami GOLD jest ona zalecana u pacjentów z co najmniej umiarkowaną postacią POChP).14 Działania niepożądane związane ze stosowaniem długodziałających leków rozkurczających oskrzela występują rzadko i zazwyczaj są łagodne. Zwykle należy zachować ostrożność przy stosowaniu leków cholinolitycznych u pacjentów z retencją moczu w pęcherzu i jaskrą z wąskim kątem przesączania, a w przypadku β2-mimetyków u pacjentów z niestabilnymi chorobami serca i tachyarytmią. Bez względu na to, który z tych leków zostanie wybrany, należy kontynuować stosowanie leków ratunkowych – krótkodziałających β2-mimetyków – w razie potrzeby, w celu przerwania napadu świstów lub duszności. Bromek ipratropium (zarówno sam, jak i jako składnik leku złożonego) będzie niewłaściwym lekiem ratunkowym, jeśli jako długodziałający lek wybrano tiotropium.
Metyloksantyny (teofilina) mogą być stosowane jako leczenie dodane do powyższego schematu lub jako terapia alternatywna u pacjentów z objawami nietolerancji β2-mimetyków. Obecnie zalecane dawki (ok. 300 mg raz dziennie wieczorem lub 200 mg co 12 godzin) są istotnie mniejsze niż stosowane zwykle choćby dekadę temu i dzięki temu ryzyko zatrucia jest małe. Monitorowanie stężenia metyloksantyn we krwi (stężenie leku w surowicy powinno mieścić się w przedziale 5-10 mg/l) przy stosowaniu małych dawek nie jest konieczne.15
Powyższe metody terapii można łączyć, jeśli uzasadniają to uporczywe objawy. Stosowanie u pacjentów z ciężką postacią choroby tiotropium razem z LABA w terapii podtrzymującej jako leczenie podstawowe i krótkodziałającego β2-mimetyku w razie potrzeby oraz – co jest możliwe – dodatkowo metyloksantyny nie jest postępowaniem rzadkim czy przeciwwskazanym. Nie zaleca się jednak przekraczania standardowych dawek czy zwiększania częstości podawania leku długodziałającego z którejkolwiek grupy farmakologicznej, ponieważ w USA nie są one dopuszczone do stosowania jako leki ratunkowe [w Polsce formoterol, długodziałający β2-mimetyk, jest zarejestrowany do stosowania doraźnego w inhalatorze typu Turbuhaler – przyp. tłum.].
Leczenie ciężkiej postaci POChP: dodanie glikokortykosteroidów
Metaanaliza dużych, starannie zaplanowanych, wieloośrodkowych badań wykazała, że regularne stosowanie wziewnych glikokortykosteroidów (ICS – inhaled corticosteroids) nie zmniejsza długoterminowego tempa spadku czynności płuc.16-20 U pacjentów z ciężką i bardzo ciężką postacią przewlekłej obturacyjnej choroby płuc (III i IV stopień wg klasyfikacji GOLD) regularne stosowanie wziewnych glikokortykosteroidów może jednak poprawić stan zdrowia.21 W przypadku pacjentów z III i IV stopniem POChP w ciągu roku może wystąpić jedno lub więcej ciężkich zaostrzeń choroby. Mogą one wpływać na pogorszenie czynności płuc i jakości życia, a ponadto ich leczenie jest drogie. Spodziewanym efektem stosowania wziewnych glikokortykosteroidów w leczeniu podtrzymującym jest redukcja częstości zaostrzeń o 20-25%.9 U pacjentów z III i IV stopniem POChP z częstymi zaostrzeniami choroby poza przewlekłą terapią wziewnymi glikokortykosteroidami w leczeniu podtrzymującym zaleca się stosowanie opisanych już wcześniej leków rozkurczających oskrzela. Wciąż nie określono jednoznacznie stosunku korzyści do ryzyka w przypadku dodania wziewnych glikokortykosteroidów do terapii we wcześniejszych stadiach POChP. Wczesne lub niewłaściwe zastosowanie leków z tej grupy może w końcu prowadzić do pojawienia się działań niepożądanych związanych z ich stosowaniem, takich jak: osteoporoza, osłabienie siły mięśniowej, miopatie, jaskra i zaćma. Objawy te nie pojawiają się zbyt często w raportach z badań klinicznych, trzeba jednak wziąć pod uwagę, że badania trwały stosunkowo krótko, a do wystąpienia objawów klinicznych może upłynąć ≥10 lat. Ostatnio wykazano, że w przypadku przewlekłego stosowania wziewnych glikokortykosteroidów u tych pacjentów częściej stwierdza się również zapalenie płuc.22
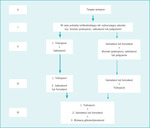
Rycina 2. Proponowany 3-stopniowy algorytm (1, 2 i 3; pogrubione strzałki) do stosowania w terapii łagodnej, umiarkowanej i ciężkich postaci przewlekłej obturacyjnej choroby płuc
Jeśli stan pacjenta uzasadnia stosowanie u niego wziewnych glikokortykosteroidów, powinien on również otrzymywać długodziałające β2-mimetyki. W takim przypadku właściwe i wygodniejsze dla chorych jest stosowanie obu leków skojarzonych w jednym inhalatorze. Jak dotąd w USA zarejestrowano tylko jedno połączenie wziewnego glikokortykosteroidu i β2-mimetyku (flutykazon 250 μg z salmeterolem 50 μg), drugie (budezonid 160 μg z formoterolem 4,5 μg) jest w trakcie oceny przez Food and Drug Administration [w Polsce do leczenia POChP zarejestrowano flutykazon 500 μg z salmeterolem 50 μg z w Dysku oraz budezonid z formoterolem w Turbuhalerze w dawkach 160/4,5 μg i 320/9 μg – przyp. tłum.]. Obecnie nie jest dostępne połączenie w jednym inhalatorze lub preparacie do nebulizacji długodziałającego cholinolityku z β2-mimetykiem czy długodziałającego cholinolityku z wziewnym glikokortykosteroidem. Prawdopodobnie zmieni się to w ciągu kilku najbliższych lat. Na rycinie 2 przedstawiono dwa alternatywne algorytmy terapeutyczne oparte na stopniach intensywności terapii.23
Ostatnie badanie kliniczne nad lekiem złożonym zawierającym wziewny glikokortykosteroid i długodziałający β2-mimetyk – Towards a Revolution in COPD Health (TORCH) – oceniało jego skuteczność u chorych na umiarkowaną do ciężkiej postać przewlekłej obturacyjnej choroby płuc.22 Wykazano w nim, że stosowanie 50 μg salmeterolu w połączeniu z 500 μg flutykazonu dwa razy dziennie (ta dawka nie jest zarejestrowana do stosowania w USA [jest natomiast zarejestrowana w Polsce – przyp. tłum.]) zmniejsza częstość zaostrzeń, poprawia czynność płuc i polepsza stan zdrowia w większym stopniu niż którykolwiek składnik leku podawany osobno lub placebo.22 W badaniu nie udało się wykazać istotnej zmiany w zakresie pierwszorzędowego parametru oceny końcowej, którym była redukcja zgonów w wyniku stosowania leku złożonego w porównaniu z placebo. Wyniki badania potwierdziły dobrą tolerancję długodziałającego β2-mimetyku w monoterapii i skuteczność takiego postępowania u chorych na POChP, które powinno być preferowane w stosunku do monoterapii wziewnymi glikokortykosteroidami.24 Zarówno lek złożony, jak i sam salmeterol redukowały roczną liczbę hospitalizacji z powodu ciężkich zaostrzeń w porównaniu z placebo, czego nie osiąg-nięto, podając flutykazon w monoterapii. Dodatkowo u pacjentów stosujących przewlekle wziewne glikokortykosteroidy stwierdzono większe ryzyko wystąpienia zapalenia płuc w porównaniu z grupą przyjmującą placebo lub leczoną salmeterolem. Co interesujące, w analizie post hoc wykazano redukcję tempa spadku czynności płuc we wszystkich grupach stosujących aktywne leki w porównaniu z placebo.25
