Postępowanie w częstoskurczu komorowym
Postępowanie w stanach nagłych i ocena początkowa
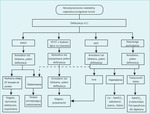
Rycina 2. Postępowanie w stanach nagłych przy niestabilnym hemodynamicznie częstoskurczu komorowym/migotaniu komór. Fab – fragmenty przeciwciał wiążące antygen; MVT – monomorficzny częstoskurcz komorowy; NaHCO3 – wodorowęglan sodowy; PMVT– polimorficzny częstoskurcz komorowy. Zaadaptowano z: Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care, American Heart Association.24
Niezależnie od etiologii przetrwały częstoskurcz komorowy wywołujący objawowy spadek ciśnienia, obrzęk płuc lub niedokrwienie mięśnia serca uzasadnia zastosowanie kardiowersji w trybie pilnym. Na rycinie 2 został pokazany algorytm resuscytacji w przypadku niemiarowości pochodzenia komorowego (za The American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care).24 Przede wszystkim należy leczyć przyczyny odwracalne, takie jak ostre niedokrwienie, zaburzenia elektrolitowe czy zatrucie lekami.
Przedwczesne skurcze komorowe i krótkotrwały częstoskurcz komorowy mogą wskazywać na chorobę serca, niedokrwienie mięśnia sercowego, niedotlenienie lub zaburzenia elektrolitowe. Dlatego uzasadniona jest diagnostyka tych potencjalnych czynników wyzwalających częstoskurcz. Niemiarowości tego rodzaju występują często u chorych z zaburzeniami czynności komór, a ich częstość wzrasta proporcjonalnie do narastania niewydolności lewej komory. Choć ektopowe pobudzenia komorowe i epizody częstoskurczu komorowego są czynnikami zwiększającymi umieralność, farmakologiczne tłumienie tych zaburzeń nie zmniejsza ryzyka nagłego zgonu.
Po ustabilizowaniu częstości rytmu serca większość pacjentów wymaga oceny ewentualnych strukturalnych zmian w sercu przy użyciu EKG lub technik obrazowych (np. rezonansu magnetycznego). Należy m.in. wykluczyć chorobę wieńcową. Dalsze leczenie zależy od rodzaju schorzenia leżącego u podstaw niemiarowości komorowej oraz od typu niemiarowości. Wielokształtny częstoskurcz komorowy sugeruje niedokrwienie mięśnia sercowego lub dziedziczny zespół predysponujący do arytmii. Przetrwały częstoskurcz monomorficzny może być idiopatyczny, bez współistnienia chorób serca powodujących zmiany morfologiczne i związany jest z dobrym rokowaniem; częściej jednak jest objawem blizny pozawałowej, która staje się źródłem pobudzeń nawrotnych. Rokowanie (zwłaszcza ryzyko nagłego zgonu) i rodzaj wymaganej terapii w największym stopniu zależą od choroby serca będącej przyczyną częstoskurczu.
Nagły zgon i niemiarowość pochodzenia komorowego
W Stanach Zjednoczonych nagłe zgony stanowią ponad połowę wszystkich przypadków śmierci z powodu chorób układu krążenia i niemal 15% wszystkich zgonów.25 W badaniach epidemiologicznych nagły zgon jest określany najczęściej jako niespodziewany zgon mający miejsce natychmiast lub w ciągu godziny od nagłej zmiany stabilnego wcześniej stanu zdrowia. Często jest efektem progresji częstoskurczu do migotania komór. Określono już wiele czynników ryzyka nagłego zgonu sercowego. Ponad- dwukrotnie częściej występuje wśród mężczyzn niż wśród kobiet i ponad 3-5 razy częściej przy współistnieniu strukturalnych zmian w sercu, w szczególności miażdżycy naczyń wieńcowych.26,27 Ponad 2/3 wszystkich zatrzymań krążenia ma związek z chorobą wieńcową i może być pierwszym objawem tej choroby, co utrudnia identyfikację pacjentów z grupy wysokiego ryzyka zgonu.
W grupie podwyższonego ryzyka są też chorzy po przebytym zawale serca, przy czym odsetek nagłych zgonów lub zatrzymań krążenia jest najwyższy (1,4% na miesiąc) w pierwszym miesiącu po zawale, by po dwóch latach spaść do 0,14% na miesiąc.28 Jedną z najłatwiejszych metod nieinwazyjnych i najczęściej używanych do szacowania ryzyka nagłego zgonu jest ocena frakcji wyrzutowej lewej komory.29 Spadek tej frakcji poniżej 30% wiąże się ze wzrostem rocznego odsetka umieralności ogólnej do 0,1.30,31 Inne czynniki ryzyka nagłego zgonu to nieprawidłowa zmienność rytmu serca, mikrowoltowa zmienność załamka T (naprzemienność) i komorowe zaburzenia rytmu w postaci licznych (>10/h) pobudzeń przedwczesnych, par lub wstawek niepodtrzymującego się częstoskurczu komorowego.32-35 Przydatność określanych w sposób nieinwazyjny czynników ryzyka do selekcji pacjentów, którzy mogliby odnieść korzyść z wszczepienia kardiowertera-defibrylatora, wciąż pozostaje przedmiotem badań i kontrowersji, mimo że w wybranych populacjach wykazano ich związek ze wzrostem częstości nagłych zgonów sercowych. U pacjentów z chorobą niedokrwienną serca, u których zazwyczaj wskazane jest wszczepienie kardiowertera-defibrylatora, częstoskurcz komorowy indukowany podczas inwazyjnych badań elektrofizjologicznych z programowaną stymulacją komór też podwyższa ryzyko nagłego zgonu sercowego.36
Pacjenci, u których czynność komór uległa pogorszeniu na skutek kardiomiopatii, wrodzonych chorób serca lub wad zastawkowych, również znajdują się w grupie podwyższonego ryzyka wystąpienia częstoskurczu komorowego i nagłego zgonu. W tych grupach chorych czynniki ryzyka są mniej dokładnie określone niż u pacjentów z chorobą wieńcową. Choć w kardiomiopatiach na tle chorób innych niż niedokrwienie rzadko dochodzi do powstania dużych obszarów zbliznowacenia, przetrwały częstoskurcz komorowy często wydaje się związany z blizną, którą można uwidocznić jako obszar opóźnionego wychwytu gadolinu w rezonansie magnetycznym serca. Obecnie są prowadzone intensywne badania nad ustaleniem, czy obrazowanie metodą rezonansu magnetycznego może pomóc w identyfikacji pacjentów o podwyższonym ryzyku.37
Niewielki odsetek nagłych zgonów jest skutkiem dziedzicznych kardiomiopatii (zarówno przerostowych, jak i rozstrzeniowych) lub genetycznych nieprawidłowości w budowie kanałów jonowych (takich jak zespół wydłużonego QT, zespół krótkiego QT czy zespół Brugadów). Nagłe zgony w wywiadzie rodzinnym powinny skłonić lekarza do przeprowadzenia diagnostyki różnicowej w tym kierunku. Co ciekawe, wykazano także istnienie rodzinnej predyspozycji do nagłych zgonów u pacjentów z podwyższonym ryzykiem choroby wieńcowej. Jedną z hipotez mogących to wyjaśnić jest istnienie genetycznych predyspozycji do migotania komór podczas niedokrwienia.
Leczenie farmakologiczne komorowych zaburzeń rytmu
Wykazano, że u pacjentów z chorobą wieńcową lub niewydolnością serca β-adrenolityki i inhibitory ACE zmniejszają umieralność i ryzyko nagłego zgonu.38-40
Częstoskurcz komorowy jest często powodowany pobudzeniem adrenergicznym, a β-adrenolityki mogą zmniejszyć częstość nawrotów niemiarowości. Leki antyarytmiczne działające błonowo w większości przypadków nie spełniły pokładanych w nich nadziei i nie obniżają śmiertelności u pacjentów z grup podwyższonego ryzyka wystąpienia komorowych zaburzeń rytmu.41,42 Leki antyarytmiczne klasy III, takie jak sotalol i amiodaron, zmniejszają częstość nawrotów arytmii, ale nie mają wpływu na umieralność.43,44 Z kolei leki klasy I (np. chinidyna, flekainid i propafenon) zwiększają umieralność chorych z komorowymi zaburzeniami rytmu i przebytym zawałem serca.41,45,46 U pacjentów z organiczną chorobą serca, którzy mieli utrwalony częstoskurcz komorowy lub migotanie komór, w celu zmniejszenia ryzyka nawrotów objawowych arytmii można stosować leki antyarytmiczne po wszczepieniu kardiowertera-defibrylatora.
Idiopatyczny częstoskurcz komorowy często dobrze poddaje się leczeniu β-adrenolitykami lub antagonistami kanałów wapniowych niebędącymi pochodnymi dihydropirydyny (werapamil lub diltiazem). Skuteczne mogą też okazać się leki antyarytmiczne klasy I lub III, ale zazwyczaj jeśli zastosowanie β-adrenolityków i antagonistów kanałów wapniowych okaże się nieskuteczne, rozważa się raczej przezskórną ablację niż długotrwałe leczenie farmakologiczne. W idiopatycznym częstoskurczu komorowym ablacja kończy się z powodzeniem nawet u 80% pacjentów.47
Rola wszczepianych kardiowerterów-defibrylatorów u chorych obarczonych ryzykiem nagłego zgonu
U większości pacjentów wszczepialne kardiowertery-defibrylatory skutecznie przerywają częstoskurcz komorowy i migotanie komór, a w niektórych grupach o podwyższonym ryzyku nagłego zgonu zmniejszają także śmiertelność. Właściwa selekcja chorych do wszczepienia tych urządzeń jest tematem licznych badań. Kandydatów do wszczepienia kardiowertera-defibrylatora można podzielić na dwie kategorie: tych, u których urządzenie wszczepiane jest w ramach wtórnej profilaktyki nagłego zgonu po przeżyciu zatrzymania krążenia, oraz tych, u których wszczepienie dokonywane jest w ramach profilaktyki pierwotnej nagłego zgonu, bez wcześniejszego epizodu zatrzymania krążenia ani przetrwałego częstoskurczu komorowego.
Pacjenci, którzy przeżyli zatrzymanie krążenia, oraz ci, którzy cierpią z powodu przetrwałego częstoskurczu komorowego upośledzającego hemodynamikę, przy czym częstoskurcz ten nie miał innej przyczyny (np. ostry zawał serca), znajdują się w grupie wysokiego ryzyka (>40%) nawrotu częstoskurczu lub migotania komór w ciągu kolejnych dwóch lat. Wszczepialny kardiowerter-defibrylator jako narzędzie prewencji wtórnej zwiększa szanse przeżycia (31% zmniejszenie umieralności w ciągu 3 lat).28
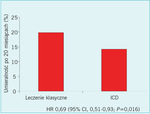
Rycina 3. Śmiertelność 20-miesięczna u pacjentów z chorobą niedokrwienną serca i frakcją wyrzutową lewej komory <30%; dane z drugiego badania Multicenter Automatic Defibrillator Implantation Trial (MADIT-II). CI – przedział ufności; HR – współczynnik ryzyka; ICD – wszczepialny kardiowerter-defibrylator.
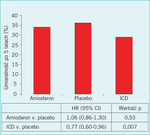
Rycina 4. Śmiertelność pięcioletnia u pacjentów z kardiomiopatią pochodzenia niedokrwiennego lub innego niż niedokrwienne, opracowana na podstawie badania Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT). CI – przedział ufności; HR – współczynnik ryzyka; ICD – wszczepialny kardiowerter-defibrylator.