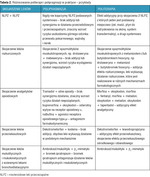
7. Nieuwzględnienie u pacjentów przyjmujących tramadol jego istotnych klinicznie interakcji
Tramadol ulega metabolizmowi wątrobowemu przy udziale izoenzymu CYP2D6. W jego wyniku powstaje farmakologicznie czynny metabolit O-demetylotramadol (M1). Z tego też względu nie zaleca się równoczesnego stosowania tramadolu z lekami hamującymi aktywność CYP2D6, gdyż z jednej strony spowalnia to powstawanie czynnego metabolitu, a z drugiej, szczególnie w przypadku stosowania form o przedłużonym działaniu, może prowadzić do wystąpienia objawów niepożądanych, a nawet toksycznych. Nie należy zapominać, że w rasie kaukaskiej 5-10% populacji to osoby wolno metabolizujące leki przy udziale izoenzymu CYP2D6. W związku z tym u tych pacjentów ryzyko niepożądanych interakcji farmakokinetycznych jest dodatkowo spotęgowane. W mechanizmie działania tramadolu oprócz wpływu na receptory opioidowe istotne jest także hamowanie wychwytu zwrotnego serotoniny w układzie antynocyceptywnym zstępującym, co z kolei pociąga za sobą wzrost ryzyka wystąpienia zespołu serotoninowego.
Ostrożność należy zachować przy łącznym stosowaniu trójpierścieniowych leków przeciwdepresyjnych (w szczególności amitryptyliny) oraz inhibitorów wychwytu zwrotnego serotoniny (w szczególności fluoksetyny i paroksetyny), gdyż skojarzenie takie z jednej strony hamuje metabolizm tramadolu, z drugiej zwiększa ryzyko wystąpienia drgawek. Nie należy kojarzyć tramadolu z karbamazepiną, ponieważ powstający w wyniku interakcji N-demetylotramadol nie działa analgetycznie, natomiast indukuje wystąpienie napadu padaczkowego.
Niekorzystne jest także stosowanie metoklopramidu jako leku przeciwwymiotnego podczas terapii tramadolem. Metoklopramid jest silnym inhibitorem metabolizmu tramadolu, co zmniejsza efektywność przeciwbólową metabolitów tramadolu. Tramadolu nie można także kojarzyć z setronami, np. ondansetronem, z uwagi na antagonizowanie aktywowania przez lek zstępujących szlaków antynocyceptywnych.
Tramadol nasila działanie depresyjne na OUN leków nasennych, pochodnych benzodiazepiny oraz leków neuroleptycznych. Podany łącznie z neuroleptykami może wywołać drgawki. Stosowanie tramadolu z lekami hipotensyjnymi zwiększa ryzyko wystąpienia hipotonii.
Nie należy także stosować równocześnie tramadolu z mirtazapiną, która jest antagonistą receptora 5-HT3 i w tym mechanizmie może redukować efekt analgetyczny tramadolu. U pacjentów leczonych tramadolem z uwagi na interakcje farmakokinetyczne nie należy jednocześnie stosować leków roślinnych i suplementów diety, które zawierają wyciągi z ostropestu plamistego.6-9
8. Kojarzenie doustnych leków przeciwzakrzepowych z grupy antagonistów witaminy K z paracetamolem
Warto przypomnieć, że paracetamol ma zdolność hamowania metabolizmu warfaryny i acenokumarolu, skutkiem czego jest nasilenie antykoagulacji i wzrost ryzyka krwawień.
9. Kojarzenie analgetyków z lekami o ośrodkowym działaniu cholinolitycznym
Warto pamiętać, że jednym z mechanizmów działania analgetycznego jest aktywacja nadrdzeniowych szlaków cholinergicznych. W wyniku stosowania leków o działaniu antycholinergicznym mechanizm ten może zostać osłabiony, co w konsekwencji doprowadza do redukcji ich działania analgetycznego. U pacjentów leczonych z powodu dolegliwości bólowych nie zaleca się równoczesnego stosowania fenotiazyn (promazyna, perazyna, prometazyna, lewomepromazyna), a także hydroksyzyny i innych leków przeciwhistaminowych dobrze penetrujących do OUN, np. difenhydraminy.
10. Kojarzenie analgetyków z cyproheptadyną
Cyproheptadyna wykazuje silne działanie antyserotoninowe i w tym mechanizmie może osłabiać lub nawet antagonizować (tramadol) efekt przeciwbólowy analgetyków. Cyproheptadyny nie należy stosować u pacjentów leczonych z powodu bólu.
Witamina C – niewinna moda czy istotne zagrożenie?
Od kilku lat istnieje swoista moda na przyjmowanie dużych dawek witaminy C. Mnożą się gabinety, w których podaje się tzw. kroplówki witaminowe, i zapewnienia w internecie, że wszystko odbywa się pod kontrolą lekarza. Niestety, rzeczywistość jest inna. W praktyce klinicznej spotykamy coraz większą liczbę chorych, u których na skutek podawania dużych dawek witaminy C jednocześnie z innymi lekami dochodzi do powikłań o różnym obrazie klinicznym. O ile pacjent przed podaniem kroplówki witaminowej jest badany przez lekarza, o tyle – jak wynika z analizy powikłań – niestety nie analizuje się konsekwencji interakcji witaminy z innymi stosowanymi przez pacjenta lekami. Pacjenci niejednokrotnie poszukują preparatów „lewoskrętnych”, uznając je za swoiście lepsze od innych postaci witaminy C. Tymczasem witamina C, czyli kwas L-askorbinowy, jest prawoskrętna. Przekonanie, że jest odwrotnie, wynika ze swoistego nieporozumienia wynikającego z tego, że litera „L” w nazwie „kwas L-askorbinowy” została błędnie utożsamiona z lewoskrętnością. W rzeczywistości litera „L” i pojęcie „lewoskrętność” oznaczają zupełnie coś innego. Na cząsteczkę kwasu askorbinowego składa się sześć atomów węgla, osiem atomów wodoru i sześć atomów tlenu. Gdy zwizualizujemy tę trójwymiarową cząsteczkę na płaszczyźnie (tzw. projekcja Fischera), wtedy grupa atomów złożona z wodoru i tlenu może znaleźć się po prawej albo lewej stronie tego schematu (w konfiguracji D lub L). W kwasie L-askorbinowym ta grupa atomów znajduje się po lewej stronie, stąd literka „L” w nazwie. W biochemii odzwierciedleniem prawo- lub lewoskrętności kwasu askorbinowego są znaki (+) albo (–). Cząsteczce, którą uznaje się za witaminę C, przypisuje się konfigurację L (mylnie utożsamianą z lewoskrętnością) oraz prawoskrętność (+). Za witaminę C uznawana jest jedynie konfiguracja L kwasu askorbinowego, czyli kwas L-askorbinowy. Każda inna forma kwasu askorbinowego nie jest witaminą C, lecz zgoła innym związkiem, i nie może być ona nazywana ani dystrybuowana jako witamina. Wszystkie witaminy C dostępne na rynku bez względu na to, co piszą producenci, to kwas L-askorbinowy.
Wśród pacjentów funkcjonuje także wiele mitów dotyczących witaminy C naturalnej i sztucznej (syntetycznej). Powszechnie uważa się, że najbardziej wartościowa jest naturalna witamina C, np. występująca w owocach i warzywach, a ta sztuczna (syntetyczna), wyprodukowana w laboratorium, jest mniej wartościowa. Syntetyczna nie oznacza „niewystępująca w przyrodzie”, lecz „będąca efektem syntezy chemicznej”. Z chemicznego punktu widzenia witamina C, która znajduje się w owocach czy warzywach, również jest syntetyczna, ponieważ powstała na drodze reakcji chemicznej z cukrów. W związku z tym niezależnie od tego, skąd pochodzi witamina C, ma ona identyczną budowę oraz właściwości biologiczne i farmakologiczne. Warto jednak zaznaczyć, że witamina C pochodząca z diety jest lepiej przyswajana w porównaniu z witaminą C pochodzącą z suplementów. Do tego naturalnie występująca witamina C dłużej utrzymuje się w ustroju, za co mogą być również odpowiedzialne współwystępujące bioflawonoidy swoiście chroniące witaminę C.
Sugeruje się, że nadmierna podaż witaminy C powoduje zwiększenie wydalania szczawianów i sprzyja powstawaniu kamieni nerkowych. Duże dawki mogą także powodować biegunkę.
Za bezpieczne uznano dawki dobowe nieprzekraczające 1000 mg, przy czym najmniejsza dawka, przy której obserwowano działania niepożądane, wynosi około 2500 mg/24 h.
Warto pamiętać, że witamina C wchodzi w niekorzystne interakcje z ponad 130 lekami. Należy odradzać jej stosowanie podczas chemioterapii nowotworów, ponieważ może zmniejszać, szczególnie podawana w wysokich dawkach, skuteczność niektórych cytostatyków, a ponadto nasila nefrotoksyczność pochodnych platyny. Witamina C skraca czas działania morfiny i oksykodonu. Leki te w postaci o natychmiastowym działaniu (formy doustne i pozajelitowe) zamiast działać około 4 godzin, oddziałują tylko około 30 minut.