Kongres Akademii po Dyplomie Pediatria 2026 👉 200 zł taniej do 23:59! Spotkajmy się 17-18 kwietnia w Warszawie | Skorzystaj z oferty >
Chociaż objawy zwykle rozwijają się w ciągu pierwszych dwóch tygodni leczenia przeciwpsychotycznego, NMS może wystąpić po pojedynczej dawce lub po leczeniu tym samym środkiem w tej samej dawce przez wiele lat. Nie jest to zjawisko zależne od dawki, ale wyższe dawki są czynnikiem ryzyka rozwoju NMS, podobnie jak rozpoczęcie terapii neuroleptykiem, szybka eskalacja dawki, zmiana z jednego środka na inny oraz podawanie pozajelitowe14.
Złośliwy zespół neuroleptyczny obserwuje się również u pacjentów leczonych z powodu parkinsonizmu w sytuacji odstawienia lewodopy lub agonisty dopaminy, a także po zmniejszeniu dawki i przejściu z jednego leku na inny. Nie jest do końca jasne, czy wówczas mamy do czynienia z ostrym zespołem neuroleptycznym, czy z zespołem hiperpyreksja–parkinsonizm, ostrą akinezą lub złośliwym zespołem w chorobie Parkinsona, które również mogą być śmiertelne15.
Patomechanizm NMS jest nieznany. Uznaje się, że kluczowe znaczenie ma blokada receptorów dopaminowych, która w podwzgórzu może powodować hipertermię i inne objawy dysautonomii. Ingerencja w nigrostriatalne szlaki dopaminy może prowadzić do wystąpienia objawów zespołu parkinsonowskiego. Uznaje się jednak, że na rozwój NMS mają również wpływ zaburzenia innych neuroprzekaźników, w tym kwasu γ-aminomasłowego, epinefryny, serotoniny i acetylocholiny16. Ponadto mutacja genu receptora dopaminowego D2 stanowi genetyczną predyspozycję do wystąpienia tej choroby17.
Obraz kliniczny złośliwego zespołu neuroleptycznego w postaci klasycznej tetrady objawów rozwija się w ciągu 1-3 dni i obejmuje:
- zmianę stanu psychicznego, która zwykle przybiera postać pobudzenia, delirium, dezorientacji lub nawet psychozy; często występują katatonia i mutyzm, a w ostateczności śpiączka
- uogólnioną sztywność mięśni; mogą również występować dystonia, szczękościsk, dyskinezy, ślinotok, dyzartria i dysfagia
- hipertermię, rzadziej występującą w przypadku neuroleptyków atypowych
- dysautonomię najczęściej objawiającą się tachykardią, zwyżkami ciśnienia tętniczego i obfitym poceniem się14.
W badaniach laboratoryjnych charakterystyczne jest podwyższone stężenie kinazy kreatynowej. W NMS jej stężenie wynosi zazwyczaj >1000 j./l i może sięgać nawet 100 000 j./l14.
W diagnostyce różnicowej należy uwzględnić polekowe zespoły dysautonomii z dominującą sztywnością mięśniową i hipertermią: zespół serotoninergiczny, hipertermię złośliwą (rzadka choroba genetyczna, ujawniająca się po zastosowaniu silnych halogenowych środków znieczulających i sukcynylocholiny), katatonię złośliwą, odstawienie dooponowego leczenia baklofenem, związane ze zmniejszoną aktywnością kwasu γ-aminomasłowego, zespół antycholinergiczny.
Leczenie
Leczenie należy rozpocząć od odstawienia czynnika sprawczego. Niezwykle ważne jest prowadzenie terapii wspomagającej, ponieważ najczęstszymi przyczynami zgonu w przebiegu NMS są powikłania. Terapia wspomagająca w pierwszej kolejności obejmuje leczenie:
- odwodnienia
- zaburzeń elektrolitowych
- ostrej niewydolności nerek związanej z rabdomiolizą
- zaburzeń rytmu serca
- niewydolności krążenia
- niewydolności oddechowej
- infekcji, w tym zachłystowego zapalenia płuc
- powikłań zakrzepowo-zatorowych (profilaktycznie).
W ramach farmakologicznego leczenia złośliwego zespołu neuroleptycznego stosuje się: lorazepam, amantadynę, bromokryptynę, lewodopę, apomorfinę, karbamazepinę, bupropion, klonazepam.
Nasilony złośliwy zespół neuroleptyczny bezwzględnie wymaga leczenia na oddziale intensywnej terapii.
Większość epizodów ustępuje w ciągu 2 tygodni. Gros pacjentów wraca do zdrowia bez następstw neurologicznych z wyjątkiem przypadków, w których doszło do rozwoju ciężkich powikłań14.
Wznowienie leczenia neuroleptykami może prowadzić do ponownego wystąpienia złośliwego zespołu neuroleptycznego. W zależności od źródeł ryzyko wznowy szacowane jest na 10-90%. Wśród czynników ryzyka nawrotu NMS wymienia się: wczesne wznowienie terapii przeciwpsychotycznej, stosowanie pozajelitowych leków przeciwpsychotycznych o dużej sile działania, jednoczesne przyjmowanie litu18.
Ponowne rozpoczęcie terapii powinno być oparte na dokładnej analizie ryzyka i wymaga stałego monitorowania pacjenta pod kątem wystąpienia objawów NMS. W celu minimalizacji ryzyka wznowy należy stosować się do poniższych wytycznych:
- odczekać co najmniej 2 tygodnie przed wznowieniem terapii lub dłużej, jeśli istnieją jakiekolwiek pozostałości kliniczne
- terapię rozpoczynać od preparatów o mniejszej sile działania
- leczenie rozpoczynać od niskich dawek i powoli miareczkować
- unikać jednoczesnego stosowania litu
- unikać odwodnienia18.
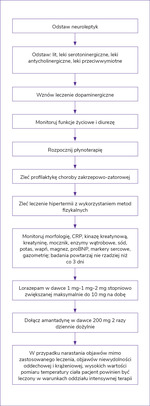
Protokół postępowania w złośliwym zespole neuroleptycznym przedstawiono na rycinie 2.