Minisympozjum – choroby zakaŹne
Mononukleoza zakaźna
Elżbieta Ołdak
Wprowadzenie
Mononukleoza zakaźna jest kliniczną prezentacją pierwotnego zakażenia wirusem Epsteina-Barr (EBV). U chorych immunokompetentnych, z prawidłowo funkcjonującym układem odpornościowym, przebieg pierwotnego zakażenia EBV jest zwykle łagodny i samoograniczający. W obrazie klinicznym dominuje triada objawów: wysoka gorączka, zapalenie gardła i migdałów podniebiennych oraz powiększenie węzłów chłonnych. Ciężkie powikłania neurologiczne, hematologiczne, zapalenie wątroby czy pęknięcie powiększonej śledziony w przebiegu choroby opisywane są rzadko. Wirus EB należący do rodziny Herpesvirideae pozostaje w zakażonych, krążących limfocytach B i być może komórkach nabłonka jamy ustnej do końca życia (zakażenie latentne). U niewielkiej liczby zakażonych z pierwotnymi lub nabytymi nieprawidłowościami układu immunologicznego zakażenie latentne może prowadzić do rozwoju powiązanych z EBV chłoniaków lub nowotworów nabłonkowych.
Rys historyczny
Pierwszy opis choroby, charakteryzującej się gorączką, bólem gardła, złym samopoczuciem, powiększeniem wątroby, śledziony i węzłów chłonnych, przedstawili Nil Filatov i Emil Pfeiffer w latach 80. XIX wieku. Pfeiffer nazwał chorobę gorączką gruczołową. Nazwa ta funkcjonuje do chwili obecnej w krajach anglojęzycznych (glandural fever), niekiedy z podaniem nazwisk autorów opisów – gorączka gruczołowa Pfeiffera lub gorączka gruczołowa Fiłatowa. W 1920 roku Thomas P. Sprunt i Frank A. Evans opisali zjawisko występowania atypowych limfocytów u młodych osób cierpiących na identyczny zespół objawów i wprowadzili nową nazwę choroby, stosowaną powszechnie do chwili obecnej – mononukleoza zakaźna.1-3 Pięć lat później I. Davidsohn wykrył w surowicy chorych na mononukleozę zakaźną przeciwciała heterofilne, zdolne do aglutynacji czerwonych krwinek końskich, bydlęcych i baranich.4 W 1932 roku J.R. Paul i W.W. Bunnell opracowali test wykrywający te przeciwciała, który po modyfikacji wprowadzonej przez Davidsohna w 1937 roku był wykorzystywany w diagnostyce mononukleozy zakaźnej do lat 90. XX wieku jako test Paula-Bunnella-Davidsohna.5-7 W ostatnich kilkunastu latach obecność przeciwciał heterofilnych we krwi chorych na mononukleozę zakaźną potwierdza się łatwiejszymi i szybszymi w wykonaniu testami lateksowymi.8
Mimo wiedzy na temat klinicznych i laboratoryjnych kryteriów diagnostycznych mononukleozy zakaźnej do 1968 roku nie znano czynnika sprawczego choroby. Wirus został rozpoznany przy użyciu mikroskopu elektronowego w komórkach chłoniaka Burkitta i następnie opisany przez Michela A. Epsteina i Yvonne Barr w 1964 roku.9 Na cześć odkrywców nazwano go wirusem Epsteina-Barr. Po kolejnych czterech latach EBV został wyizolowany ze śliny chorych na mononukleozę zakaźną, co potwierdziło wcześniejsze przypuszczenia, że jest on odpowiedzialny za wywoływanie tej choroby.10
Przyczyna i patogeneza zakażenia
Wirus EB, a według klasyfikacji taksonomicznej herpeswirus 4 (HHV-4), jest jednym z ośmiu znanych do chwili obecnej herpeswirusów. Genom wirusa stanowi liniowy, dwuniciowy DNA (dsDNA), otoczony białkowym kapsydem o symetrii kubicznej i lipidową otoczką z zakotwiczonymi w niej glikoproteinami. Między kapsydem a lipidową otoczką znajduje się warstwa białkowa (tegument). Glikoproteiny zewnętrznej otoczki odpowiadają za tropizm komórkowy EBV, ich swoistość gatunkową oraz rozpoznanie receptorów gospodarza.2,9 Zidentyfikowano 2 typy EBV – A i B (odpowiednio 1 i 2), które różnią się między sobą nieznacznie sekwencją genów antygenów jądrowych (Epstein-Barr nuclear antigen, EBNA). Wirusy EB zakażają wyłącznie ludzi, a docelowymi komórkami, które atakują, są głównie komórki nabłonka błony śluzowej jamy ustnej i gardła oraz limfocyty B. Glikoproteiny gH, gL i gp42 EBV łączą się z receptorami C3D (CR2) komórek nabłonkowych lub z receptorami CD21 limfocytów B i T, a następnie przy udziale antygenów zgodności tkankowej typu II (HLA II) wnikają do wnętrza komórek docelowych.11 Uwolniony w cytoplazmie genom EBV wchodzi do jądra komórki docelowej, gdzie przy udziale polimerazy DNA gospodarza i enzymów wirusowych rozpoczyna się replikacja wirusów. Znaczna liczba potomnych cząstek wirusa doprowadza do „rozerwania” i śmierci (lizy) zaatakowanej komórki, dlatego ten etap zakażenia nazywany jest cyklem litycznym. Uwolnione wirusy atakują następne komórki docelowe i w ten sposób zakażenie rozszerza się na sąsiadujące komórki. Istotnym następstwem zakażenia limfocytów B jest ich aktywacja w kierunku wzrostu i różnicowania się w komórki pamięci. W fazie litycznej zakażenia EBV około 0,5% całej populacji limfocytów jest zakażonych. Zakażone komórki pamięci typu B migrują do krwi i wraz z nią rozprowadzane są po całym organizmie – faza wiremii.9 W okresie wiremii mogą zostać zakażone wątroba, tarczyca, mózg, opony mózgowo-rdzeniowe, mięsień sercowy i osierdzie oraz wiele innych narządów.
Zakażone w fazie litycznej komórki ujawniają na swojej powierzchni charakterystyczne białka wirusa, między innymi antygen błonowy (membrane antigen, MP), wczesny kompleks antygenowy (early antigen complex, EA) i kompleks antygenowy kapsydu wirusa (viral capsid antigen complex, VCA). Białka te stymulują układ immunologiczny osoby zakażonej do nieswoistej i swoistej odpowiedzi humoralnej i komórkowej. Swoiste przeciwciała neutralizujące, skierowane przeciw wymienionym kompleksom białkowym wirusa oraz zaktywowane limfocyty T i NK, przy współudziale licznych cytokin, doprowadzają do wyeliminowania znacznej liczby zakażonych komórek, ograniczenia zakażenia i ustąpienia objawów choroby. W niewielkiej liczbie komórek pamięci typu B i być może komórek nabłonkowych EBV pozostaje jednak w fazie „uśpienia” do końca życia gospodarza. Jest to faza latentna zakażenia. Przyjmuje się, że u osób zakażonych, po ustąpieniu ostrej fazy, jeden do pięćdziesięciu na milion limfocytów B zawiera materiał genetyczny EBV.9,12 Materiał genetyczny EBV pozostaje w jądrach komórkowych, w postaci kolistej (episomy) i nie jest zintegrowany z chromosomami. W stanie uśpienia ekspresja antygenów wirusowych (EBNA i latent membrane protein [LMP]) w zakażonych komórkach jest ograniczona i w ten sposób komórki wymykając się spod kontroli układu immunologicznego, stają się nieśmiertelne. W pewnych nie do końca wyjaśnionych okolicznościach może dojść do reaktywacji fazy litycznej, co powoduje ponowną replikację EBV, a osoba zakażona ponownie może zakażać osoby wrażliwe. Reaktywacja zakażenia u osób immunokompetentnych nie wywołuje objawów klinicznych. U osób z pierwotnym zaburzeniem odporności komórkowej, leczonych immunosupresyjnie, po transplantacji narządów lub w przebiegu zakażenia HIV, zakażenie EBV może prowadzić do rozwoju choroby limfoproliferacyjnej. Udokumentowano również związek między zakażeniem EBV a rozwojem chłoniaka Burkitta, chłoniaka z komórek B lub T, raka jamy nosowo-gardłowej czy chorób o podłożu autoimmunologicznym.12,13
Epidemiologia
Wirusy Epsteina-Barr rozpowszechnione są na całym świecie, przy czym typ A występuje częściej. W krajach europejskich jest on odpowiedzialny za blisko 90% zakażeń, podczas gdy typ B dominuje w krajach Afryki równikowej.2 Prawie każdy człowiek w pewnym okresie swego życia zostaje zakażony EBV. Wyniki badań seroepidemiologicznych wykazały, że 90-95% populacji światowej jest zakażona EBV.14 Najczęściej pierwotne zakażenie nabywane jest w okresie wczesnego dzieciństwa przez bezpośredni kontakt z zakażoną śliną, obecną na wspólnych zabawkach, butelkach czy innych przedmiotach wkładanych do ust (oblizane przez rodziców smoczki). Pierwotne zakażenie nabyte w pierwszej dekadzie życia jest zwykle bezobjawowe lub skąpoobjawowe, a przez to często zostaje przeoczone. Zakażenie nabyte w okresie młodzieńczym lub w wieku dorosłym klinicznie prezentuje zespół objawów opisanych jako mononukleoza zakaźna. Istnieją udokumentowane różnice dotyczące czasu pierwszego kontaktu z EBV w społeczeństwach ubogich i bogatych. W krajach ubogich do pierwotnego zakażenia częściej dochodzi w młodym wieku, natomiast w krajach bogatych, o wysokich standardach sanitarno-higienicznych, ten czas przesuwa się na okres młodzieńczy, co prowadzi z kolei do częstszego występowania mononukleozy zakaźnej.15 Źródłem zakażenia są chorzy, ozdrowieńcy, ale również osoby klinicznie zdrowe, u których doszło do reaktywacji zakażenia latentnego. Transmisja wirusa następuje przez bezpośredni kontakt z zakażoną śliną, często w czasie intymnych pocałunków, stąd potoczna nazwa mononukleozy zakaźnej brzmi „choroba pocałunków”. Zakażenia dotyczą w równym stopniu obu płci i nie wykazują sezonowości. Przebywanie w towarzystwie osoby zakażonej w tym samym pomieszczeniu jest bezpieczne i nie grozi zakażeniem. Chorzy nie wymagają zatem izolacji na oddziałach zakaźnych. Zakażenie EBV może być również przeniesione w czasie transfuzji zakażonej krwi, szpiku czy po przeszczepieniu zakażonych EBV narządów. Takie zakażenia zwykle przebiegają ciężko i mogą zagrażać życiu, szczególnie biorców pozostających w immunosupresji.9 Okres wylęgania choroby jest długi i wynosi 4-8 tygodni (30-50 dni).
Obraz kliniczny mononukleozy zakaźnej
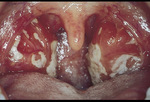
Pełnoobjawowa mononukleoza zakaźna występuje najczęściej u osób w przedziale wiekowym 15-25 lat. Choroba rozpoczyna się zwykle uczuciem osłabienia, zmęczenia i/lub bólami mięśni. Po kilku dniach utrzymywania się powyższych objawów występuje charakterystyczna triada objawów: gorączka, ból gardła i powiększenie migdałów podniebiennych oraz węzłów chłonnych, zwłaszcza szyjnych tylnych. Wysoka gorączka powyżej 38,5ºC jest najbardziej stałym i wczesnym objawem mononukleozy zakaźnej i utrzymuje się długo, 10-14 dni. Ciepłota ciała wzrasta zwłaszcza w godzinach popołudniowych i wieczornych. U niewielkiego odsetka chorych gorączka może trwać ponad dwa tygodnie mimo podawania środków przeciwgorączkowych. Gorączce towarzyszy ból gardła, spowodowany stanem zapalnym błony śluzowej gardła i migdałków podniebiennych. Podczas oglądania jamy ustnej stwierdza się znacznie powiększone, niekiedy stykające się ze sobą w linii pośrodkowej, migdałki podniebienne, pokryte grubym, białoszarawym nalotem włóknikowym, który łatwo można usunąć szpatułką bez wywoływania krwawienia. Na granicy podniebienia twardego i miękkiego mogą być widoczne drobne wybroczyny (rycina). Często wyczuwalny jest przykry zapach z ust – foetor ex ore. Znacznie powiększone migdałki podniebienne oraz pokrywający je nalot włóknikowy utrudniają połykanie pokarmów stałych, a nawet oddychanie, co szczególnie u młodszych chorych jest wskazaniem do hospitalizacji. Powiększone węzły chłonne szyi mogą być widoczne (zmieniony zarys szyi, tzw. szyja Nerona) i/lub wyczuwalne w badaniu palpacyjnym. Najczęściej powiększone są węzły chłonne wzdłuż tylnego i przedniego brzegu mięśni mostkowo-obojczykowo-sutkowych. Są one bolesne, przesuwalne względem skóry i podłoża i osiągają wielkość od ziarna fasoli do orzecha włoskiego. Skóra nad nimi pozostaje niezmieniona. Charakterystyczny dla mononukleozy zakaźnej jest obrzęk powiek i twarzy, ale te objawy występują rzadko. Po kilku dniach utrzymywania się gorączki może nastąpić powiększenie śledziony i wątroby. W tym czasie chorzy skarżą się na ból brzucha czy uczucie pełności w nadbrzuszu oraz brak apetytu. U młodszych dzieci może wystąpić biegunka. Ponadto w przebiegu mononukleozy zakaźnej można obserwować różnego rodzaju wysypki skórne na tułowiu i kończynach o charakterze plamistym, plamisto-grudkowym czy drobne wybroczyny (petecchie). U większości chorych objawy kliniczne utrzymują się średnio 16 dni, co nie jest typowe dla innych zakażeń wirusowych.9 Powrót do zdrowia następuje powoli, ale uczucie zmęczenia i zaburzenia koncentracji mogą utrzymywać się przez wiele miesięcy.
U młodszych chorych (poniżej 10 roku życia) obraz kliniczny choroby jest częściej skąpoobjawowy. Najbardziej stałym objawem jest długo utrzymująca się gorączka lub stany podgorączkowe oraz powiększone obwodowe węzły chłonne i zmieniona zapalnie błona śluzowa gardła. Rzadziej obserwuje się charakterystyczny nalot włóknikowy na migdałkach podniebiennych, powiększoną śledzionę czy wątrobę.
Rozpoznanie
Kliniczny obraz mononukleozy zakaźnej nie jest charakterystyczny. W rozpoznaniu różnicowym należy uwzględnić anginę paciorkowcową, pierwotne zakażenie cytomegalowirusem (CMV) i innymi herpeswirusami (HSV 6), a także nabyte zarażenie toksoplazmozą. Ustalenie prawidłowego rozpoznania jest istotne ze względu na dalsze postępowanie terapeutyczne. Podejrzewając mononukleozę zakaźną na podstawie obrazu klinicznego, należy wykonać badania laboratoryjne, które dzielimy na swoiste i nieswoiste.