W pierwszym miesiącu po transplantacji zakażenia u biorców przeszczepu są związane głównie z powikłaniami chirurgicznymi i silną immunosupresją. Najczęściej występują:
- bakteryjne i grzybicze zakażenia rany
- zapalenia płuc, zakażenia układu moczowego, posocznica
- zakażenia drenów i cewników
- zakażenia związane z pobytem na oddziale intensywnej terapii (np. Clostridium difficile, Enterococci oporne na wankomycynę [VRE])
- zakażenia przeszczepionego narządu
- zakażenia obecne u biorcy przed przeszczepieniem narządu
- zakażenie HSV
- reaktywacja lub nowe zakażenie
Od 2 do 6 miesiąca po transplantacji zakażenia u biorców przeszczepu związane są głównie z:
- reaktywacją lub nowym zakażeniem
- zakażeniem wirusowym: CMV, EBV, HCV, HBV, HHV 6, HIV
- zakażeniami oportunistycznymi spowodowanymi immunosupresją (Pneumocystis carinii, Nocardia, Listeria)
Zakażenia u biorców przeszczepu występujące po upływie 6 miesięcy od transplantacji zależą między innymi od rodzaju i nasilenia immunosupresji. U otrzymujących tzw. małą immunosupresję najczęściej obserwuje się zakażenia podobne do występujących w ogólnej populacji: zakażenia wirusowe dróg oddechowych, grypę, paragrypę, wirus syncytium nabłonka oddechowego (RSV), zakażenia pneumokokowe, zakażenia układu moczowego (80% biorców nerek).
Pacjenci otrzymujący zwiększoną immunosupresję, np. w związku z częstymi epizodami ostrego lub przewlekłego odrzucania, są bardziej podatni na wystąpienie zakażeń, a szczególnie zwiększone jest u nich ryzyko zakażeń oportunistycznych, takich jak Legionella pneumophila, Toxoplasma gondii, i grzybiczych (Candida albicans,Aspergillus) oraz CMV.
Większość zakażeń CMV u pacjentów w ciągu 1-4 miesięcy po przeszczepieniu wątroby zależy od stanu serologicznego biorca-dawca, stosowanej immunosupresji, przeszczepionego narządu.1,2,8,26 Ocenia się, że zakażenie bezobjawowe lub zakażenie CMV występują u 8% biorców nerki, 29% wątroby, 25% serca, 50% trzustki, 22% jelita cienkiego i 38% biorców płuca i serca.
W przebiegu zakażenia CMV najczęściej mamy do czynienia z postacią gorączkową (której mogą towarzyszyć bóle mięśni, stawów) oraz zespołem mononukleozopodobnym. Rzadziej występują supresja szpiku (leukopenia, trombocytopenia), zapalenie wątroby, jelit, śródmiąższowe zapalenie płuc, zapalenie mięśnia sercowego, zapalenie siatkówki.26
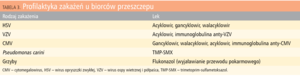
W celu rozpoznania zakażenia CMV stosowane są badania serologiczne (wykrycie swoistych przeciwciał klasy IgM i IgG – najczęściej immunoenzymatyczną metodą ELISA), metody biologii molekularnej opartej na analizie kwasów nukleinowych (najczęściej reakcja łańcuchowa polimerazy [polymerase chain reaction, PCR]) czy reakcja łańcuchowa polimerazy z odwrotną transkryptazą (RT-PCR). Pozwala ona na odróżnienie aktualnie toczącego się zakażenia CMV od zakażenia latentnego. W leczeniu zakażenia CMV stosuje się gancyklowir dożylnie oraz w wybranych przypadkach hiperimmunizowaną globulinę anty-CMV. Zalecane jest przedłużone leczenie doustne walgancyklowirem. W przypadku niepowikłanego zakażenia rokowanie jest dobre. Jeśli jednak zakażenie CMV towarzyszy przewlekłemu odrzucaniu, rokowanie jest poważne (możliwość utraty przeszczepu lub nawet zgonu chorego). Obecnie zaleca się leczenie wyprzedzające (przed wystąpieniem objawów) oraz profilaktykę zakażeń CMV u biorców przeszczepu, szczególnie seronegatywnych.26 Zalecane leczenie profilaktyczne u pacjentów po przeszczepieniu narządu przedstawiono w tabeli 3.
Potransplantacyjna choroba limfoproliferacyjna
Potransplantacyjna choroba limfoproliferacyjna (posttransplantation lymphoproliferative disease, PTLD) jest jednym z najczęstszych powikłań przewlekłej immunosupresji, jakiej są poddani biorcy narządów.1,2,8,27,28 Wtórne nowotwory, w tym rozrosty układu chłonnego, zwane potransplantacyjnymi zespołami limfoproliferacyjnymi, występują stosunkowo rzadko – dotyczą około 1% biorców, choć w przypadku intensywnej immunosupresji (stosowanej na przykład przy przeszczepieniach serca i płuc) mogą sięgać nawet 20%. Zarówno u dzieci, jak i u dorosłych proliferacja dotyczy głównie (w ok. 85% przypadków) limfocytów B i ma związek z zakażeniem wirusem Epsteina-Barr, w ok. 15% przypadków rozrost obejmuje limfocyty T, a niezwykle rzadko komórki NK.
PTLD jest jednym z najcięższych i zagrażających życiu powikłań po przeszczepieniu narządów. Obserwowana jest zależność między silną immunosupresją a częstością występowania PTLD.27,28
Objawy PTLD są zwykłe mało charakterystyczne. Może to być gorączka, zapalenie jamy ustnej, zapalenie gardła, biegunka, utrata masy ciała, bóle brzucha, krwawienie z przewodu pokarmowego, niedokrwistość, hipoalbuminemia lub tzw. zespól mononukleozopodobny z lub bez limfadenopatii. W zaawansowanych przypadkach stwierdza się jeden lub więcej guzów węzłowych lub pozawęzłowych z najczęstszą lokalizacją w jamie brzusznej, klatce piersiowej lub OUN lub postać rozsianą o piorunującym posocznicopodobnym przebiegu.
O nowotworowym charakterze zmian w PTLD decydują badania histologiczne i immunohistochemiczne.27,28 W ramach diagnostyki PTLD zależnej od zakażenia EBV wykonywane są następujące badania:
- monitorowanie wiremii (EBV PCR)
- morfologia krwi, proteinogram, obecność białka monoklonalnego we krwi
- cytometria przepływowa
- stężenie immunoglobulin
- ocena powiększenia węzłów chłonnych (badanie przedmiotowe, USG, RTG, TK)
- badanie histologiczne (węzły chłonne, bioptat wątroby, biopsja jelita)
W ramach profilaktyki PTLD należy unikać nadmiernej immunosupresji. W leczeniu zaleca się w pierwszym rzędzie redukcję lub zaprzestanie immunosupresji oraz gancylowir. W przypadkach opornych na wyżej wymienione leczenie zastosowanie znajdują przeciwciała monoklonalne skierowane przeciwko limfocytom B (szczególnie rytuksymab), a w przypadku zmian zlokalizowanych – operacja, chemioterapia lub naświetlania.
Dziecko gorączkujące po przeszczepieniu wątroby
W praktyce pediatrycznej bardzo częstym problemem jest występowanie stanów gorączkowych i nie omija to oczywiście dzieci po przeszczepieniu narządu miąższowego. U tych dzieci konieczne jest zebranie dodatkowo dokładnego wywiadu dotyczącego problemów pooperacyjnych, w tym zwłaszcza związanych z obecnością cewników dożylnych typu vascuport, cewnika centralnego lub drenów. W każdym przypadku gorączki o nieustalonej etiologii obowiązuje kontrola morfologii, CRP, ewentualnie prokalcytoniny, badanie ogólne moczu i ewentualnie posiew moczu oraz zachowanie czujności, jeśli gorączka utrzymuje się ponad 24 godziny, a etiologia nie została ustalona. U pacjentów po transplantacji wskazane jest agresywne leczenie wszelkich zakażeń oraz konieczna osłona antybiotykowa w trakcie wszelkich zabiegów naruszających ciągłość tkanek (np. przed zabiegami stomatologicznymi ekstrakcji zęba). Przy przedłużającym się zakażeniu u dziecka po transplantacji wskazany jest kontakt z ośrodkiem wykonującym przeszczepienie narządu ze względu na możliwość rozwoju PTLD.1,2,8,27,28