Innym rekomendowanym w profilaktyce PEP postępowaniem jest agresywne nawadnianie pacjenta roztworem Ringera z dodatkiem mleczanów. Powinno być ono wdrażane u wszystkich pacjentów z przeciwwskazaniami do doodbytniczego podania NLPZ. Agresywne nawadnianie pacjentów należy prowadzić według następujących zasad:
- 3 ml/kg/h podczas ECPW
- bolus 20 ml/kg bezpośrednio po ECPW
- 3 ml/kg/h do 8 h po ECPW.
W przypadku powyższego postępowania należy zachować szczególną ostrożność u pacjentów z ryzykiem przeciążenia objętościowego łożyska naczyniowego tj. osób w starszym wieku, obciążonych chorobami sercowo-naczyniowymi oraz niewydolnością nerek. Ponadto agresywne nawadnianie roztworem Ringera z dodatkiem mleczanów nie powinno być prowadzone u pacjentów poddawanych ECPW w trybie ambulatoryjnym1.
U pacjentów z przeciwwskazaniami do podania NLPZ lub agresywnego nawodnienia w profilaktyce PEP zalecanym postępowaniem jest podjęzykowe podanie 5 mg nitrogliceryny 5 min przed ECPW. Mimo że zmniejsza to częstość występowania PEP, to pozostaje bez wpływu na stopień ciężkości omawianego powikłania. Innym nitratem, który znajduje zastosowanie w profilaktyce PEP, jest monoazotan izosorbidu, również podawany w dawce 5 mg na 5 min przed zabiegiem. Ponadto wykazano, że kombinacja nitratów i NLPZ jest skuteczniejsza w prewencji PEP niż wyłącznie doodbytnicze NLPZ4. Podanie nitrogliceryny w postaci transdermalnej lub miejscowej (bezpośrednio na brodawkę dwunastniczą) nie zapobiega występowaniu PEP i nie jest obecnie rekomendowane. Do działań niepożądanych nitratów zaliczane są przede wszystkim bóle głowy oraz epizody hipotensji.
Do substancji farmakologicznych, które obecnie nie są rekomendowane w prewencji PEP, zaliczane są somatostatyna i jej analog oktreotyd, inhibitory proteaz, tj. nafamostat, gabeksat i ulinastatyna, jak również nitrogliceryna podawana miejscowo bezpośrednio na brodawkę dwunastniczą po ECPW1.
Inne rekomendowane metody
Do innych rekomendowanych przez towarzystwa naukowe (ESGE, ASGE) zasad profilaktyki PEP zaliczane jest protezowanie przewodu trzustkowego. To postępowanie wskazane jest u pacjentów narażonych na duże ryzyko wystąpienia omawianego powikłania, np. w sytuacji niezamierzonego wprowadzenia prowadnicy do przewodu trzustkowego, zakontrastowania przewodu trzustkowego czy uzyskania kaniulacji przewodu żółciowego za pomocą techniki dwóch prowadnic. Należy jednak podkreślić, że rutynowe protezowanie przewodu trzustkowego w pozostałych przypadkach nie jest zalecane. Rekomendowane jest użycie krótkich plastikowych stentów średnicy 5 Fr, bez wewnętrznego zaczepu, ale z zaczepem od strony dwunastnicy. Alternatywnie można wykorzystać stent typu single pigtail. Położenie stentu powinno być ocenione radiologicznie po 5-10 dniach od zabiegu. W przypadku braku samoistnej ewakuacji stentu należy go usunąć po tym czasie endoskopowo1.
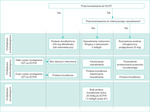
Rycina 2. Profilaktyka ostrego zapalenia trzustki po ECPW według Dumonceau i wsp.1 (modyfikacja własna)
W prospektywnym, randomizowanym badaniu, obejmującym 1950 pacjentów, które opublikowali Elmunzer i wsp.5 w 2024 roku, oceniano skuteczność NLPZ w połączeniu z protezowaniem przewodu trzustkowego w zapobieganiu PEP u pacjentów z grupy podwyższonego ryzyka wystąpienia tego powikłania (wywiad PEP, tzw. trudna kaniulacja [>6 prób kaniulacji dróg żółciowych lub czas trwania kaniulacji >6 min], nacięcie wstępne [precut], sfinkteroplastyka balonowa, kliniczne podejrzenie dysfunkcji zwieracza Oddiego, zakontrastowanie przewodu trzustkowego, sfinkterotomia trzustkowa)5. W cytowanym badaniu wykazano, że zastosowanie wyłącznie indometacyny wiąże się z wyższym odsetkiem wystąpienia PEP w porównaniu z postępowaniem obejmującym dodatkowo protezowanie przewodu trzustkowego (14,9% vs 11,3%). Powyższe rozważania sugerują zasadność identyfikacji pacjentów z grupy podwyższonego ryzyka wystąpienia PEP i zastosowania u nich profilaktyki farmakologicznej oraz protezowania przewodu trzustkowego.
Zasady zapobiegania PEP podsumowano na rycinie 2.
Postępowanie
Postępowanie w przypadku wystąpienia PEP nie różni się zasadniczo od stosowanego u pacjenta z OZT o innej etiologii. W zależności od stopnia ciężkości obejmuje: intensywne nawodnienie, leczenie przeciwbólowe, leczenie żywieniowe oraz antybiotykoterapię (w uzasadnionych przypadkach, takich jak zakażenie martwicy trzustki lub współistniejące zakażenie). Szczegółowe zasady postępowania są przedmiotem opublikowanych wytycznych i wykraczają poza zakres niniejszego opracowania6. Na uwagę zasługują próby tzw. ratunkowego protezowania przewodu trzustkowego, które są podejmowane u pacjentów z PEP o ciężkim przebiegu (nasilony ból brzucha, ponad 10-krotne zwiększenie aktywności amylazy i lipazy, podwyższone stężenie białka C-reaktywnego, leukocytoza), aczkolwiek wyniki badań dotyczących omawianego zagadnienia są niejednoznaczne. Ponadto takie postępowanie może zwiększać odsetek zakażenia martwicy trzustki u pacjentów z PEP. Z tego względu w opublikowanych rekomendacjach nie zaleca się rutynowo ratunkowego protezowania przewodu trzustkowego1.
Powikłania infekcyjne
Definicja i częstość występowania
Powikłania infekcyjne po ECPW obejmują ostre zapalenie dróg żółciowych oraz ostre zapalenie pęcherzyka żółciowego. Ostre zapalenie dróg żółciowych definiowane jest jako wystąpienie po ECPW gorączki >38°C przez >24 h ze współistniejącą cholestazą. Ostre zapalenie pęcherzyka żółciowego powoduje ból w prawym górnym kwadrancie brzucha, wzrost parametrów zapalnych oraz charakterystyczne cechy w badaniach obrazowych, które pojawiły się po ECPW. Powikłania infekcyjne po ECPW występują w 1,4-5% przypadków. Spośród nich 20% charakteryzuje się ciężkim przebiegiem, a całkowita śmiertelność z powodu powikłań infekcyjnych po ECPW sięga 0,11%.
Czynniki ryzyka
Źródłem infekcji po ECPW mogą być zarówno patogeny endogenne (flora górnego odcinka przewodu pokarmowego i skóry pacjenta), jak i patogeny egzogenne (Pseudomonas aeruginosa, Klebsiella pneumoniae, Enterobacter cloacae, Escherichia coli)1,7. Podatne na powikłania infekcyjne po ECPW są głównie osoby z obniżoną odpornością, ciężkimi chorobami układu krwiotwórczego z neutropenią oraz pacjenci po transplantacji wątroby. Udokumentowanym czynnikiem ryzyka powikłań infekcyjnych jest niekompletny drenaż żółci, dotyczący przede wszystkim pacjentów z niedrożnością dróg żółciowych na poziomie wnęki wątroby (guz Klatskina w stopniu zaawansowania III i IV według klasyfikacji Bismutha-Corlette’a), zaawansowaną kamicą żółciową, torbielowatością wewnątrzwątrobowych dróg żółciowych (chorobą Carolego) lub z pierwotnym stwardniającym zapaleniem dróg żółciowych (PSC – primary sclerosing cholangitis)8. Czynnikiem ryzyka powikłań infekcyjnych jest też cholangioskopia, a bakteriemię po tym badaniu stwierdza się u 13,9% pacjentów. Do innych czynników ryzyka zaliczane są zabiegi terapeutyczne w obrębie dróg żółciowych, takie jak pobieranie biopsji czy poszerzanie zwężeń. Ryzyka powikłań infekcyjnych nie zwiększają natomiast marskość wątroby, niewielkie doświadczenie operatora czy obecność uchyłku okołobrodawkowego1. Dlatego przed ECPW u pacjentów z wyżej wymienionymi czynnikami ryzyka zalecana jest profilaktyczna antybiotykoterapia dostosowana do lokalnych warunków epidemiologicznych.
Zapobieganie
Najlepszym sposobem zapobiegania powikłaniom infekcyjnym jest używanie jednorazowych duodenoskopów do ECPW, a wskazania do ich zastosowania określono w tabeli 4.
