IV edycja Kongresu HPV już 12-13 czerwca! Poznaj najnowsze trendy w profilaktyce, diagnostyce i leczeniu raka szyjki macicy i innych schorzeń związanych z HPV | Sprawdź >
Współczesne wytyczne jednoznacznie podkreślają konieczność włączenia doustnego inhibitora receptora P2Y12 u wszystkich pacjentów hospitalizowanych z powodu ACS, zarówno ze STEMI, jak i ostrym zespołem wieńcowym bez uniesienia odcinka ST (NSTE-ACS – non-ST-segment elevation acute coronary syndrome), jako uzupełnienia terapii ASA (klasa zaleceń 1, poziom dowodów A).
W badaniach klinicznych – TRITON-TIMI 38 (Trial to Assess Improvement in Therapeutic Outcomes by Optimizing Platelet Inhibition With Prasugrel-Thrombolysis In Myocardial Infarction 38), dotyczącym prasugrelu, oraz PLATO, dotyczącym tikagreloru – wykazano, że oba leki istotnie redukują ryzyko złożonego punktu końcowego obejmującego śmiertelność sercowo-naczyniową, zawał mięśnia sercowego oraz udar mózgu, o 16-20% względem klopidogrelu4,5. Ponadto obserwowano zmniejszenie częstości występowania zakrzepicy w stencie. W badaniu PLATO stwierdzono również istotne statystycznie, choć umiarkowane, obniżenie śmiertelności całkowitej w grupie leczonej tikagrelorem. W populacji pacjentów ze STEMI uczestniczących w badaniu TRITON-TIMI 38 stosowanie prasugrelu wiązało się z 21% redukcją częstości występowania MACE oraz 42% redukcją zakrzepicy w stencie podczas 15-miesięcznej obserwacji, bez istotnego zwiększenia ryzyka krwawień6.
W omawianych wytycznych podkreślono, że tikagrelor może powodować przemijającą duszność nawet u 10-15% pacjentów po przebytym ACS. Prasugrel jest natomiast przeciwwskazany u pacjentów z przebytym udarem mózgu lub przemijającym atakiem niedokrwiennym (TIA – transient ischemic attack) z uwagi na zwiększone ryzyko niekorzystnych wyników klinicznych, co wykazano w analizie wtórnej badania TRITON-TIMI 38 (klasa zaleceń 3 [szkodliwość], poziom dowodów B-R)4. W populacji osób ≥75 r.ż. lub z masą ciała <60 kg należy rozważyć z kolei redukcję dawki prasugrelu.
Na podstawie powyższych badań u pacjentów ze STEMI poddawanych PPCI preferowane jest stosowanie prasugrelu lub tikagreloru ze względu na ich udowodnioną skuteczność w redukcji MACE i ryzyka zakrzepicy w stencie (klasa zaleceń 1, poziom dowodów B-R). Jeśli jednak dostępność tych leków jest ograniczona, są przeciwwskazane lub źle tolerowane, klopidogrel stanowi rekomendowaną alternatywę (klasa zaleceń 1, poziom dowodów C-LD).
Z kolei u pacjentów z NSTE-ACS poddawanych PCI rekomenduje się stosowanie prasugrelu lub tikagreloru w celu redukcji ryzyka MACE oraz zakrzepicy w stencie (klasa zaleceń 1, poziom dowodów B-R).
W randomizowanym badaniu CHAMPION PHOENIX (Cangrelor Versus Standard Therapy to Achieve Optimal Management of Platelet Inhibition) oceniano skuteczność kangreloru w porównaniu z klopidogrelem u pacjentów poddawanych PCI z powodu ostrych lub przewlekłych zespołów wieńcowych7,8. Kangrelor podawano w bolusie dożylnym przed zabiegiem, po czym kontynuowano we wlewie przez co najmniej 2 godziny lub do zakończenia PCI. W ciągu 48 godzin od zabiegu częstość występowania złożonego punktu końcowego (zgonu z jakiejkolwiek przyczyny, zawału mięśnia sercowego, rewaskularyzacji zależnej od niedokrwienia lub zakrzepicy w stencie) była istotnie niższa w grupie leczonej kangrelorem. Korzyści te odnotowano zarówno wśród pacjentów z NSTE-ACS, jak i STEMI.
W związku z tym wg omawianych wytycznych wśród pacjentów z ACS poddawanych PCI, u których nie zastosowano wcześniej inhibitora receptora P2Y12, dożylne podanie kangreloru może stanowić rozsądną opcję terapeutyczną w celu redukcji okołozabiegowych incydentów niedokrwiennych (klasa zaleceń 2b, poziom dowodów B-R).
U pacjentów z ACS poddawanych PCI, u których stwierdza się dużą masę skrzepliny, zjawisko no-reflow lub zwolniony przepływ wieńcowy, zastosowanie inhibitora receptora glikoproteinowego IIb/IIIa w formie dożylnej lub dojelitowej może być uzasadnione jako terapia wspomagająca w celu poprawy skuteczności zabiegu oraz ograniczenia rozległości zawału (klasa zaleceń 2a, poziom dowodów C-LD). Należy jednak zaznaczyć, że owe leki nie powinny być stosowane rutynowo, ze względu na brak udowodnionych korzyści w zakresie redukcji incydentów niedokrwiennych oraz istotnie zwiększone ryzyko krwawień (klasa zaleceń 3, poziom dowodów B-R).
Leczenie hipolipemizujące
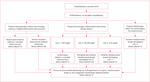
W wytycznych istotny rozdział odzwierciedlający dynamiczny rozwój w dziedzinie lipidologii poświęcono leczeniu hipolipemizującemu. U pacjentów z ACS zaleca się stosowanie intensywnej terapii statynami w celu zmniejszenia ryzyka wystąpienia MACE (klasa zaleceń 1, poziom dowodów A). Podział terapii na poszczególne poziomy intensywności przedstawiono na rycinie 1. Co ważne, u wspomnianej grupy chorych dopuszcza się także jednoczesne rozpoczęcie terapii ezetymibem w skojarzeniu z maksymalnie tolerowaną dawką statyny w celu redukcji ryzyka MACE (klasa zaleceń 2b, poziom dowodów B-R).
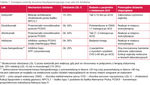
U chorych z ACS, którzy otrzymują już maksymalnie tolerowaną terapię statynami i u których stężenie cholesterolu frakcji lipoprotein o niskiej gęstości (LDL-C – low-density lipoprotein cholesterol) utrzymuje się na poziomie ≥70 mg/dl (≥1,8 mmol/l), zaleca się dodanie leku hipolipemizującego niebędącego statyną w celu dalszej redukcji ryzyka MACE (klasa zaleceń 1, poziom dowodów A). Warto jednak pamiętać o sile poszczególnych metod leczenia farmakologicznego (tab. 1). W przypadku niższego stężenia LDL-C, mieszczącego się w zakresie 55-69 mg/dl (1,4-<1,8 mmol/l), rozważenie takiego postępowania również jest uzasadnione, choć rekomendacja ma wówczas niższą siłę (klasa zaleceń 2a, poziom dowodów B-R).
Badania kliniczne inhibitorów proteinowej konwertazy subtylizyny/keksyny typu 9 (PCSK9 – proprotein convertase subtilisin/kexin type 9) wykazały 15% względne zmniejszenie ryzyka MACE w ciągu 2-3 lat u pacjentów po ponad miesiącu od ACS, przy czym większe korzyści odnotowano u osób włączonych bliżej tego zdarzenia9,10. Ewolokumab skutecznie redukuje stężenie LDL-C we wczesnym okresie po ACS i powoduje korzystne zmiany w składzie blaszki miażdżycowej oceniane za pomocą obrazowania wewnątrznaczyniowego u chorych z NSTE-ACS. Podobne efekty regresji blaszki zaobserwowano u pacjentów leczonych alirokumabem po zawale mięśnia sercowego11. Inklisiran obniża stężenie LDL-C poprzez hamowanie translacji mRNA kodującego białko PCSK9. Mimo braku danych dotyczących wpływu leku na twarde punkty końcowe przyjmuje się, że korzyść kliniczna będzie proporcjonalna do uzyskanej redukcji LDL-C12.
U pacjentów z ACS, u których występuje nietolerancja statyn, zaleca się zastosowanie terapii hipolipemizującej opartej na lekach nienależących do tej grupy. Dostępne opcje terapeutyczne obejmują ezetymib, przeciwciała monoklonalne przeciw PCSK9, inklisiran i kwas bempediowy. Takie postępowanie ma na celu obniżenie stężenia LDL-C oraz redukcję ryzyka wystąpienia MACE (klasa zaleceń 1, poziom dowodów B-R). Również tutaj należy pamiętać o sile poszczególnych metod leczenia farmakologicznego (tab. 1). Rozpoznanie nietolerancji statyn wymaga próby leczenia co najmniej dwoma różnymi lekami z tej grupy, w tym jednym podawanym w najniższej zatwierdzonej dawce dziennej.
Kolchicyna
W wytycznych pojawiła się również kwestia przewlekłego przyjmowania kolchicyny przez pacjenta po ACS. Jako naturalny lek przeciwzapalny stosowany m.in. w leczeniu dny moczanowej działa ona poprzez zmniejszenie przylegania neutrofili do śródbłonka i płytek krwi oraz obniżenie stężenia białka C-reaktywnego, wskutek czego wpływa na redukcję objętości niestabilnych blaszek miażdżycowych u pacjentów już leczonych ASA i statynami. Badania kliniczne pokazują, że stosowanie niskiej dawki kolchicyny 0,5-0,6 mg/24 h po zawale serca redukuje ryzyko MACE o ok. 30%13.
Zgodnie z omawianymi wytycznymi niskie dawki kolchicyny 0,5 mg/24 h mogą być rozważane jako terapia dodatkowa po ostrym zawale serca u pacjentów leczonych standardowo ASA i statynami. Obecnie prowadzone są dalsze badania oceniające skuteczność i bezpieczeństwo tego leczenia (klasa zaleceń 2b, poziom dowodów B-R).