Tabela 2. Skala National Institutes of Health Stroke Scale (NIHSS)*
|
Oceniany parametr |
Punktacja |
Nasilenie |
|
IA Świadomość |
0 |
Przytomny |
|
1 |
Podsypiający |
|
|
2 |
Splątany |
|
|
3 |
Nieprzytomny |
|
|
IB Orientacja auto- i allopsychiczna |
0 |
Prawidłowa odpowiedź na dwa pytania (np. dotyczące czasu lub danych osobowych chorego) |
|
1 |
Prawidłowa odpowiedź na jedno pytanie |
|
|
2 |
Nieprawidłowa odpowiedź na oba pytania |
|
|
IC Spełnianie poleceń |
0 |
Prawidłowe wykonanie dwóch poleceń (np. zaciśnięcia dłoni i otwarcia oczu) |
|
1 |
Prawidłowe wykonanie jednego polecenia |
|
|
2 |
Niewykonanie poleceń |
|
|
II Ruchomość gałek ocznych |
0 |
Prawidłowa |
|
1 |
Zbaczanie gałek ocznych (skierowanie gałek ocznych w stronę objętej niedokrwieniem półkuli mózgu) |
|
|
2 |
Przymusowe ustawienie gałek ocznych |
|
|
III Pole widzenia |
0 |
Prawidłowe |
|
1 |
Częściowe niedowidzenie połowicze (kwadrantowe) |
|
|
2 |
Całkowite niedowidzenie połowicze |
|
|
3 |
Obustronne niedowidzenie połowicze |
|
|
IV Porażenie nerwu twarzowego (symetria twarzy) |
0 |
Nie stwierdza się |
|
1 |
Niewielki niedowład n. VII (wygładzenie fałdu nosowo-wargowego) |
|
|
2 |
Częściowe porażenie n. VII (niedowład dolnej części twarzy) |
|
|
3 |
Całkowite porażenie n. VII (niedowład dolnej i górnej części twarzy) |
|
|
V Siła mięśniowa kończyn górnych |
0 |
Prawidłowa, chory utrzymuje kończynę pod kątem 90° (lub 45°) przez 10 s |
|
1 |
Chory utrzymuje kończynę pod kątem 90° (lub 45°) krócej niż 10 s |
|
|
2 |
Zachowany jest opór przeciw sile ciężkości (pacjent może przesunąć kończynę po płaskiej powierzchni) |
|
|
3 |
Ślad ruchu |
|
|
4 |
Brak jakiegokolwiek ruchu w kończynie |
|
|
VI Siła mięśniowa kończyn dolnych |
0 |
Prawidłowa, chory utrzymuje kończynę pod kątem 30° przez 5 s |
|
1 |
Kończyna opada przed upływem 5 s |
|
|
2 |
Zachowany jest opór przeciw sile ciężkości (pacjent może przesunąć kończynę po płaskiej powierzchni) |
|
|
3 |
Ślad ruchu |
|
|
4 |
Brak jakiegokolwiek ruchu w kończynie |
|
|
VII Ataksja kończyn (w próbie palec-nos i pięta-kolano) |
0 |
Nieobecna |
|
1 |
Obecna w jednej kończynie |
|
|
2 |
Obecna w dwóch kończynach |
|
|
VIII Czucie powierzchniowe |
0 |
Prawidłowe |
|
1 |
Niewielkie osłabienie czucia |
|
|
2 |
Znaczne osłabienie lub całkowity brak czucia |
|
|
IX Mowa |
0 |
Prawidłowa |
|
1 |
Łagodna afazja |
|
|
2 |
Nasilona afazja |
|
|
3 |
Całkowita afazja (niemożność mówienia lub rozumienia mowy albo utrata obu tych modalności) |
|
|
X Dyzartria |
0 |
Brak |
|
1 |
Łagodna |
|
|
2 |
Ciężka |
|
|
XI Zespół zaniedbywania połowiczego |
0 |
Brak |
|
1 |
Niemożność różnicowania strony działania bodźca jednego rodzaju (dotyku, dźwięku, wzroku) |
|
|
2 |
Niemożność różnicowania strony działania więcej niż jednego bodźca |
* Im wyższa punktacja, tym zwykle większy deficyt neurologiczny, co w uproszczeniu oznacza rozleglejsze ognisko niedokrwienia lub ognisko w rejonie przebiegu dróg ruchowych lub czuciowych (np. w torebce wewnętrznej).
Ich znajomość nie jest niezbędna w przypadku lekarzy innych specjalności niż neurolodzy, natomiast pozwala ocenić nasilenie objawów, a co za tym idzie – założyć, że im większy deficyt (a więc wyższa punktacja), tym zwykle rozleglejsze ognisko niedokrwienia (z zakresu unaczynienia większej tętnicy), a przez to czas wdrożenia leczenia istotniejszy. W uproszczeniu można przyjąć, że deficyt obejmujący objawy ze strony nerwów czaszkowych i kończyn spowodowany jest niedokrwieniem większego obszaru. Niemniej w przypadku niedokrwienia struktur głębokich (np. torebki wewnętrznej) lub pnia mózgu nawet niewielki udar może być przyczyną znacznego deficytu. W związku z tym w wytycznych3,4 funkcjonuje pojęcie istotnego deficytu, do którego należy zaliczyć np. afazję i niedowidzenia połowicze, które mimo iż w dostępnych skalach udarowych uzyskują małą punktację, są objawami silnie inwalidyzującymi, a więc wymagają intensywnego leczenia.
Po wysunięciu podejrzenia udaru mózgu, najlepiej jeszcze w izbie przyjęć lub na SOR, zanim rozpocznie się diagnostykę radiologiczną, należy pobrać krew w celu przeprowadzenia podstawowych badań laboratoryjnych, obejmujących morfologię (z oceną liczby płytek krwi), koagulogram (z uwzględnieniem parametrów ocenianych podczas terapii przeciwkrzepliwej prowadzonej zarówno za pomocą klasycznych, jak i nowych leków przeciwkrzepliwych), oznaczenie stężenia glukozy, elektrolitów, parametrów nerkowych i wątrobowych, gazometrię (jeśli to konieczne).2,4 Ponieważ testy oceniające aktywność nowych leków przeciwkrzepliwych (ECT i TT dla bezpośrednich inhibitorów trombiny oraz anty-Xa dla inhibitorów czynnika Xa) oraz określające ich stężenie we krwi nie są powszechnie dostępne, natomiast donoszono o wpływie dabigatranu, rywaroksabanu i apiksabanu na inne parametry krzepnięcia (aPTT i PT),8 powinno założyć się, że nieprawidłowe wyniki testów laboratoryjnych, takich jak APTT (u przyjmujących dabigatran) czy PT (u przyjmujących np. rywaroksaban), świadczą o tym, że pacjent jest skutecznie leczony przeciwkrzepliwe i nie jest kandydatem do leczenia trombolitycznego.2,9 Zakres pozostałych badań (np. toksykologicznych) zależy od indywidualnej oceny prawdopodobieństwa innych przyczyn wystąpienia objawów neurologicznych. Markery martwicy mięśnia sercowego są podwyższone u 5-36% chorych w ostrej fazie udaru mózgu,10 dlatego ich oceny należy dokonywać w odpowiednim kontekście klinicznym. Dodatkowe badania (EKG, RTG klatki piersiowej) nie powinny opóźniać wdrożenia leczenia trombolitycznego, niemniej EKG należy wykonać najszybciej, jak to możliwe. Należy ponadto zapewnić dostęp dożylny, jeśli nie zrobił tego personel karetki pogotowia, i rozpocząć umiarkowaną płynoterapię (płynami izotonicznymi). Nie należy stosować leków podawanych doustnie.
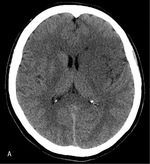
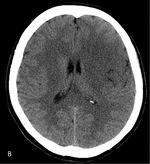
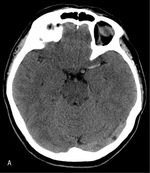
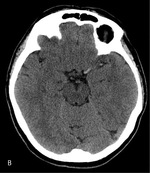
Standardem postępowania radiologicznego jest badanie metodą tomografii komputerowej (TK) bez kontrastu, które pozwala różnicować udar niedokrwienny i krwotoczny, zlokalizować ognisko niedokrwienia i ocenić jego rozległość oraz ewentualnie wykazać inną przyczynę stwierdzanych objawów. Ponieważ w bardzo wczesnej fazie udaru mózgu obszar niedokrwienia może nie być widoczny, pomocne może się okazać poszukiwanie tzw. wczesnych objawów udaru (zatarcie korowo-podkorowe w rejonie objętym niedokrwieniem [ryc. 1], tzw. objaw hiperdensyjnej tętnicy środkowej [ryc. 2] lub objaw wstęgi), które nie tylko świadczą o tworzącym się ognisku, lecz także pozwalają przewidywać skuteczność wdrożonego leczenia i nasilenie deficytu neurologicznego.
Tak zwany objaw hiperdensyjnej tętnicy środkowej mózgu uznaje się za objaw słabej odpowiedzi na leczenie trombolityczne i jest niekorzystny rokowniczo niezależnie od wdrożonego leczenia, świadczy bowiem o niedrożności tętnicy zaopatrującej ok. 2/3 półkuli mózgu; stanowi również czynnik ryzyka wystąpienia poważnego powikłania udaru niedokrwiennego, jakim jest tzw. złośliwy obrzęk mózgu.
Inne techniki neuroobrazowania (MR, angio-TK lub angio-MR tętnic wewnątrz- lub zewnątrzczaszkowych, perfuzja w TK lub MR) często pozwalają wykazać ognisko niedokrwienne w bardzo wczesnej fazie udaru, gdy nie stwierdza się jeszcze zmian w TK (sekwencja DWI w MR), lub też ujawnić zwężenie albo niedrożność dużych naczyń domózgowych bądź wewnątrzczaszkowych (angio-TK lub angio-MR), lub ocenić obszary potencjalnie odwracalnego niedokrwienia (perfuzja w TK lub MR). Jednak w warunkach ostrego udaru i ograniczonego okna czasowego leczenia trombolitycznego ich wykonanie i przydatność uzyskanych informacji (np. do określenia wskazań do leczenia endowaskularnego) należy ocenić indywidualnie i najlepiej pozostawić do decyzji neurologa. Należy również pamiętać, że zastosowanie niektórych z powyższych metod może być przeciwwskazane u pewnych chorych (np. u osób ze stymulatorem serca w przypadku MR lub niewydolnością nerek w przypadku angio-TK albo badań perfuzyjnych ze względu na konieczność podania środka kontrastowego).
Klasyczna angiografia może się okazać przydatna u chorych, u których rozważa się leczenie wewnątrznaczyniowe niedrożności dużych tętnic mózgowych (tętnicy środkowej mózgu lub tętnicy podstawnej), gdy dożylna terapia trombolityczna okazała się nieskuteczna, jest przeciwwskazana lub pacjent został skierowany do szpitala poza oknem czasowym dożylnego leczenia trombolitycznego, ale w oknie czasowym stosowania trombolizy dotętniczej (tab. 3)11-14 lub mechanicznej embolektomii (tab. 4).15-19 Metody te nie są jednak powszechnie dostępne.
Tabela 3. Wskazania i przeciwwskazania do zastosowania dotętniczego leczenia trombolitycznego
|
Wskazania:
|
|
Kryteria wykluczające:
|
BA (basilar artery) – tętnica podstawna; ICA (internal carotid artery) – tętnica szyjna wewnętrzna; M1 – odcinek M1 (proksymalny) tętnicy środkowej mózgu; M2 – odcinek M2 (dystalny) tętnicy środkowej mózgu; MCA (middle cerebral artery) – tętnica środkowa mózgu; mRS – zmodyfikowana skala Rankina; rt-PA – rekombinowany tkankowy aktywator plazminogenu
Tabela 4. Wskazania do zastosowania mechanicznej embolektomii
|
Niedrożność dużego naczynia (ICA, MCA, BA) |
|
Nieskuteczność dożylnego leczenia trombolitycznego |
|
Przeciwwskazania do podania dożylnego leczenia trombolitycznego |
BA (basilar artery) – tętnica podstawna; ICA (internal carotid artery) – tętnica szyjna wewnętrzna; MCA (middle cerebral artery) – tętnica środkowa mózgu
Wykonywanie badania tętnic domózgowych metodą Dopplera i badania przezczaszkowego (TCD – transcranial doppler) również nie powinno opóźniać wdrożenia leczenia trombolitycznego. Niemniej postępowanie ultrasonograficzne zależy od sytuacji klinicznej (w przypadku podejrzenia rozwarstwienia tętnicy domózgowej jest cennym narzędziem diagnostycznym), dostępności badania i algorytmu terapeutycznego w odpowiednim ośrodku leczenia udarów. Dowiedziono, że TCD jest przydatny nie tylko w ocenie stopnia zwężenia lub niedrożności naczynia docelowego czy ocenie skuteczności rekanalizacji po zastosowanym leczeniu, lecz także we wzmacnianiu efektu terapeutycznego zastosowania rekombinowanego tkankowego aktywatora plazminogenu (rt-PA).20,21
W razie wątpliwości diagnostycznych do rozważenia pozostaje wykonanie nakłucia lędźwiowego (w przypadku podejrzenia krwawienia podpajęczynówkowego przy prawidłowym wyniku badania obrazowego) lub EEG (przy podejrzeniu niedrgawkowego stanu padaczkowego).
Inne badania dodatkowe (echokardiografia przezklatkowa/przezprzełykowa, 24-godzinne monitorowanie EKG lub ciśnienia tętniczego, lipidogram, badanie ogólne moczu, oznaczenie stężenia CRP i pomiar OB) należy wykonać w zależności od wskazań jeszcze w trakcie hospitalizacji z powodu udaru.
Ogólne zasady postępowania terapeutycznego w ostrym udarze niedokrwiennym mózgu
Po przyjęciu chorego na oddział należy rozpocząć uważne monitorowanie funkcji życiowych (oddech, tętno, ciśnienie tętnicze, temperatura ciała). Parametry te należy notować w dokumentacji medycznej co 4 godziny przez pierwszą dobę, a następnie co 12 godzin przez co najmniej 7 dni. W przypadku leczenia trombolitycznego tętno i ciśnienie tętnicze należy mierzyć co 15 minut przez 2 godziny od rozpoczęcia terapii, następnie co 30 minut przez kolejne 6 godzin, potem co godzinę przez następne 16 godzin.2-4 U pacjentów zakwalifikowanych do leczenia trombolitycznego należy przeprowadzić badanie neurologiczne przed podaniem leku i po zakończeniu wlewu rt-PA.
Pacjent powinien pozostawać w pozycji leżącej (jeśli nie ma przeciwwskazań wynikających z innych chorób współistniejących układu krążenia lub oddechowego), która poprawia perfuzję mózgową.2 U pacjentów z zaburzeniami drożności dróg oddechowych lub gdy ryzyko zachłyśnięcia jest duże, można unieść tułów do kąta 30°.
W przypadku zaburzeń oddychania i hipoksji, które występują dość powszechnie w rozległych udarach półkulowych i udarach pnia, należy zapewnić drożność dróg oddechowych, zastosować tlenoterapię (w celu utrzymania saturacji >94%),2 ew. dokonać intubacji i wdrożyć respiratoroterapię zgodnie z zasadami obowiązującymi w innych stanach zagrożenia życia (tab. 5).22
Tabela 5. Wskazania do intubacji i mechanicznej wentylacji
|
Wskazania do intubacji:
|
|
Wskazania do wentylacji mechanicznej:
|
GCS – Glasgow Coma Scale; PaO2 – ciśnienie parcjalne tlenu we krwi tętniczej; PaCO2 – ciśnienie parcjalne dwutlenku węgla we krwi tętniczej