Neurologia
Udar mózgu – etiologia, objawy, diagnostyka, leczenie i profilaktyka wtórna
lek. Michał Kubiak1
dr hab. n. med. Jacek Staszewski, prof. WIM-PIB1,2
- Udar mózgu, jego wybrane rodzaje, przyczyny oraz metody diagnostyczne
- Postępowanie w przypadku udaru w warunkach przedszpitalnych i wczesnoszpitalnych
- Profilaktyka wtórna zależna od przyczyny incydentu
Udar mózgu (UM) jest drugą pod względem częstości występowania przyczyną zgonów oraz główną przyczyną niepełnosprawności osób dorosłych. Mimo wprowadzenia nowych metod leczenia zapadalność jest wysoka, a przebieg udaru zarówno niedokrwiennego (UN), jak i krwotocznego (UK) często pozostaje niepomyślny. Podstawową strategią postępowania w UN jest jak najszybsza rekanalizacja zwężonego naczynia wewnątrzczaszkowego oraz przywrócenie perfuzji w tym obszarze, zaś w UK wczesne leczenie neurochirurgiczne w przypadku krwotoku spowodowanego malformacjami naczyniowymi oraz wczesna stabilizacja hemodynamiczna i przywrócenie hemostazy w przypadku krwawień idiopatycznych lub w przebiegu stosowania leków przeciwkrzepliwych1.
W ostatnich latach w Polsce jest obserwowany istotny wzrost częstości leczenia reperfuzyjnego UN rekombinowanym tkankowym aktywatorem plazminogenu (rtPA – recombinant tissue plasminogen activator) i mechaniczną trombektomią (MT), jednak są one wciąż stosowane średnio u co piątego chorego z UN i zwykle pod koniec standardowego okna terapeutycznego, kiedy ich skuteczność jest najniższa (<4,5 h od zachorowania dla rtPA i <6 h dla MT). Wielokrotnie chorzy zwlekają z wezwaniem pomocy medycznej, w przypadku niewielkich lub intermitujących objawów samodzielnie szukają pomocy doraźnej bądź zgłaszają się do lekarza podstawowej opieki zdrowotnej (POZ), co opóźnia proces diagnostyczno-terapeutyczny. Dodatkowo co czwarty chory skierowany na szpitalny oddział ratunkowy (SOR) w oknie terapeutycznym nie zdąży otrzymać leczenia wskutek opóźnień związanych z diagnostyką lub transportem międzyszpitalnym do ośrodka wykonującego MT. Od niedawna możliwości leczenia reperfuzyjnego rozszerzyły się do 9 godzin dla rtPA i nawet 24 godzin dla MT u chorych spełniających kryteria radiologiczne, tzw. niewspółmierności rozmiaru zmian w badaniu dyfuzyjnym rezonansu magnetycznego (MR) lub tomografii komputerowej (TK) z opcją perfuzji. Niemniej tacy chorzy stanowią mniej niż 10% wszystkich pacjentów z UN, a diagnostyka jest dostępna tylko w nielicznych ośrodkach w trybie 24/7.
Przypadek 1 – przemijające niedokrwienie mózgu

Tabela 2. Skale oceny ryzyka wystąpienia udaru niedokrwiennego po przemijającym niedokrwieniu mózgu (TIA): ABCD2 i ABCD3
Pacjentka w wieku 62 lat zgłosiła się samodzielnie na SOR z powodu wystąpienia przed 4 godzinami nagłego osłabienia siły mięśniowej prawej kończyny górnej i bełkotliwej mowy. Według jej relacji epizod trwał około 5 minut, wystąpił pierwszy raz w życiu, nie był poprzedzony objawami prodromalnymi. Wśród obciążeń wymieniała nadciśnienie tętnicze oraz cukrzycę typu 2. Badanie neurologiczne bez istotnych odchyleń, w National Institutes of Health Stroke Scale (NIHSS, tab. 1) 0 pkt, w badaniu internistycznym zarejestrowano hipertensję (ciśnienie tętnicze 180/110 mmHg) i szmer skurczowy nad tętnicami szyjnymi. Tomogram bez wzmocnienia kontrastowego nie wykazał cech krwawienia śródczaszkowego ani innych istotnych zmian ogniskowych, stwierdzono natomiast hiperintensywny sygnał wewnątrzczaszkowych odcinków tętnic szyjnych. W badaniu EKG: rytm zatokowy miarowy, zapis prawidłowy. Wstępnie rozpoznano przemijający epizod niedokrwienny (TIA – transient ischemic attack). W skali ABCD2 (tab. 2) pacjentka uzyskała 8 punktów i została przyjęta do kliniki neurologicznej w celu przeprowadzenia diagnostyki oraz ustalenia optymalnej prewencji wtórnej.
W trybie pilnym podano dawkę nasycającą klopidogrelu (C) 300 mg oraz kwas acetylosalicylowy (ASA) 150 mg, ponadto zalecono stosowanie podwójnej terapii przeciwpłytkowej (DAPT – dual antiplatelet therapy) C + ASA w dawkach 75 mg/24 h przez kolejne 21 dni, następnie w monoterapii C lub ASA, a także atorwastatynę w dawce 80 mg/24 h. W badaniach dodatkowych stwierdzono zaburzenia gospodarki lipidowej z przewagą cholesterolu frakcji LDL (LDL-C) (280 mg/dl), w badaniu USG doppler tętnic dogłowowych krytyczne zwężenie lewej tętnicy szyjnej wewnętrznej do 90% według North American Symptomatic Carotid Endarterectomy Trial (NASCET), w automatycznej całodobowej rejestracji ciśnienia tętniczego (ABPM – ambulatory blood pressure monitoring) wykazano jego nieprawidłową kontrolę (średnia dobowa 160/95 mmHg), w badaniu EKG metodą Holtera nie stwierdzono migotania przedsionków (MP). Po konsultacji radiologa interwencyjnego i chirurga naczyniowego chora została zakwalifikowana do pilnego zabiegu wewnątrznaczyniowej angioplastyki lewej tętnicy szyjnej wewnętrznej (LICA – left internal carotid artery) z implantacją stentu, który bez powikłań wykonano w 7 dobie od wystąpienia incydentu TIA.
Przypadek 2 – udar niedokrwienny mózgu leczony reperfuzyjnie
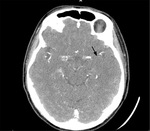
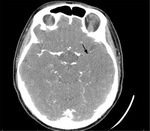
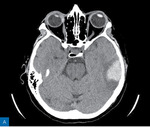
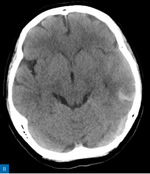
Kobieta w wieku 49 lat, dotychczas obciążona wyłącznie nikotynizmem, została przyjęta na rejonowy oddział neurologii z powodu nagłego niedowładu połowiczego prawostronnego i zaburzeń mowy od godzin porannych; w skali NIHSS uzyskała 18 pkt. W badaniu angio-TK stwierdzono niedrożność lewej tętnicy środkowej mózgu w odcinkach M1 i M2 (ryc. 1), a po wykluczeniu przeciwwskazań bezwzględnych podano leczenie trombolityczne i przetransportowano pacjentkę do centrum interwencyjnego leczenia udaru mózgu (CILUM) w celu wykonania MT. Podczas transportu do CILUM zarejestrowano poprawę w zakresie niedowładu – NIHSS 6 pkt. Z uwagi na spełnienie kryteriów (niedrożność dużego naczynia w zasięgu trombektomu, okno terapeutyczne <6 h, NIHSS >6 pkt) przeprowadzono zabieg MT, uzyskując efekt terapeutyczny oceniony w zmodyfikowanej skali leczenia w niedokrwieniu mózgu (mTICI – modified treatment in cerebral ischemia) na 2c (całkowita rekanalizacja, ale wolniejsze wypełnianie naczynia środkiem kontrastowym) oraz zmniejszenie zaburzeń mowy (NIHSS 4 pkt). W wykonanej kontrolnej TK mózgu po 24 godzinach stwierdzono hipodensyjną strefę w strukturach głębokich lewej półkuli mózgu. W prewencji wtórnej włączono ASA w dawce 150 mg/24 h oraz atorwastatynę 80 mg/24 h.
Podczas hospitalizacji obserwowano dalszą poprawę stanu neurologicznego oraz ustępowanie zaburzeń mowy i niedowładu kończyn. W toku wykonanej diagnostyki nie wykazano obecności zmian miażdżycowych, migotania przedsionków ani nadciśnienia tętniczego. W badaniu echokardiografii przezprzełykowej stwierdzono obecność przetrwałego otworu owalnego (PFO – patent foramen ovale) z przeciekiem prawo-lewym, nie odnotowano cech zakrzepicy żył głębokich. Zlecono wykonanie panelu badań w kierunku trombofilii, a po konsultacji z kardiologiem interwencyjnym zakwalifikowano chorą do zabiegu zamknięcia PFO w trybie planowym.
Przypadek 3 – udar żylny
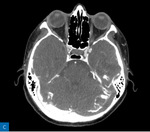
Rycina 2. A. Podostry krwiak śródmózgowy w lewym płacie skroniowym (TK w fazie natywnej). B. Hiperdensyjna lewa zatoka poprzeczna (TK w fazie natywnej). C. W angiografii TK w fazie żylnej uwidoczniono skrzeplinę wypełniającą światło zatoki poprzecznej po stronie lewej (opis dr n. med. Emilia Frankowska, Klinika Neurologiczna, Wojskowy Instytut Medyczny – Państwowy Instytut Badawczy w Warszawie)
Chora, lat 38, nielecząca się przewlekle, została skierowana na SOR z powodu podostrego, narastającego od 2 tygodni bólu głowy. Dwa dni wcześniej dołączyły się nudności oraz zaburzenia ostrości widzenia, a kilka godzin przed wezwaniem zespołu ratownictwa medycznego (ZRM) wystąpił niedowład prawej kończyny górnej. Przy przyjęciu na SOR ciśnienie tętnicze wynosiło 130/85 mmHg, przedmiotowo stwierdzono zespół piramidowy obustronny oraz średniego stopnia izolowany niedowład prawej kończyny górnej (NIHSS 2 pkt). W wywiadzie przewlekła antykoncepcja hormonalna, nikotynizm (10 paczkolat), brak obciążeń rodzinnych w kierunku trombofilii oraz zakrzepicy żylnej. W badaniach obrazowych stwierdzono zakrzepicę zatoki poprzecznej lewej powikłaną krwiakiem śródmózgowym w lewym płacie skroniowym (ryc. 2). Do leczenia włączono enoksaparynę w dawce terapeutycznej (1 mg/kg 2 ×/24 h), uzyskując stopniową poprawę stanu neurologicznego. W badaniach dodatkowych nie stwierdzono zaburzeń krzepnięcia oraz infekcji.
Po 10 dniach do leczenia włączono bezpośredni doustny inhibitor krzepnięcia (apiksaban) w dawce terapeutycznej 5 mg 2 ×/24 h, zalecono kontrolę czynników ryzyka zakrzepicy (niestosowanie antykoncepcji hormonalnej oraz zakaz palenia papierosów). W kontrolnym badaniu MR wykonanym ambulatoryjnie po 6 miesiącach stwierdzono pełną rekanalizację zatoki i z uwagi na wyeliminowanie czynników ryzyka zakrzepicy przez chorą podjęto decyzję o odstawieniu apiksabanu.