III Kongres Akademii po Dyplomie Okulistyka już w ten piątek! Kup bilet i dołącz do ekspertów podczas Siatkówka Meeting! Sprawdź >
Neuroinfekcje
Opryszczkowe zapalenie mózgu – trudności diagnostyczne
Joanna M. Zajkowska,1 Andrzej Ustymowicz,2 Maciej Kondrusik1
Wprowadzenie
Mimo ogromnego postępu w badaniach nad zakażeniami wirusem Herpes simplex typu 1 (HSV-1) i 2 (HSV-2), pozostają one ważnym problemem klinicznym, zależnym od biologicznych właściwości wirusa, takich jak neuroinwazyjność, neurotoksyczność i latencja, a także z powodu powszechnego występowania wirusa w populacji.
Zakażenie wirusem opryszczki zwykłej przybiera wiele postaci klinicznych – od bezobjawowych, przez zakażenia śluzówkowo-skórne i zapalenia rogówki, do najcięższych, obarczonych dużą śmiertelnością zapaleń ośrodkowego układu nerwowego (OUN) (tab. 1). W ostatnich latach wyniki niektórych badań sugerowały również znaczący udział zakażeń HSV-1 w patogenezie choroby Alzheimera.
W przypadku podejrzenia zapalenia mózgu istnieje skuteczna terapia. Stosowany z wyboru acyklowir jest znakomitym lekiem, który jest aktywowany jedynie w zakażonych komórkach, powstrzymując proces replikacji wirusa. Obecnie przy podejrzeniu klinicznym zakażenia wczesna diagnostyka opiera się na wykryciu materiału DNA metodą PCR, które zwykle uzupełniane jest badaniem neuroobrazowym.
Epidemiologia
Wirus opryszczki zwykłej (Herpes simplex virus, HSV) jest szeroko rozpowszechniony w populacji ogólnej, a jego naturalnym rezerwuarem jest jedynie człowiek. Wirus rozprzestrzenia się tylko przez kontakt bezpośredni przez zakażone wydzieliny. Chorują osoby w każdym wieku, jednak 1/3 stanowią dzieci i młodzi dorośli. W krajach słabo rozwiniętych pierwotna infekcja HSV-1z serokonwersją ma miejsce w pierwszych dwóch dekadach życia. W krajach rozwiniętych połowa serokonwersji przypada na wiek 20-40 lat. W świecie średnio 80-90% osób jest seropozytywnych. Do zachorowania na opryszczkowe zapalenie mózgu (Herpes simplex encephalitis, HSE) dochodzi stosunkowo rzadko, a częstość jego występowania ocenia się na 1-3 przypadki na milion, jednak jest najczęstszą przyczyną sporadycznego, śmiertelnego zapalenia mózgu. U nieleczonych śmiertelność może sięgać 60-70%, a u leczonych 11-30%. Zakażenie charakteryzuje również duży odsetek poważnych następstw neurologicznych. Zachorowania nie mają związku z porą roku ani płcią. Obserwuje się dwa szczyty zachorowań – poniżej 20i powyżej 50 roku życia.
Wirus HSV
Wyróżnia się dwa typy wirusa opryszczki – 1 i 2. Oba typy HSV należą do rodziny Herpetiviridae. Poza wirusami HSV-1 i HSV-2 należą do niej wirusy cytomegalii (CMV), półpaśca (VZV), mononukleozy (EBV), ludzki herpeswirus typu 6 (HHV-6), ludzki herpeswirus typu 7 (HHV-7) i małpi herpeswirus typu B (HBLV). Wszystkie z wymienionych wirusów mają zdolność do latencji i reaktywacji. Wirusy HSV-1 i HSV-2 należą do podrodziny alfa, charakteryzują się krótkim czasem replikacji z powodu szybkiej destrukcji komórki gospodarza i zdolne są do przejścia w fazę latencji, zazwyczaj w zwojach czuciowych. Wirus HSV składa się podwójnej helisy DNA 125-240 kb (materiał genetyczny kodujący 100-200 białek), otoczonej ikosaedralnym kapsydem i lipidową otoczką. Przestrzeń między kapsydem a lipidową warstwą, zwana tegumentem, zawiera białka, które mogą odgrywać rolę w transporcie wirusa. Sekwencja genomu HSV-1 i HSV-2 i biologiczne właściwości wirusów są podobne (70% homologii genomu).
Klinicznie choroby, u podłoża których leżą zakażenia HSV-1 i HSV-2, są nie do odróżnienia. Uważa się, że HSV-1 daje objawy w obrębie górnej połowy ciała, a HSV-2 w obrębie dolnej połowy. HSV-1 odpowiada za 90% przypadków HSE. Niemniej głównym czynnikiem opryszczki narządów płciowych (herpes genitalis) w krajach o niskim statusie socjoekonomicznym, a często także w Stanach Zjednoczonych i Anglii, jest HSV-1. HSV-2 może być również czynnikiem opryszczki wargowej (herpes labialis). Oba typy mogą być przyczyną zakażenia OUN. Typ 1 wywołuje najczęściej zapalenie mózgu u dorosłych i u starszych dzieci, natomiast typ 2 – przeważnie łagodnie przebiegające limfocytarne zapalenie opon mózgowo-rdzeniowych, rzadziej rdzenia kręgowego i zapalenie korzeni nerwowych. U noworodków może spowodować ostre krwotoczno-martwicze zapalenie mózgu o charakterze rozlanym. Tzw. aseptyczne zapalenie opon mózgowo-rdzeniowych wywołane przez wirusy opryszczki ma charakter łagodny, ustępuje samoistnie i wymaga jedynie leczenia objawowego. W przypadkach zakażenia OUN dorosłych wydaje się, że postać kliniczna może zależeć od sposobu rozprzestrzeniania się wirusa. Droga krwionośna, związana z zakażeniem HSV-2, powoduje zapalenie opon mózgowo-rdzeniowych, a drogą neurogenną, związaną z zakażeniem HSV-1 dochodzi do zapalenia mózgu. Przebieg opryszczkowego zakażenia OUN (łagodny lub prowadzący do nieodwracalnych uszkodzeń i śmierci) może zależeć od: miejsca wniknięcia wirusów, miejsca ich replikacji, miejsca pierwotnego zakażenia oraz właściwości neurowirulentnych wirusa. Rola układu immunologicznego w przebiegu zakażenia jest wciąż badana.
Zakażenie i patogeneza (latencja i reaktywacja)
Pierwotne zakażenia są zwykle bezobjawowe, pochodzą z powierzchni śluzówkowych jamy ustnej nosa, spojówek i układu płciowego. Do zakażenia dochodzi przez bezpośredni kontakt zakażonych śluzówek lub przez zakażone wydzieliny. Nieuszkodzona skóra z warstwą keratynocytów stanowi przeszkodę dla wirusów. W wydzielinach ok. 0,65-15% dorosłych stale występuje HSV-1 lub HSV-2. Do nawrotów zakażenia wirusem opryszki w okolicy ust i warg dochodzi u 20-40% populacji. Rzadszą postacią jest nawracające opryszczkowe zapalenie rogówki.
Po wniknięciu do skóry HSV namnaża się miejscowo w komórkach przypodstawnych i pośrednich, powodując ich lizę w ciągu 24-48 godzin i jednocześnie wzbudzając lokalną odpowiedź zapalną. Wirus uwalniany jest z zakażanych komórek, a nowe cząsteczki wirusa zakażają sąsiednie komórki. W zakażonym miejscu powstaje cienkościenny pęcherzyk na zapalnej podstawie. W tym czasie może pojawić się odczyn węzłowy. Dalsza replikacja jest skutkiem wiremii i rozsiewu trzewnego, zależnego od stanu odporności zakażonego ustroju. Czy wirus pozostanie lokalnie czy ulegnie rozprzestrzenieniu zależy m.in. od mechanizmów obronnych, takich jak produkowany interferon, cytotoksyczność komórkowa naturalna (komórki NK) i zależna od przeciwciał (antibody dependent cell cytotoxity, ADCC) (komórki limfoidalne K), krążące przeciwciała. Wiremia umożliwia rozprzestrzenienie się wirusów do innych narządów, takich jak wątroba, płuca i ośrodkowy układ nerwowy.
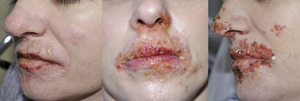
Na pewnym etapie zakażenia wirusy wnikają w zakończenia nerwów i wstecznie przedostają się do komórki nerwowej w zwojach grzbietowych (dorsal root ganglia, DRG), gdzie pozostają do końca życia w postaci latentnej. Skutkiem zakażenia błony śluzowej jamy ustnej jest zakażenie nerwu trójdzielnego, czasem zwoje szyjne. Zakażenia narządów płciowych przebiegają z zajęciem zwojów krzyżowych. W badaniach autopsyjnych obecność latentnego HSV-1 stwierdzano w zwojach nerwu trójdzielnego w 55% przypadków, a HSV-2 w zwojach krzyżowych w 20%. W zakażonych latentnie komórkach nerwowych wirus jest obecny w postaci episom wewnątrz jądra, które nie produkują białek wirusa i nowych cząsteczek wirusa. Pozostając w fazie latencji, wirus nie uszkadza komórki. Dopiero reaktywacja, która przebiega z powstawaniem nowych cząsteczek wirusa przemieszczających się wzdłuż aksonu, powoduje kliniczne objawy choroby. Zakażenia nawracające w większości spowodowane są endogenną reaktywacją wirusa, której nie zapobiegają przeciwciała, znacznie rzadziej – egzogenną reinfekcją. Tak się dzieje w nawrotach opryszczki warg i okolicy ust (herpes labialis), którym sprzyjają nasłonecznienie, gorączka, lokalne urazy, zabiegi chirurgiczne w okolicy nerwu trójdzielnego (w tym zabiegi stomatologiczne, chirurgiczne, zabiegi z zastosowaniem lasera), menstruacje i stres, immunosupresja (w tym leczenie biologiczne), a także inne ciężkie zakażenia bakteryjne (ryc. 1).
U osób immunokompetentnych do reaktywacji dochodzi zwykle w granicach anatomicznego unerwienia i sąsiedztwie jednego zwoju grzbietowego i o ile pierwotna infekcja ma miejsce w 1-4 dekadzie życia, reaktywacja może nastąpić w każdym momencie.
Mechanizmy odpowiadające za wnikanie, latencję i reaktywacje są nadal badane, m.in. granzym B wydzielany przez komórki CD8+, który degraduje białko ICP-4 wirusa niezbędne do jego reaktywacji, utrzymując go w latencji. Ponadto badana jest rola ograniczonej transkrypcji wiązanej z obecnością RNA (latency-associated transcripts, LAT).