Krioterapia jest stosowana w okulistyce przede wszystkim w leczeniu zmian skóry powiek, takich jak kępki żółte, trichiasis, distichiasis, dermatofibroma, rak podstawnokomórkowy, prosaki (milia), torbiel śluzowata, rogowacenie słoneczne, rogowacenie łojotokowe, rogowacenie starcze, mięczak zakaźny, brodawki zwykłe, brodawki nitkowate, torbiele, rogowiaki kolczystokomórkowe. Znajduje również zastosowanie w leczeniu jaskry (zabiegi cyklodestrukcyjne). Opisano też przypadki użycia krioterapii w leczeniu amyloidozy spojówek, skrzydlika, keratopatii taśmowatej, górnego rąbkowego zapalenia rogówki i spojówki, wiosennego zapalenia rogówki i spojówek14.
Elektrochirurgia
Procedury elektrochirurgiczne są grupą zabiegów, w których do zniszczenia tkanek wykorzystuje się prąd elektryczny. Opracowanie pierwszego komercyjnego urządzenia elektrochirurgicznego przypisuje się Williamowi T. Boviemu, który wykonał pierwszy aparat elektrochirurgiczny podczas pracy na Uniwersytecie Harvarda. Pierwsze użycie generatora elektrochirurgicznego w sali operacyjnej nastąpiło w październiku 1926 r. w Peter Bent Brigham Hospital w Bostonie, a pierwszą operację z użyciem tego urządzenia – usunięcie guza z głowy pacjenta – wykonał Harvey Cushing. Ze względu na bezpieczeństwo, prostotę wykonania i czynniki ekonomiczne urządzenia elektrochirurgiczne są powszechnie stosowane do leczenia łagodnych i niektórych złośliwych schorzeń. W przypadku nowotworów dobre wyniki leczenia uwarunkowane są odpowiednią kwalifikacją chorych. Elektrochirurgia polega na wykorzystaniu energii elektrycznej do termicznego zniszczenia tkanki, najczęściej w postaci dehydratacji – odwodnienia tkanki, koagulacji lub odparowania15. Zabiegi elektrochirurgiczne można podzielić na różne typy ze względu na mechanizm uszkodzenia tkanek i są to:
- koblacja, w której prąd zmienny o wysokiej częstotliwości jonizuje ośrodek przewodzący prąd elektryczny przekazujący ciepło, powodując powierzchowne uszkodzenia naskórka i częściowo skóry właściwej, przy minimalnym zniszczeniu tkanki pobocznej; metoda służy do odmładzania twarzy
- elektrokauteryzacja, w której prąd stały lub zmienny o wysokiej częstotliwości rozgrzewa element, tj. elektrodę, powodując uraz termiczny; w przeciwieństwie do elektrochirurgii wysokiej częstotliwości elektroda w elektrokoagulacji jest gorąca, ta metoda nie jest właściwą techniką elektrochirurgiczną, gdyż nie dochodzi w niej do przepływu prądu elektrycznego przez ciało chorego, dlatego może być wykorzystana u osób ze stymulatorem serca
- elektrochirurgia wysokiej częstotliwości, w której oporność tkanki na przepływ prądu zmiennego o wysokiej częstotliwości przekształca energię elektryczną w ciepło, powodując termiczne uszkodzenie tkanki; wytwarzanie ciepła następuje w tkance, podczas gdy elektroda zabiegowa pozostaje zimna; ta metoda, w zależności od stopnia destrukcji tkanek, obejmuje elektrodesykację, elektrofulgurację, elektrokoagulację i elektrosekcję.
Elektrodesykacja i elektrofulguracja są metodami wywołującymi najbardziej powierzchowną destrukcję tkanek. Przy elektrodesykacji dochodzi do kontaktu elektrody i tkanki, a efekt destrukcji osiągany jest przez iskrę elektryczną15,16.
Koagulacja elektryczna (elektrokoagulacja) powoduje głębszą, w porównaniu z elektrodesykacją i elektrofulguracją, destrukcję tkanek (szczególnie naczyń krwionośnych). Jest powszechnie stosowana jako narzędzie hemostatyczne małych naczyń (<1 mm) podczas zabiegów chirurgicznych. Jest również często wykorzystywana w celu usuwania niewielkich zmian naczyniowych (naczyniaki starcze, ziarniniaki naczyniowe). Cięcie elektryczne (elektrosekcja) zapewnia separację tkanek przy użyciu prądu elektrycznego o wysokim natężeniu i niskim napięciu. Czyste cięcie prądem stałym nie zapewnia hemostazy, dlatego większość urządzeń wykorzystuje prąd tnący (stały) i koagulacyjny (zmienny). Elektrosekcja powoduje minimalne termiczne uszkodzenie tkanek, dlatego brzegi rany mogą być zszyte. Najczęściej używa się elektrod w kształcie ostrza, pętli lub igły15,16.
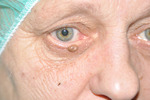
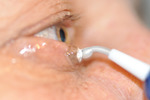
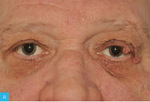
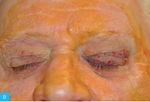
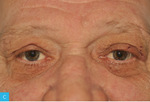
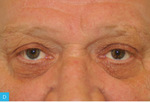
Rycina 8A-D. Usunięcie zmian łagodnych powiek górnych metodą elektrochirurgiczną. A. Pacjent przed zabiegiem. B. Bezpośrednio po zabiegu. C. 7 dni po zabiegu. D. 14 dni po zabiegu
Zabiegi elektrochirurgiczne ze względu na małą inwazyjność, łatwość wykonania, dużą dostępność, bezpieczeństwo oraz korzystne czynniki ekonomiczne znalazły szerokie zastosowanie w medycynie, a aparaty elektrochirurgiczne stanowią podstawowe wyposażenie sal operacyjnych i większości gabinetów ambulatoryjnych. Wskazania do zabiegów z ich użyciem obejmują łagodne i złośliwe choroby skóry (tab. 2). Niewiele jest natomiast przeciwwskazań do tych zabiegów. Do najważniejszych należą: wszczepiony stymulator serca, skaza krwotoczna, choroby sprzyjające zaburzeniom gojenia (przewlekła niewydolność żylna, cukrzyca), skrajne wyniszczenie. Mimo że procedury elektrochirurgiczne nie powinny wpływać na pracę nowoczesnych stymulatorów serca, należy zachować daleko idącą ostrożność w tych przypadkach. Większość tych zabiegów wykonuje się w znieczuleniu miejscowym, uzyskanym za pomocą iniekcji roztworu anestetyku lub jego miejscowego zastosowania (krem, żel). Część zabiegów można wykonać bez znieczulenia. Większość chorych dobrze toleruje krótkotrwałe dolegliwości bólowe związane z usuwaniem niewielkich, pojedynczych zmian (brodawczaki, włókniaki czy naczyniaki) (ryc. 8A-D). Elektrochirurgia cechuje się wysokim profilem bezpieczeństwa. Prawidłowe stosowanie instrumentów niezwykle rzadko prowadzi do powikłań, które w większości przypadków są stosunkowo łagodne15,16.
Epilacja
Epilacja jest metodą trwałego usuwania pojedynczych włosów, takich jak rzęsy o nieprawidłowym kierunku wzrostu. Podstawową i najprostszą metodę stanowi elektrokoagulacja. Polega na zniszczeniu cebulki włosa prądem elektrycznym. Trichiasis, czyli nieprawidłowy wzrost rzęs, może być wrodzony lub nabyty, np. na skutek urazu, zakażenia, w przebiegu zespołu Stevensa-Johnsona, chorób przewlekłych, alergii, stosowanych leków, a nawet w wyniku procesu starzenia. Prawdziwy trichiasis jest stanem nabytym, w którym wzrost pojedynczej rzęsy (lub kilku) skierowany jest niewłaściwie – ku tyłowi, w kierunku spojówki lub rogówki. Może to powodować poważne problemy, od zadrażnienia aż do otarć lub owrzodzeń rogówki.
Pojedyncze włosy najdogodniej usuwa się pęsetą, a jeżeli pojawią się ponownie, wykorzystuje się ablację. Uważa się, że opuszka mieszka włosowego rzęsy znajduje się w odległości 2,4 mm od powierzchni brzegu powieki górnej oraz 1,4 mm powieki dolnej. Do epilacji używa się specjalnie przeznaczonych do tego zaizolowanych cienkich elektrod igłowych lub giętkich. Podczas zabiegu należy pamiętać, aby nie wprowadzać igły zbyt głęboko i nie stosować zbyt wysokich mocy, co może doprowadzić do niepożądanego bliznowacenia. W trakcie zabiegu należy delikatnie naciągnąć łodygę włosa, która wskazuje bezpośrednio na mieszek włosowy. Giętką elektrodę (najlepiej) przeznaczoną do epilacji wprowadza się wzdłuż przebiegu włosa. Końcówki sztywne, niedostosowujące się do przebiegu włosa mogą nie dochodzić do korzenia. Niepełna elektroliza może zniekształcić mieszek włosowy i odseparować go od linii właściwego wzrostu, co spowoduje wrastanie włosa17.
Toksyna botulinowa
Toksyna botulinowa (TB) w przyrodzie występuje w postaci siedmiu serotypów oznaczanych literami A-G. Obecnie na świecie komercyjnie dostępne są dwa serotypy neurotoksyny botulinowej: A i B (BTX-A i BTX-B). W Polsce dostępne są oba serotypy w różnych preparatach. Zastosowanie BTX-B jest jednak bardzo ograniczone, ponieważ został on zarejestrowany tylko w jednym wskazaniu (kręczu karku) i zarezerwowany dla chorych, którzy wytworzyli przeciwciała przeciwko serotypowi A. Zarejestrowane w Polsce preparaty toksyny botulinowej zawierają odpowiedni serotyp neurotoksyny botulinowej i tzw. substancje wspomagające (białka nietoksyczne). Czysta neurotoksyna botulinowa zbudowana jest z dwóch łańcuchów polipeptydowych: lekkiego (50 kDa) i ciężkiego (100 kDa), połączonych mostkami dwusiarczkowymi, których stabilność warunkuje efekt działania TB. W zależności od preparatu BTX-A pochodzi z odmiennego szczepu bakterii Clostridium botulinum, co spowodowało rozróżnienie 4 podtypów – A1-A4. Po podaniu do docelowej tkanki TB wiąże się z glikoproteinami zlokalizowanymi na cholinergicznych zakończeniach nerwowych, BTX-A z białkiem SV2C, BTX-B z synaptotagminą, dzięki czemu dostaje się do wnętrza komórki nerwowej. Wewnątrzkomórkowo lekki łańcuch rozszczepia białka odpowiedzialne za transport i sekrecję pęcherzyków z acetylocholiną do przestrzeni synaptycznej (SNARE proteins). Tak zablokowane synapsy w procesie regeneracji zostają zastąpione przez nowe zakończenia (zjawisko znane jako sprouting), z czym związane jest czasowe i wyczerpujące się zwykle po 12 tygodniach działanie TB. W zależności od docelowej tkanki TB blokuje przekazywanie cholinergiczne impulsu zarówno w płytce motorycznej mięśni szkieletowych, jak i we włóknach autonomicznych unerwiających gruczoły potowe, łzowe, ślinowe lub mięśnie gładkie. Działanie TB w mięśniu szkieletowym można wykryć po 2 dniach od iniekcji, maksymalny efekt osiąga się po dwóch tygodniach; stopniowo zmniejsza się on po 2,5 miesiąca. W tkance gruczołowej działanie TB może utrzymywać się 6-9 miesięcy. Dawniej uznawano, że blok nerwowo-mięśniowy wywołany przez TB jest nieodwracalny, obecnie wiemy jednak, że po zaprzestaniu leczenia po pewnym czasie dochodzi do odtworzenia fizjologicznej funkcji zablokowanej płytki nerwowo-mięśniowej18.
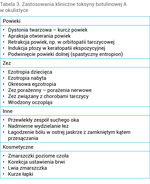
Odkąd w latach 70. ubiegłego stulecia toksyna botulinowa została po raz pierwszy wykorzystana w leczeniu zeza przez amerykańskiego okulistę Allana B. Scotta, stała się przełomem w leczeniu schorzeń przebiegających z nadmiernymi skurczami mięśni, takich jak kurcz powiek, połowiczy kurcz twarzy czy kręcz karku. Lista wskazań do jej zastosowania w okulistyce stale się rozszerza i obejmuje również choroby niezwiązane z nadaktywnością mięśni, takie jak nadmierne łzawienie, przewlekły zespół suchego oka czy kosmetyczna redukcja zmarszczek okolicy okołooczodołowej (tab. 3)19.
Spośród schorzeń okulistycznych obecnie toksyna botulinowa najczęściej stosowana jest w leczeniu kurczu powiek, tzw. blefarospazmu. Jest to ogniskowa dystonia charakteryzująca się nawracającymi mimowolnymi skurczami mięśnia okrężnego oka, prowadzącymi do częstego mrugania lub silnego zaciskania powiek18. Choroba często zaczyna się uczuciem pieczenia oczu, piasku pod powiekami, nadmiernym łzawieniem, częstszym mruganiem, światłowstrętem, które powoli postępuje, prowadząc nierzadko do funkcjonalnej ślepoty. Może zacząć się jednostronnie. Częstość występowania szacuje się na 1,6-13,3/100 000 osób. U kobiet występuje ok. dwukrotnie częściej19. Średni wiek zachorowania to 55,7 roku. U ponad 1/3 chorych kurcz powiek ulega progresji do dystonii segmentalnej z zajęciem także mięśni dolnej części twarzy (zespół Meige’a). Tylko u 20% chorych występuje izolowane zaciskanie powiek, a u 80% dodatkowe skurcze innych mięśni twarzy (w tym mięśni krtani i szyi). Ma to istotne znaczenie przy planowaniu leczenia TB18. Kurcz powiek z reguły jest samoistny i sporadyczny. Występowanie rodzinne (ok. 10%) dotyczy zwykle pacjentów, u których kurcz powiek jest składową dystonii segmentalnej lub uogólnionej. Bardzo rzadko może mieć charakter objawowy (wskazane neuroobrazowanie). Blefarospazm może wystąpić również w trakcie przyjmowania niektórych leków (np. neuroleptyków, leków przeciwhistaminowych) lub w przebiegu chorób neurozwyrodnieniowych (np. choroby Parkinsona, postępującego porażenia nadjądrowego, choroby Huntingtona, choroby Wilsona, neuroakantocytozy).
Food and Drug Administration (FDA) już w 1989 r. zarejestrowała preparat Botox w leczeniu kurczu powiek. Znajomość anatomii mięśni twarzy jest kluczowa w leczeniu TB chorych z blefarospazmem. Mięsień okrężny oka jest podstawowym mięśniem powodującym kurcz powiek, zarówno jego część dystalna, jak i proksymalna (przedtarczkowa). Najczęściej TB wstrzykuje się w przyśrodkową i boczną część przedtarczkowej części mięśnia okrężnego oka, zarówno w powiekach górnych, jak i dolnych, ale często także w przedprzegrodową część włókien mięśnia okrężnego oka oraz mięśnie – podłużny, czołowy i marszczący brwi. Iniekcja w część przedtarczkową mięśnia okrężnego jest bardziej bolesna dla pacjenta, ale skuteczniejsza (dłuższy i lepszy efekt przy mniejszych dawkach leku) i powoduje mniej powikłań. Korzyści z leczenia utrzymują się średnio do 13 tygodni18,19. W przypadku niewystarczającej odpowiedzi na TB warto rozważyć większe dawki leku, zanim skierujemy chorego np. na leczenie operacyjne. W przypadkach gdy TBX-A staje się nieskuteczna, można zastosować toksynę botulinową typu B, stosując od 750 do 2500 jednostek na oko. Ma ona jednak krótszy czas działania (8-10 tygodni) i wykazuje większą tendencję do dyfuzji do otaczających tkanek oraz rozprzestrzeniania się na sąsiednie obszary z towarzyszącymi działaniami niepożądanymi i powoduje większy ból przy wstrzyknięciu19.
Najczęstszym powikłaniem leczenia kurczu powiek za pomocą TB jest opadanie powiek (4-18%). Wskaźnik opadania powiek wzrasta do 74% wraz ze wzrostem liczby (>10 wstrzyknięć) i z podaną dawką pojedynczej iniekcji TB. Aby zmniejszyć ryzyko wystąpienia tego powikłania, należy unikać podawania leku w środkowej części powieki górnej. Częstość pozostałych działań niepożądanych mieści się w granicach 2% i są to: podwójne widzenie, zamazane widzenie, suchość spojówek, łzawienie, odwinięcie dolnej powieki, osłabienie mięśni dolnej części twarzy.