IV edycja Kongresu HPV już 12-13 czerwca! Poznaj najnowsze trendy w profilaktyce, diagnostyce i leczeniu raka szyjki macicy i innych schorzeń związanych z HPV | Sprawdź >
Autofluorescencja dna oka jest techniką obrazowania wykorzystującą naturalne właściwości fluorescencyjne tkanek. Głównym źródłem FAF w siatkówce jest lipofuscyna – substancja gromadząca się w komórkach RPE. W zdrowym oku poziom autofluorescencji odzwierciedla równowagę między produkcją a usuwaniem lipofuscyny w RPE. Nadmiar lub niedobór FAF wskazuje na patologiczne zmiany w nabłonku barwnikowym. Obszary hiper- i hipofluorescencyjne często tworzą charakterystyczne wzory, które mogą być szczególnie widoczne w przypadku chorób typu CSCR (ryc. 4).
Angiografia fluoresceinowa
Angiografia fluoresceinowa pozwala na identyfikację wielu postaci zmian na poziomie RPE i siatkówki neurosensorycznej, a co ważniejsze, umożliwia ich dokładną lokalizację, której znajomość jest niezbędna w przypadku ewentualnej fotokoagulacji. Do najczęstszych typów patologicznej fluorescencji obserwowanych w CSCR należą:
- ubytki okienkowe odpowiadające uszkodzeniom RPE
- nasilająca się w czasie hiperfluorescencja o stałych, wyraźnych granicach, zaznaczająca się w miejscach PED
- hiperfluorescencja związana z aktywnym przeciekiem przez uszkodzony RPE.
Przeciek może mieć charakter:
- plamy atramentowej (kleksa) – jest to najczęstsza forma przecieku (nawet 80% przypadków) charakteryzująca się postępującą i równomierną ekspansją hiperfluorescencji, rozpoczynającą się od małego, okrągłego punktu przecieku
- wzoru dymu z komina/dymu papierosowego – jest to hiperfluorescencyjne pasmo unoszące się ku górze, z następczym bocznym rozproszeniem na górnej granicy surowiczego odwarstwienia siatkówki.
W ostrej postaci CSCR nawet 44% przypadków wykazuje wieloogniskowe punkty przecieku, z dominującą lokalizacją w okolicy dołka13. Obszar sPED uwidacznia się w pośrednich i późnych fazach angiografii jako delikatna hiperfluorescencja wynikająca z tzw. efektu poolingu, czyli gromadzenia się barwnika w ograniczonej przestrzeni płynowej. Dodatkowym wykorzystaniem FA jest ocena pod kątem obecności zmian wtórnych o typie ukrytej CNV. Wspomniane wcześniejsze zmiany RPE o charakterze FIPED mogą zawierać składową naczyniową, której uwidocznienie wpływa na późniejsze postępowanie terapeutyczne.
Angiografia indocyjaninowa
Użycie w technice angiografii zieleni indocyjaninowej zamiast fluoresceiny pozwala na lepsze uwidocznienie krążenia naczyniówkowego. Indocyjanina dzięki swemu większemu powinowactwu do białek osocza pozostaje w naczyniach naczyniówki, co umożliwia ich pełną wizualizację. Wykorzystanie ICGA jest w założeniu uzupełnieniem diagnostyki angiograficznej siatkówki i naczyniówki – ta technika jest niezastąpiona w przypadku wątpliwości diagnostycznych związanych z różnego rodzaju makulopatiami wysiękowymi, w których FA, OCT i FAF nie wystarczają do postawienia ostatecznego rozpoznania. W angiografii indocyjaninowej CSCR wykazuje zwiększoną przepuszczalność naczyń oraz wyraźne zwiększenie średnicy naczyń żylnych, które są widoczne w miejscach aktywności choroby i często można prześledzić ich poszerzoną strukturę wzdłuż ich przebiegu do ujścia w bańkach żył wirowatych – ich asymetryczność jest również jedną z cech CSCR w ICGA14,15. Warto dodać, że angiografia indocyjaninowa jest niezbędna do przeprowadzenia terapii fotodynamicznej uważanej za najskuteczniejszą metodę leczenia CSCR.
Przypadek 1
Mężczyzna, lat 48, w wywiadzie zgłosił pogorszenie VA, ubytki w polu widzenia, które utrzymują się od kilkunastu lat z okresowymi epizodami zaostrzeń. Ogólnie nie choruje, nie przyjmuje leków na stałe. Do tej pory nie był leczony okulistycznie. Parametry widzenia – BCVA oka lewego 0,6 na tablicach Snellena. W badaniu przedmiotowym odcinka przedniego nie stwierdzono odchyleń. W ramach diagnostyki multimodalnej wykonano zdjęcia barwne dna, FAF, ICGA oraz OCT obojga oczu (ryc. 5-9).
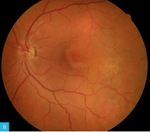
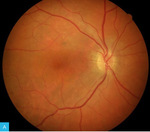
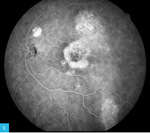
Rycina 5A, B. Zdjęcie barwne bieguna tylnego obojga oczu. Zwracają uwagę obszary depigmentacji, które są najbardziej wyraźne wokół tarczy nerwu wzrokowego i wzdłuż arkad skroniowych w oku prawym. Natomiast w oku lewym zmiany przyjmują pierścieniowaty kształt okalający dołeczek oraz plamisty w skroniowej i górnej części plamki. W plamce oka prawego ponadto między dołeczkiem a arkadą skroniową górną zaznacza się pojedynczy obszar hiperplazji nabłonka barwnikowego
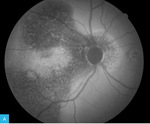
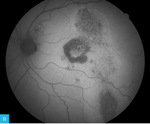
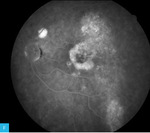
Rycina 6A, B. Autofluorescencja dna obojga oczu. Badanie to najlepiej ukazuje uszkodzenia i atrofię nabłonka barwnikowego
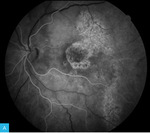
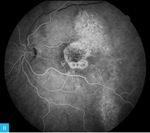
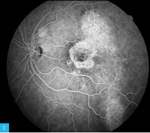
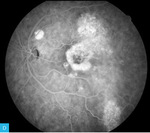
Rycina 7A-F. Angiografia fluoresceinowa dna oka lewego. Obrazy w górnym rzędzie przedstawiają angiogram od fazy tętniczej przez fazę tętniczo-żylną do fazy żylnej
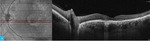
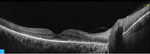
Rycina 8A, B. Optyczna koherentna tomografia siatkówki oka lewego – dwa wybrane skany B reprezentujące wzorzec skanowania typu raster
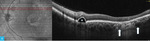
Rycina 9A, B. Zdjęcia angiografii fluoresceinowej oraz centralny skan horyzontalny plamki oka prawego
Na zdjęciu barwnym bieguna tylnego obojga oczu (ryc. 5) zwracają uwagę obszary depigmentacji, które są najbardziej wyraźne wokół tarczy nerwu wzrokowego i wzdłuż arkad skroniowych w oku prawym. Natomiast w oku lewym zmiany przyjmują pierścieniowaty kształt okalający dołeczek oraz plamisty w skroniowej i górnej części plamki. Poza tym w plamce oka prawego – między dołeczkiem a arkadą skroniową górną – zaznacza się pojedynczy obszar hiperplazji nabłonka barwnikowego.
Najlepiej uszkodzenia i atrofię nabłonka barwnikowego pokazuje FAF obojga oczu (ryc. 6). Zmiany zanikowe widoczne na zdjęciu barwnym prezentują się tu wyraźniej, zakreślając rzeczywistą mapę uszkodzeń. Obszary jednolitej hipoautofluorescencji odzwierciedlają atrofię RPE, natomiast miejsca wzmożonej autofluorescencji świadczą o zaburzeniach funkcji RPE (przeciążenie metaboliczne związane z nadmierną akumulacją lipofuscyny – głównego fluorofora odpowiedzialnego za efekt autofluorescencji) i/lub o obecności płynu w przestrzeni podsiatkówkowej. W oku zarówno prawym, jak i lewym zwracają uwagę obszary hipo- oraz hiperautofluorescencji w postaci wertykalnych pasm wykraczających poza dolne granice uzyskanych zdjęć. Reprezentują one przebyty lub aktualny rozkład płynu podsiatkówkowego, który wraz z upływem czasu grawitacyjnie przemieszcza się w kierunku dolnych, obwodowych sektorów siatkówki.
Obrazy na rycinie 7 (górny rząd) przedstawiają angiogram fazy od tętniczej przez tętniczo-żylną do żylnej. Widoczne w ICGA obszary hiperfluorescencji mają charakter ubytku okienkowego – od faz wczesnych, o stałych, niezmiennych granicach i wysokiej intensywności, która zmniejsza się na kolejnych etapach badania. Ubytki okienkowe korespondują z obszarami hipoautofluorescencji widocznymi na zdjęciach FAF (ryc. 6). Drugim rodzajem hiperfluorescencji uwidocznionym na powyższych angiogramach ryciny 7 (dolny rząd) jest obszar nasilającej się w czasie hiperfluorescencji o ostrych i stałych granicach, który reprezentuje PED o średnicy <1 DD nieco powyżej i skroniowo od górnego bieguna tarczy nerwu wzrokowego (zaznaczony białą gwiazdką na zdjęciu OCT na ryc. 8). W przypadku opisanego pacjenta nie zaobserwowano typowego dla aktywnego CSCR przecieku barwnika.