IV edycja Kongresu HPV już 12-13 czerwca! Poznaj najnowsze trendy w profilaktyce, diagnostyce i leczeniu raka szyjki macicy i innych schorzeń związanych z HPV | Sprawdź >
Erytrodermia oznacza uogólniony stan zapalny skóry, obejmujący ponad 90% powierzchni ciała, któremu w ciężkich przypadkach może towarzyszyć wyłysienie i utrata paznokci. Rozległa odpowiedź zapalna i wzrost przepływu krwi przez skórę prowadzą do zaburzeń podstawowej przemiany materii, równowagi wodno-elektrolitowej, utraty białka i hipoalbuminemii, enteropatii, niedokrwistości oraz hipotermii.
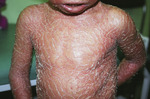
U dzieci najczęstszą przyczyną erytrodermii są leki, atopowe i łojotokowe zapalenie skóry (ryc. 8) oraz genodermatozy należące do zespołu dziecka kolodionowego (collodion baby).13 Jest to opisowe określenie schorzeń z grupy rybiej łuski, objawiających się pokrywającą po urodzeniu ciało dziecka błoniastą warstwą. Obraz dziecka kolodionowego obserwuje się w następujących jednostkach chorobowych: płód arlekin (ok. 50%), różne rodzaje rybiej łuski oraz w zespole Nethertona.
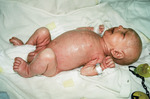
Rybia łuska sprzężona z płcią (ryc. 9) objawia się już w chwili urodzenia, obejmując skórę całego ciała. Mogą jej towarzyszyć m.in. zaburzenia narządu wzroku (ektropion, zapalenie rogówki, zaćma).14 U tych dzieci z powodu rozległej erytrodermii obserwuje się znacznego stopnia obniżenie frakcji gammaglobulin w proteinogramie, co zwykle nie skutkuje ciężkimi zakażeniami, ponieważ układ odporności tych pacjentów funkcjonuje prawidłowo mimo hipogammaglobulinemii spowodowanej utratą przez skórę.
Zespół Nethertona (ryc. 10) jest rzadką genetycznie uwarunkowaną dermatozą objawiającą się uogólnionym złuszczaniem i rumieniem, często występującym od urodzenia, krótkimi, suchymi i łamliwymi włosami oraz rzadkimi lub nieobecnymi brwiami i rzęsami, w badaniu mikroskopowym wykazującymi nieprawidłowości o charakterze trichorrhexis invaginata – włosy bambusowe – oraz pierwotnym niedoborem odporności wynikającym z zaburzenia dojrzewania limfocytów T i B.15
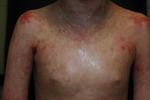
Rycina 11. Erytrodermia u chorego po przeszczepieniu macierzystych komórek krwi obwodowej z powodu SCID.
Wśród przyczyn erytrodermii w PNO wiodącym i alarmującym przykładem jest zespół Omenna (T+ B-NK+SCID) (ryc. 2). Należy on do grupy ciężkich złożonych niedoborów odporności (SCID) o zdecydowanie odmiennym, na tle reszty SCID, przebiegu klinicznym. Do objawów zespołu należą: uogólniona erytrodermia złuszczająca, limfadenopatia, hepatosplenomegalia, a obok hipogammaglobulinemii w zakresie IgG, IgA i IgM, zwiększone stężenie IgE i znaczna eozynofilia. Jest to następstwo oligoklonalnej proliferacji limfocytów Th2.16 Leczeniem zespołu Omenna jest możliwie jak najszybsze przeszczepienie macierzystych komórek krwi obwodowej od zgodnego dawcy. Zespół Omenna ze względu na przebieg kliniczny powinniśmy różnicować z chorobą przeszczep przeciw gospodarzowi (GvHD), która może wystąpić z różnym nasileniem po przeszczepieniu macierzystych komórek krwi obwodowej (ryc. 11), być uwarunkowana wcześniejszym przetoczeniem niefiltrowanych składników krwi dziecku z patologią układu odporności lub wyjątkowo rzadko występującym przekazaniem płodowi ze SCID matczynych limfocytów T przez łożysko (maternal-fetal engraftment).
Jak widać, nieswoistość obrazu klinicznego nie pozwala wnioskować o przyczynach erytrodermii. Erytrodermiczna skóra niemowlęcia z ciężkim AZS czy łojotokowym zapaleniem skóry będzie wyglądała łudząco podobnie do zmian skórnych obserwowanych w zespole Nethertona czy Omenna, dlatego też w diagnostyce niezbędne są wielokrotnie powtarzane badania histopatologiczne skóry, które w pierwotnych niedoborach odporności przebiegających z erytrodermią mają charakterystyczne cechy.
Szczepienia ochronne w pierwotnych niedoborach odporności
Szczepionki żywe
Szczepienia żywymi szczepionkami są przeciwwskazane w ciężkich wrodzonych niedoborach odporności. Do takich szczepionek należą: BCG, przeciwko ospie wietrznej, odrze, poliomyelitis, rotawirusom. Szczepienia mogą być wznowione wtedy, gdy w wyniku przeszczepienia szpiku nastąpi pełna rekonstytucja układu odporności. Pacjenci z niewielkimi izolowanymi wrodzonymi niedoborami mogą być szczepieni bez ograniczeń (tab. 1). Należy pamiętać, że decyzja o szczepieniach zapada indywidualnie i podejmuje ją lekarz specjalista immunolog.
Szczepionki inaktywowane
Inaktywowane szczepionki są w takim samym stopniu bezpieczne w stanach zaburzonej odporności, jak u osób z prawidłową odpornością. Skuteczność ich jest zróżnicowana w zależności od stopnia niedoborów odporności oraz rodzaju szczepionki. U dzieci z głębokimi niedoborami odporności są nieskuteczne.
Zaszczepienie trzema dawkami szczepionki przeciwko wzw typu B chroni przed zakażeniem nawet wtedy, gdy stężenie przeciwciał wynosi <10 j.m./l. Dotyczy to populacji dzieci zdrowych, u których nie ma wskazań do podania dodatkowej dawki szczepionki, gdyż brak lub małe stężenie przeciwciał w zdrowej populacji nie jest wynikiem braku odporności, ale braku ekspozycji na krążący wirus zapalenia wątroby typu B, który stymulowałby wytwarzanie przeciwciał. Jak dotąd w Polsce nie ma danych o zachorowaniach na wirusowe zapalenie wątroby typu B w zdrowej populacji, wśród dzieci i dorosłych szczepionych co najmniej trzema dawkami szczepionki.
Szczepionkaprzeciwko wzw typu B wykorzystywana jest w ocenie zdolności odpowiedzi na swoiste antygeny. Według obecnych zaleceń u dzieci podejrzanych o niedobór odporności, które nie mają swoistych przeciwciał, po zaszczepieniu 1 dawką po 4 tygodniach ocenia się stężenie przeciwciał. Gdy nie uzyska się odpowiedzi poszczepiennej, wówczas próbuje się jeszcze raz, oceniając stężenie przeciwciał po drugiej dawce. Jeśli ponownie nie uzyska się odpowiedzi, nie podejmuje się kolejnych prób.
W przeciwieństwie do zdrowej populacji dzieci z obniżoną odpornością i z chorobami przewlekłymi (patrz obowiązkowe szczepień przeciwko pneumokokom) są szczególnie narażone na powikłania choroby zasadniczej w przebiegu zakażenia wirusem grypy i one przede wszystkim powinny być szczepione każdego roku.17 Jedyną szczepionką, która ma rejestrację w grupie dzieci z obniżoną odpornością i dzieci z wybranymi chorobami przewlekłymi (Program Szczepień Ochronnych na 2013 rok) jest szczepionka PCV13, zapewniająca ochronę przed inwazyjną chorobą pneumokokową u 81,5% dzieci do 2 roku życia, wg danych z KOROUN na 2011 rok. Szczepienia w grupach ryzyka dzieci do lat 5 są bezpłatne. Od bieżącego roku szczepionka PCV13 zarejestrowana jest w grupie dzieci do 17 roku życia, co ułatwi szczepienia wszystkich dzieci chorych z grup ryzyka.
Uwaga. Gdy szczepienie osoby z obniżoną odpornością jest niebezpieczne (szczepionki żywe) lub nieskuteczne (szczepionki inaktywowane), zalecane jest szczepienie osób z najbliższego otoczenia. Zalecane są szczepienia przeciwko: grypie, pneumokokom, meningokokom, odrze, śwince i różyczce, ospie wietrznej. Należy pamiętać, że dzieci zaszczepione żywą szczepionką polio przez 4-6 tygodni nie powinny kontaktować się z osobami z zaburzoną odpornością, gdyż wydalają w tym czasie żywy wirus szczepionkowy, a niemowlęta szczepione przeciwko rotawirusom przez 7 dni mogą być źródłem zakażenia.
Do zapamiętania
• Neutropenia autoimmunizacyjna najczęściej przebiega bezobjawowo i samoistnie ustępuje w pierwszych miesiącach życia.
• Gdy u dziecka z głęboką neutropenią wystąpi choćby jednorazowo wzrost liczby granulocytów, świadczy to z dużym prawdopodobieństwem o prawidłowej funkcji układu granulocytarnego.
• Brak neutrofilów we krwi obwodowej, szczególnie podczas banalnych zakażeń, oraz współistniejące poważne zakażenia są pilnym wskazaniem do biopsji szpiku. Biopsja szpiku rozstrzyga o przyczynie neutropenii.
• Niedobór IgA jest elementem fizjologicznego dojrzewania układu odporności. Izolowany brak lub niedobór IgA <0,07 g/l u dziecka w wieku poniżej 4 roku życia nie powinien budzić niepokoju.