Kontrola po leczeniu obejmuje powtarzalne badania obrazowe wykonywane zazwyczaj w schemacie 0, 1, 3, 6 i 12 miesięcy, w zależności od preferencji ośrodka. Z uwagi na dostępność i koszty najczęściej jest to wielofazowa, spiralna TK oceniająca zakres martwicy i zmniejszenie wymiarów zmiany. Przydatną metodą oceny jest też MR z kontrastem. Ocenę wyników leczenia można określać na podstawie kryteriów zawartych w Response evaluation criteria in solid tumors (RECIST). Ostatnio zmodyfikowano ten system z powodu dodatkowych danych charakterystycznych dla wspomnianej metody, takich jak krwiak w zmianie czy występowanie ognisk martwicy (nie zmniejsza to wymiarów zmiany, ale jest dowodem skuteczności ablacji). Dostępne są także wytyczne oceny skuteczności terapii wydane przez Światową Organizację Zdrowia (WHO – World Health Organization), skupiające się na ocenie zmian wymiarów leczonych guzów.
Kolejna metoda termicznej destrukcji nieoperacyjnych ognisk HCC to krioablacja. Jest ona dobrze tolerowana i ma niewielki odsetek działań niepożądanych. Do najczęściej opisywanych należą powikłania krwotoczne związane z brakiem efektu ablacji kanału przejścia sondy przez miąższ wątroby. W odróżnieniu od RFA monitorowanie zakresu krioablacji jest łatwiejsze dzięki wyraźniejszej granicy destrukcji zmiany.
Metodą z wyboru jest wielofazowa spiralna TK. Przy ocenie długofalowych efektów terapeutycznych ocenia się m.in. powrót unaczynienia będący dowodem na miejscowy nawrót choroby.16
Brachyterapia to metoda polegająca na aplikacji do guza pierwiastka promieniotwórczego, np. irydu 192 (192Ir), dostarczanego za pomocą sondy. Dawka promieniowania jest duża (>50 Gy), co daje dobry efekt terapeutyczny.17 Precyzję wprowadzenia sondy do zmiany zapewnia kontrola USG i obrazowanie 3D w tomografii komputerowej. Do nawigacji wykorzystuje się specjalne oprogramowanie.
Procedury brachyterapii służą głównie niszczeniu zmian wtórnych w wątrobie. Prowadzone są jednak badania oceniające skuteczność metody w przypadku HCC w marskiej wątrobie.18
Wyniki odległe wspomnianych metod są podobne. W celu poprawy skuteczności należy łączyć miejscową ablację zmian z leczeniem systemowym. Dlatego też w ośrodkach onkologicznych wykonuje się coraz więcej procedur łączonych. Aby uzyskiwać jak najlepsze wyniki leczenia, niezbędna jest ścisła współpraca między chirurgami, onkologami, radioterapeutami i radiologami.
Techniki endowaskularne
Chemoembolizacja zmian ogniskowych w wątrobie za pomocą cząstek nasączonych cytostatykiem (DEM-TACE)
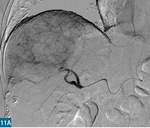
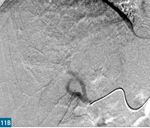
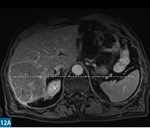
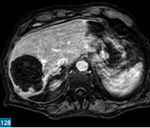
Wśród paliatywnych metod leczenia guzów wątroby istotne miejsce zajmuje chemoembolizacja przeztętnicza.19 Jest to zabieg wewnątrznaczyniowy polegający na zacewnikowaniu tętnicy wątrobowej wspólnej, a następnie na wybiórczym, selektywnym zamknięciu gałęzi tętniczych zaopatrujących guz przy użyciu cząstek embolizacyjnych nasączonych chemioterapeutykiem. Cząstkami embolizacyjnymi są mikrosfery (DEM – drug eluting microspheres) wykonane ze zmodyfikowanej skrobi. Cząstki te nasącza się chemioterapeutykiem bezpośrednio przed zabiegiem DEM-TACE. W przypadku zmian pierwotnych stosuje się doksorubicynę, a w przypadku zmian wtórnych – irynotekan. Zabieg skutkuje zmniejszeniem dopływu krwi tętniczej do guza, co z kolei prowadzi do niedokrwienia i martwicy. Jednoczesne selektywne dostarczanie chemioterapeutyku (uwalnianego stopniowo z mikrosfer) sprawia, że lek działa precyzyjnie, osiąga większe stężenia w okolicy guza, a ponadto jego działanie utrzymuje się dłużej niż w przypadku systemowej chemioterapii (ryc. 11).20 Zabieg wykonuje się 3-4 razy w odstępach 4-6-tygodniowych, a następnie przeprowadza się kontrolę za pomocą MR (ryc. 12). Skuteczność leczenia ocenia się według kryteriów Modified RECIST (mRECIST). Wyniki prezentowane w piśmiennictwie znacznie się od siebie różnią. Skuteczność tej metody nie budzi jednak wątpliwości. U większości leczonych nią pacjentów obserwuje się poprawę bądź stabilizację choroby, wydłuża się też czas przeżycia.21 Niestety część chorych nie kwalifikuje się do tego rodzaju leczenia. Czynniki wykluczające to: stopień C w skali Childa-Pugha, zakrzepica żyły wrotnej, guz przekraczający 70% miąższu wątroby oraz niewydolność nerek.
U pacjentów ze zmianami zarówno pierwotnymi, jak i wtórnymi leczenie można łączyć z innymi metodami paliatywnymi, np. RFA czy PEI.
Radioembolizacja zmian ogniskowych w wątrobie za pomocą mikrosfer zawierających radioaktywne izotopy
Radioembolizacja to zabieg, którego technika wykonania jest bardzo podobna do TACE. Różni się on natomiast mechanizmem działania przeciwnowotworowego. W obu typach zabiegów celem jest zacewnikowanie selektywne naczyń guza wątroby i podanie leku bezpośrednio do tych naczyń. W przypadku TACE efekt terapeutyczny uzyskuje się przede wszystkim przez wywołanie niedokrwienia guza i dodatkowe działanie miejscowe chemioterapeutyku. W radioembolizacji podaje się mikrosfery zawierające radioizotop jodu 131 (131I) lub itru 90 (90Y).22 Mikrosfery stosowane w radioembolizacji mają mniejszą średnicę niż te używane do TACE. Efekt embolizacyjny jest w tym przypadku minimalny, a skuteczność leczenia wynika przede wszystkim z miejscowego działania radioizotopu. Z tego powodu radioembolizację (w odróżnieniu od TACE) można wykonać w przypadku zakrzepicy żyły wrotnej.13 Skuteczność radioembolizacji została potwierdzona w licznych badaniach klinicznych, jednak ze względu na wysokie koszty oraz niedogodności logistyczne (konieczność współpracy z zakładem medycyny nuklearnej) nie jest to metoda szeroko stosowana i nie należy do standardowych terapii. Nie ma w piśmiennictwie dużych randomizowanych badań porównujących TACE i radioembolizację.